
利用喷雾干燥
实现 mRNA-LNP 的气管内递送
喷干应用
”
1
介绍
mRNA 疫苗是指将含有编码抗原蛋白的 mRNA 导入人体,直接进行翻译,形成相应的抗原蛋白,从而诱导机体产生特异性免疫应答,达到预防免疫的作用(图1)。
mRNA 疫苗的优势主要有:
研发周期短、抗原选择范围广,任何可成蛋白的抗原序列均可被选择
mRNA 疫苗的半衰期与免疫原性可通过修饰和递送系统来人工调节,由于不进入细胞核,无感染或插入突变的风险,安全性更高
多种修饰后的 mRNA 更稳定,在细胞质中被高效摄取和表达;mRNA 疫苗具备自我佐剂特点,因此表现更强的免疫原性,有效性更高
可通过体外转录技术快速、廉价地大规模生产 RNA 疫苗,在掌了病毒基因序列后即可在 40 天内完成疫苗样品的生产制备

▲ 图1. mRNA 疫苗通过转染抗原呈递细胞引起免疫
注射的 mRNA 疫苗被抗原呈递细胞内吞。
mRNA 脱离核内体进入细胞质后,被核糖体翻译成蛋白质。翻译的抗原蛋白可以通过几种方式刺激免疫系统。
细胞内抗原被蛋白酶体复合物分解成更小的片段,片段通过主要组织相容性复合体(MHC) I类蛋白在细胞表面展示给细胞毒性T细胞。
活化的细胞毒性T细胞通过分泌细胞溶解分子,如穿孔素和颗粒酶,杀死被感染的细胞。
此外,分泌的抗原可以被细胞摄取,在核内体内降解,并通过 MHC II 类蛋白在细胞表面呈递给辅助性T细胞。
辅助性T细胞通过刺激 B 细胞产生中和抗体,并通过炎症因子激活吞噬细胞,如巨噬细胞,促进循环病原体的清除。BCR:B 细胞受体;ER:内质网;TCR:T 细胞受体。
随着 COVID-19 的全球大流行,mRNA 疫苗已经作为一种新兴的疫苗技术进入市场,LNPs 是目前 mRNA 递送时克服体内给药时的许多胞外和胞内屏障的首选载体。然而大多数 LNP mRNA 疫苗需要严格控制的冷链基础设施。喷雾干燥是一种快速、可扩展且连续的过程,可生产室温稳定且适合吸入的细粉,并可以通过喷雾干燥工艺参数来控制粉末的物理性质。但喷雾干燥过程中,LNP 也要承受剪切应力、液体界面膨胀和收集过程中热脱水引起的应力。以下分享阿斯利康应用 BUCHI 小型喷雾干燥仪 B-290 实现脂质纳米颗粒实现对 mRNA 的气管内递送。
小型喷雾干燥仪 B-290

▲ 小型喷雾干燥仪 B-290
干燥参数 | _ |
入口温度 | 90℃ |
出口温度 | 54℃ |
抽气机效率 | 100% |
雾化气流 | 1850 L/h |
进料速率 | 2mL/min |
2
方法
该团队首先关注了磷脂和缓冲液对 LNP 本身温度敏感性的影响。由于 DSPC 的相变温度(Tm)为 55℃,接近喷雾干燥器的出口温度,而 DOPE 是一种不饱和磷脂,Tm 为 -16℃,可改善LNP的温度敏感性,并有研究发现 DOPE 替代 DSPC 可以提高 mRNA 递送效率[1]。LNP 中可电离脂质的 pKa=7,因此 pH 值的大幅变化可能会导致颗粒结构和稳定性的变化,该团队测试了广泛使用的 PBS 和 20 mM Tris 缓冲液的影响。该团队将四种不同的 LNP 配方(DSPC PBS;DSPC Tris;DOPE PBS;DOPE Tris)在不同温度范围孵育以模拟LNP配方和喷雾干燥过程的温度跨度。发现 DOPE Tris 组在高达 75℃ 的温度下仍保持稳定,并且在 80℃ 时仅损失约 20% 的 RNA。
在喷雾干燥的温度条件下更稳定不等于能更好地承受喷雾干燥过程,因此该团队还验证了 DOPE Tris LNP 能更好地承受喷雾干燥过程。DOPE Tris 组在喷雾干燥和复溶 306Oi10 和 MC3 LNP 时均增强了颗粒稳定性。 Tris 缓冲液在喷雾干燥方面优于PBS,虽然两种缓冲液的 pH 值都会随着温度的升高而降低,但 Tris 的变化率比 PBS 快 10 倍,这意味着Tris缓冲液从 25°C 升至 37°C 时 pH 将减少 0.3 个单位,而 PBS 仅减少 0.025 个单位,pH 值的降低可能会确保RNA仍被封装在LNP中。作者还发现优化的LNP配方(DOPE Tris)显著提高了评估了 LNP 在肝细胞癌细胞系 HepG2 和肺支气管细胞系 16HBE 中的摄取,与 4°C 下储存的液体 LNP 制剂相比,通过喷雾干燥处理并在室温下储存的 LNP 具有更好的稳定性、更高的颗粒封装效率以及更显著的蛋白质表达(图2)。

▲ 图2. 通过修改配方,以 DOPE 代替 DSPC、Tris 缓冲液代替 PBS,可以提高喷雾干燥后 LNP 的稳定性
(A) 使用 DSPC 和 PBS 生产的 LNP 制剂对温度升高敏感
(B) 当 DSPC 替换为 DOPE、PBS 替换为 Tris 时,喷雾干燥和重新分散后LNP颗粒的稳定性显著提高。
(C) LNP 制剂在喷雾干燥(SD)后稳定性提高,导致 mRNA 对 HepG2 和 16HBE 细胞具有良好转染效率。比例尺=100μm。**P<0.01、***P<0.001、****P< 0.0001、n.s=不显著。
该团队发现,当喷雾干燥 LNP 制剂时,在干燥塔内可观察到均匀的薄膜,在旋风分离器中可观察到薄膜沉积物,这是因为在无赋形剂的情况下,喷雾干燥 LNP 制剂中每种成分的固化机制将根据其扩散速率和溶解度而有所不同,引起各组分分离。因此该团队优化了 LNP、海藻糖、三亮氨酸的比例[2]。发现 LNP 与三亮氨酸的比例为 1:4 至 1:5 时,可以减少旋风分离器中的粉末损失,并进一步提高复溶后的 mRNA 封装效率,将 LNP 负载从 1.5% 增加到 5%。喷雾干燥后,通过 SEM 分析粉末粒径和表面结构,通过 CryoTEM 分析复溶的颗粒。发现喷雾干燥后复溶的 LNP 样品为尺寸范围变化更大的致密小囊泡(图3)。

▲ 图3. 喷雾干燥配方的优化
(A) 粉末配方中三亮氨酸(LLL):LNP 比例的优化可将旋风分离器中的损失降至最低,并随着重构后 RNA 封装效率 (%EE) 的增加而实现产量最大化。
(B) 喷雾干燥产生 LNP 的扫描电镜照片。当三亮氨酸(LLL)的浓度从 3% 增加到 15% 时,颗粒的形态逐渐从光滑的表面变成高度波纹状的表面。
(C) 新制 LNP 和喷雾干燥 LNP 代表性冷冻透射电子显微镜图片。与新鲜 LNP 相比,喷雾干燥 LNP 复溶后被包裹在致密的衬里。比例尺 =200nm。
接下来,该团队验证了 mRNA LNP 粉末制剂在体内的功能性递送。使用 Penn-Century Dry Powder Insufflator™-4 装置对动物进行给药,该装置可以将粉末直接输送到大鼠的肺部。肺组织切片上的免疫组化(IHC)显示出强烈的 eGFP 阳性细胞染色。这些细胞根据其定位、形态和免疫荧光标记被鉴定为细支气管上皮细胞、II 型肺细胞和/或巨噬细胞。尽管仅识别出少数 eGFP 阳性细胞,但这些阳性细胞的染色强烈、且无背景噪点,表明 eGFP mRNA LNP 在喷雾干燥后吸入给药,可在肺部产生清晰的 eGFP 表达。
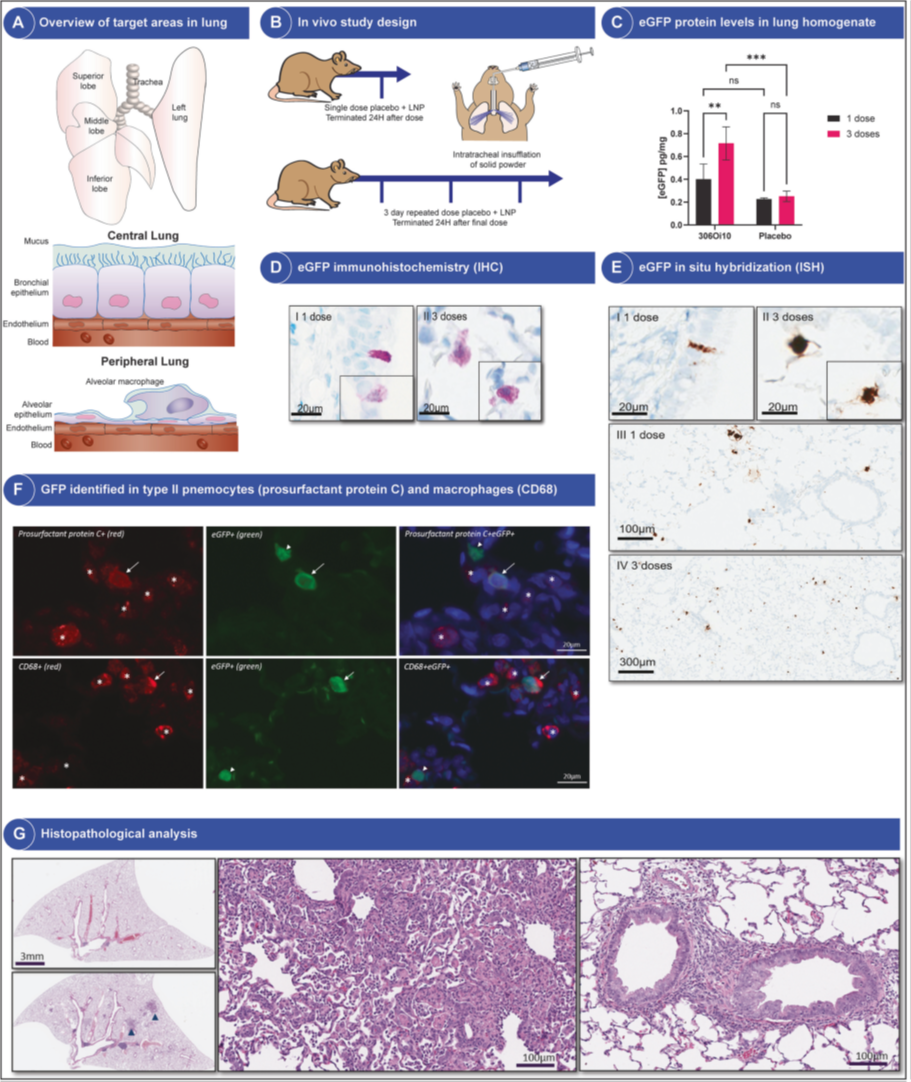
▲ 图4. 肺中的体内摄取和蛋白质表达
(A) 大鼠肺示意图
(B) 研究设计的示意图。
单次给药后 24 小时或连续3天每日给药后 24 小时处死大鼠。给药方式包括气管内(IT)滴注含有 eGFP mRNA LNP 的喷雾干燥制剂或安慰剂。
(C) 在右肺叶的肺匀浆中测量的 eGFP 蛋白水平
(D) 显示 eGFP 阳性细胞(紫色)的图像
(E) IT 滴注单次(I和III)和 3 天重复(II和IV)给药后 24 小时在大鼠左肺叶中检测到的 eGFP(棕色)。eGFP 阳性细胞(紫色)形态学上鉴定为细支气管上皮细胞 (D I) 和 II 型肺细胞和巨噬细胞 (D II)。在细支气管上皮细胞(E I)和 II 型肺细胞和巨噬细胞(E II)中鉴定出 eGFP mRNA (棕色)。
(F) eGFP 的免疫荧光标记与 II 型肺细胞或巨噬细胞标记物结合,证实两种细胞类型都表达 eGFP。
(G) 左肺叶的组织病理学分析结果。
左上:来自对照大鼠的肺组织,显示没有病变。
左下:治疗 3 天的大鼠肺组织,显示肺泡实质中的实变区域,代表炎症病变(箭头)。
中图:混合炎症细胞浸润区域的较高放大倍数,以较小的气道和描绘肺泡管为中心。
右图:代表次级细支气管上皮变化的图像。
3
结论
总的来说,该研究团队进行了一项概念验证研究,并成功通过配方优化,设计出了用于吸入的 mRNA LNP 喷雾干燥制剂。该制剂在经过喷雾干燥和复溶后仍保持功能,并可在体外和体内有效递送 mRNA,能够以临床相关剂量水平实现 LNP 的肺部给药,在吸入式 mRNA 疫苗领域开辟了新道路,具有巨大前景。
小型喷雾干燥仪 S-300


▲ 小型喷雾干燥仪 S-300
▲ 惰性气体循环装置 S-395
BUCHI 小型喷雾干燥仪 S-300 搭配惰性气体循环装置 S-395,构建完美闭环体系,创造低氧环境,轻松处理您的 mRNA 样品。
4
参考文献
Chaudhary, N., Weissman, D. & Whitehead, K.A. mRNA vaccines for infectious diseases: principles, delivery and clinical translation. Nat Rev Drug Discov 20, 817–838 (2021).
Friis K P, Gracin S, Oag S, et al. Spray dried lipid nanoparticle formulations enable intratracheal delivery of mRNA[J]. Journal of Controlled Release, 2023, 363: 389-401.

长按上方二维码联系我们
或拨打联系电话:
400 - 880 - 8720
微信公众号
步琦智慧实验室
淘宝官方旗舰店
瑞士步琦