普通的聚丙烯酰胺凝胶电泳只能通过片段大小不同在同一浓度的胶上电泳迁移率不同而分离不同的DNA片段,对于片段大小接近或相同的DNA片段无法做到有效地分离;DGGE(denaturing gradient gel electrophoresis) 即变性梯度凝胶电泳,是利用DNA在不同浓度的变性剂中解链行为的不同而导致电泳迁移率发生变化,从而将片段大小相同而碱基组成不同的DNA片段分开。
DGGE作为一种成熟的分子生物学技术被广泛应用于环境科学(土壤、海洋、河流、冰川、淤泥等)、医学(各种疾病治疗前后,病变部位微生物的差异)、人体(鼻咽、口腔、黏膜、肠道)等领域进行微生物多样性分析。
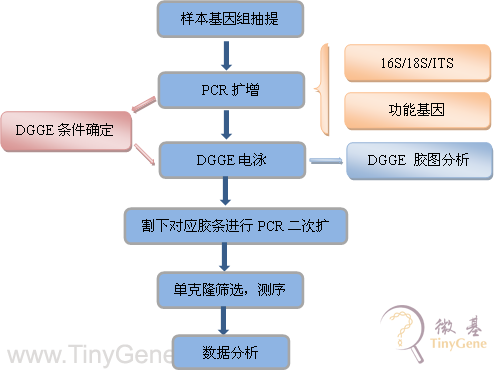
实验结果包括以下内容
以下是DGGE中常用的引物,我们将根据客户的不同需求,进行针对性的引物设计。
| 引物 | 序列(5’-3’) | |
| 细菌 16S V3区扩增引物 |
357-F-GC | CGCCCGCCGCGCGCGGCGGGCGGGGCGGGG GCACGGGGGGCCTACGGGAGGCAGCAG |
| 518r | ATTACCGCGGCTGCTGG |
| 引物 | 序列(5’-3’) | |
| 真核 18S V1-3区扩增引物 |
Euk1A | CTGGTTGATCCTGCCAG |
| EukA516r-GC | CGCCCGGGGCGCGCCCCGGGCGGGGCGGGGGCA CGGGGGGACCAGACTTGCCCTCC |
针对客户的样本来源不同,我们针对性优化不同的基因组抽提方法,已达到提取效果zei佳。
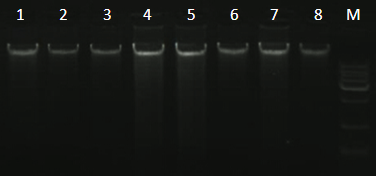
说明:1-8为样本所抽提基因组DNA,上样量3uL;M为1kb Marker上数第一条带为8 kb,中间的亮带为3kb,浓度为30ng/uL,其余为10 ng/uL。

说明:1-8为样本,负为负对照(说明我们的实验没有污染,这对分子实验是至关重要的),上样量为5uL;M为DL2000 Marker,上样量3uL。其中亮带为20ng/uL,其余为10 ng/uL。
Reconditioning PCR:
第一轮PCR产物将会作为新的模板再进行少数循环的第二轮PCR扩增,这叫做“Reconditioning PCR”。由于在“ Reconditioning PCR”的过程中引物和模板之间的比例始终保持在较高的水平上,因此可以保证引物与模板之间的退火要优先于不同模板之间的退火,消除异源双链(Heteroduplex)污染对于PCR-DGGE图谱的观察和分析。
参考文献:
(1)Heteroduplexes in mixed-template amplifications: formation, consequence and elimination by “reconditioning PCR”. 2002. Nucleic Acids Research.
(2)不同外源扰动因素对肠道菌群组成结构影响的研究. 上海交通大学 2008 届博士学位论文.
4.3微生物多样性指数

4.4 UPGAM法进行样品间的聚类分析图

常见聚类分析方法有Neighbor Joining、single linkage、complete linkage、upgama、wpgama、centroid、median、ward’s
4.5微生物群落的多维定标分析
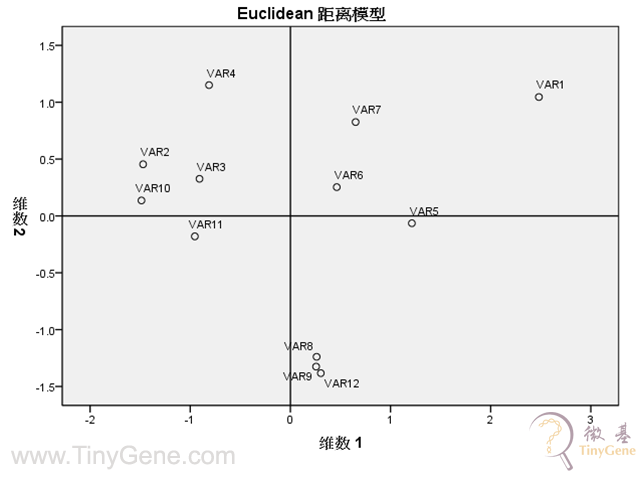
4.6 主成分分析(PCA, Principal Component Analysis)
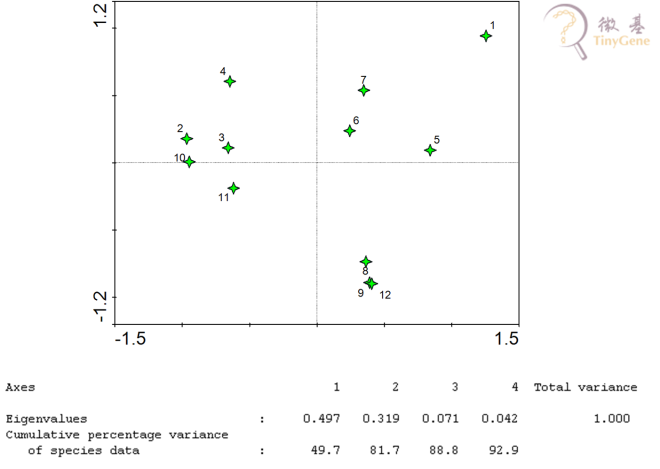
4.7 冗余分析(RDA, Redundancy Analysis)

6.1 二扩电泳检测
分别取5 μL PCR产物,于1%琼脂糖凝胶电泳检测。琼脂糖凝胶电泳检测结果如下图所示
电泳检测结果显示:PCR产物条带单一,片段大小正确,可进行胶回收。
6.2 胶回收
采用AXYGEN 公司的 AxyPrepDNA 凝胶回收试剂盒回收 PCR 产物,取3 μL回收产物进行电泳检测。
6.3 TA连接及转化
PCR产物的克隆使用 BioLinker的pED-T载体试剂盒。
6.4 阳性克隆的筛选及测序
在平板上随机挑取8个克隆摇菌,菌液进行M13检测,挑取3个阳性克隆进行测序。
7.1 fasta文件
全部测序结果进行整理,去除载体序列,将其整理为fasta格式的序列文件,为后续分析做准备。

7.2克隆子一致性分析(Alignment比对)
一般每个条带送三个克隆子进行测序,那么三个克隆子所测序列的一致性如何,我们通过clonemanager软件进行序列性的分析,如果克隆子的测序结果完全一致,那么会以绿色的覆盖形式表示,若是序列不一致,会是白色区域。如下图所示:
| 条带编号 |
克隆子编号 |
菌株名称 | GenBank序列号 | zei大相似度(%) | 条带占比(%) |
| 1 | 3 | Winogradskyella ulvae strain KMM 6390 | NR_109172.1 | 91 | 67 |
| 7 | Polaribacter irgensii strain 23-P | NR_044733.1 | 99 | 33 | |
| 2 | 4 | Cyanothece sp. ATCC 51142 strain ATCC 51142 | NR_074316.1 | 93 | 33 |
| 5 | Clostridium populeti strain 743A | NR_026103.1 | 99 | 33 | |
| 7 | Candidatus Pelagibacter ubique HTCC1062 strain HTCC1062 | NR_074224.1 | 100 | 33 | |
| 3 | 3 | Paraprevotella clara YIT 11840 | NR_041626.1 | 100 | 67 |
| 8 | Flavobacterium limicola strain ST-82 | NR_024787.1 | 97 | 33 | |
| 4 | 1 | Bacteroides vulgatus ATCC 8482 strain ATCC 8482 | NR_074515.1 | 100 | 100 |
| 5 | 1 | Bacteroides fragilis YCH46 strain YCH46 | NR_074839.1 | 99 | 100 |
| 6 | 1 | Bacteroides gallinarum strain JCM 13658 | NR_041448.1 | 98 | 100 |
| 7 | 1 | Megamonas rupellensis strain FM1025 | NR_044473.1 | 97 | 100 |
优点:1. 高效,理论上可以分离开一个碱基差异的DNA片段。
2. 方便,不用对样品进行标记
3. 快速,对于已知DGGE条件的样品,可在短时间能获取DGGE图谱
4. 直观,DGGE图谱可直观的反应出样品中个组分的丰富度
5. 稳定,DGGE作为一种成熟的技术,可重复性高
6. 可多样本同时分析,展现各样本的差异
缺点:1. 仅能检测样本中的主要微生物,占总量1%以上的微生物才能被检测到。
2. DGGE只能对200-700bp的片段有效地分离,过大或者过小的片段分离效果都不是很好。
3. 因为仪器数值有上限,对于某些某种主要菌株占比较大又要展现大部分条带的样品,通过DGGE图谱不能很好的反映出各个菌株的丰富度。
4. 不同序列的DNA有可能发生共迁移而导致某些条带会有多种不同的DNA片段
5. 因为某些物种的基因不同拷贝之间存在异质性,即使一个碱基的差别都会使他们分开,而导致不同的条带是相同物种。
6. DGGE技术对微生物的分类鉴定依赖于基因数据库,若数据库中基因序列信息不够丰富,将会限制DGGE的使用。
7. 由于某些种类的16S rDNA不同拷贝之间的多态性问题,可能导致自然群落中细菌数量的过多估计。
1) 请提供浓度大于10ng/uL,总量大于500ng的基因组DNA,DNA纯度较差或降解严重会影响后继的扩增实验。如果方便的话,可提供电子版DNA电泳检测照片及OD260/280比值。
2) 样品在保存期间避免反复冻融。
3) 送样务必标清楚样品编号,并用parafilm膜对管口进行密封。
4)请务必填写完整的送样订单,并用自封袋密封后同样品一起送样,以便收到样品后妥善保存。
1)送样样品尽量保证新鲜,为了防止微生物死亡或DNA降解,采样后建议立即冰冻保存,如样本极为珍贵,建议采用液氮速冻后-80℃冰箱保存。
2)样品在保存期间避免反复冻融。
3)若是样品中含有大量的腐殖质酸、重金属等PCR反应抑制剂,请在送样时注明。
4)请务必填写完整的送样订单,并用自封袋密封后同样品一起送样,以便收到样品后妥善保存。
送样条件:
以上两种类型的样本,送样时采用干冰保存运输;若是距离较远,建议采用干冰加冰袋,存放于冰盒中。
土壤:3-5 g(干沙土、干粘土、农田土、堆肥、底泥、泥炭土、淤泥等)
粪便:3-5 g
肠道内容物:3-5 g
动物组织:3-5g(鳃、胃粘膜、肠粘膜、口腔黏膜等)
分泌物:2-3 mL(唾液、鼻涕、汗液、泪水等)
水样:2L以上水过滤后的滤膜,若环境中微生物丰富,可适当减少水的体积。
植物内生菌:10-20g叶片;3-5g根系。
血液:10mL。
叶片:50-100g
其他来源的样品请垂询。
以上用PP材料的epp管或螺口管盛装即可。