2024-03-12 15:39

文章来源:工程菌星球
导读:目前,我国兽用生物制品主要以家畜与家禽的活疫苗和灭活疫苗为主。据报道,2021年,我国动物疫苗的产量和需求量分别达4.85万吨和4.96万吨,市场均价为33.36万元/吨,市场规模达165.4亿元,随着国内养殖业规模化程度逐步提高,未来中国动物疫苗市场需求有望进一步增长,预计2023年中国动物疫苗需求量将达到5.26万吨,市场规模将达到189.64亿元。随着mRNA技术在人体内获得的巨大成功,并且有着诸多优势,例如,开发速度快、成本低廉、无须复杂的下游纯化工艺等,人们开始考虑将mRNA技术引入到兽用疫苗领域。
事实上,目前关于mRNA疫苗在动物传染病疫苗方面的基础研究非常少,但是,新冠mRNA疫苗的巨大成功以及当前mRNA技术的蓬勃发展,使得人们看到mRNA技术在兽医领域的广泛应用前景。病毒感染仍然是全球健康和工业畜牧业生产的主要威胁。缺乏有效控制策略的家禽和牲畜主要病毒包括非洲猪瘟病毒、猪繁殖与呼吸综合征病毒(PRRSV)、猪流行性腹泻病毒(PEDV)、口蹄疫、牛病毒性腹泻病毒(BVDV)、结节性皮肤病病毒(LSDV) 、牛白血病病毒(BLV)、小反刍兽疫病毒(PPRV)等。疫苗接种是动物健康的基石,在畜牧业经营中至关重要。许多毁灭性的牲畜疾病可以通过疫苗接种来预防,但由于多种原因,尚未开发出针对一些最具毁灭性疾病的兽用疫苗。基于 mRNA 疫苗平台的开发可能会战略性地将安全有效的兽用疫苗推向市场,以预防这些畜牧疾病。
一、国外兽用mRNA疫苗行业发展
2023年11月11号,默沙东动物保健公司宣布 Sequivity IAV-S NA(猪流感疫苗,N1 和 N2,RNA 颗粒)疫苗现已成为其猪产品组合的商业部分。该公司于 2022 年获得美国农业部(USDA)对该疫苗的许可批准。这是第一种仅使用流感神经氨酸酶(NA)表面抗原为猪接种H1N1、H1N2和H3N2流感病毒株的商业疫苗。疫苗中的 NA RNA 颗粒是使用默沙东动物保健公司的创新SEQUIVITY平台技术生产的,该技术此前已用于针对现有和新兴的猪病原体。作为一个革命性的猪疫苗平台,SEQUIVITY 利用RNA颗粒技术来创建针对猪甲型流感病毒株、猪圆环病毒 (PCV)、轮状病毒等的定制处方疫苗。此外,位于爱荷华州艾姆斯的初创动物疫苗公司Genvax Technologies也专注于开发用于预防和治疗动物疾病的新型mRNA疫苗。
二、国内兽用mRNA疫苗行业起步
从去年开始,国内一批嗅觉敏锐的RNA疫苗创新企业开始寻求与传统的兽用生物制品研发生产企业合作,为抢先进入兽用mRNA疫苗市场做好充足的准备:
•2023年4月18日,苏州科锐迈德与申联生物签订动物mRNA疫苗及药物合作项目,致力于将科锐迈德的环状mRNA技术平台优势与申联生物兽用生物制品产业化开发及商业化运作等深度融合,加快推进mRNA平台技术在兽用生物制品领域产业化进程及市场化应用。
•2023年12月11号,蓝鹊生物宣布携手金宇生物共同研发创新非洲猪瘟mRNA疫苗。早在2019年,蓝鹊就同金宇生物展开战略合作,打造兽用mRNA 疫苗联合开发平台。根据本次签订的《非洲猪瘟mRNA疫苗合作开发协议》,他们将会围绕非洲猪瘟mRNA疫苗抗原筛选、结构优化、递送材料、工艺质控进行深入研究,合作开发安全、有效的非洲猪瘟mRNA疫苗。重要的是,蓝鹊称两家公司合作开发的非洲猪瘟mRNA疫苗研发已取得阶段性成果。
•2024年1月8日,江苏申基同瑞普生物共同签署猫HCPC四联mRNA疫苗合作开发协议,共同研究开发猫鼻气管炎、杯状病毒病、泛白细胞减少症、猫衣原体四联 mRNA疫苗,利用mRNA技术进军宠物疫苗市场。

图片来源:《2023年中国兽药行业全景图谱》
三、兽用mRNA疫苗基础研究
3.1 非洲猪瘟疫苗
非洲猪瘟病毒 (ASFV) 是一种高传染性的双链DNA病毒,可导致非洲猪瘟,感染后发病率和病死率可高达100%,目前尚无针对该病毒感染安全有效的商用疫苗和治疗药物,对于猪养殖业来说是一种毁灭性疾病。在2019年,非洲猪瘟病毒造成我国700万头生猪死亡,而且,由于缺乏有效的疫苗,非洲猪瘟已蔓延到许多国家。研究者将多种毒力基因删除,开发出ASFV 减毒活疫苗,并且已经证明可有效防止致命的 ASFV 感染。这些减毒疫苗的大规模生产很大程度上依赖于原代猪肺泡巨噬细胞或骨髓细胞的获取,这是耗时和成本高昂的。最近,通过名为 iVAX 的计算疫苗设计平台在 ASFV 编码蛋白中鉴定出了高度保守的细胞毒性 T 细胞表位。随后开发了一种含有预测的猪 MHC I 类和 II 类表位的 T 细胞定向 ASF DNA 疫苗,并且正在评估这种新型疫苗的免疫原性。鉴于与 DNA 疫苗拥有整合到宿主基因组中的潜在风险,基于 mRNA 的疫苗方法有可能改进安全有效的非洲猪瘟疫苗。值得注意的是,ASFV 双链 DNA 基因组大约有 170-194 个碱基对,编码 150-170 个开放阅读框,其中几乎一半缺乏任何已知或可预测的功能。进一步的研究可能会鉴定出更多潜在的 T 细胞表位,以促进开发具有更大表位宽度的 T 细胞定向 mRNA 疫苗。
3.2 猪流行性腹泻病毒疫苗
猪流行性腹泻病毒(PEDV)是猪流行性腹泻(PED)的主要病原体,可引起以腹泻、呕吐和脱水为特征的严重肠道疾病。新生仔猪特别容易感染 PEDV,死亡率高达 100%。2010年以来,高致病性PEDV变异株逐渐渗透到猪群中,在全球范围内造成了巨大的经济损失。迄今为止,PEDV 仍然是威胁养猪业的一个主要隐患。
PEDV 是一种正义、单链、有包膜 RNA 病毒,属于冠状病毒科。病毒颗粒表面的 S 糖蛋白在与宿主的相互作用中起着至关重要的作用,它负责宿主细胞受体的结合以及随后与宿主细胞膜的融合 。由于 S 蛋白含有多个中和表位,是中和抗体的主要靶标,因此它是主要免疫原,也是疫苗开发的理想抗原靶点 。
2022年12月1号,石河子大学动物科技学院陈创夫在《生物工程学报》发表文章:猪流行性腹泻mRNA疫苗的制备与免疫原性评价,他们制备了两种PEDV RBD mRNA-LNP,分别为RBD单体(RBD-M)和RBD异源二聚体(RBD-D),证明了RBD二聚体mRNA疫苗在小鼠体内具有良好的免疫原性。在妊娠母猪产前7周先用减毒灭活疫苗免疫,4周后分别用RBD-D mRNA疫苗或者灭活疫苗加强免疫,结果显示RBD-D mRNA疫苗与灭活疫苗加强免疫后可诱导相近的抗体水平。
PEDV mRNA疫苗抗原设计和妊娠母猪内抗原免疫性评价
2024年1月17号,江苏省农业科学院兽医所李彬研团队在mBio发表文章:PEDV-spike-protein-expressing mRNA vaccine protects piglets against PEDV challenge,他们设计了两种mRNA疫苗抗原:一种是编码全长 PEDV Spike蛋白(S),一种是多表位嵌合Spike蛋白(Sm)。结果发现,S mRNA-LNP 疫苗在诱导小鼠抗体和细胞免疫反应方面优于 Sm mRNA-LNP 疫苗。对 S mRNA 疫苗在仔猪中的免疫原性和功效的评估证实,它在体内诱导了强烈的 PEDV 特异性体液和细胞免疫反应。重要的是,S mRNA-LNP疫苗不仅可以保护主动免疫的仔猪免受PEDV的侵害,而且可以在母猪免疫后以初乳衍生抗体的形式为新生仔猪提供有效的被动抗PEDV免疫力。这研究结果表明,PEDV-S mRNA-LNP 疫苗是对抗 PEDV 感染非常有希望的候选疫苗。
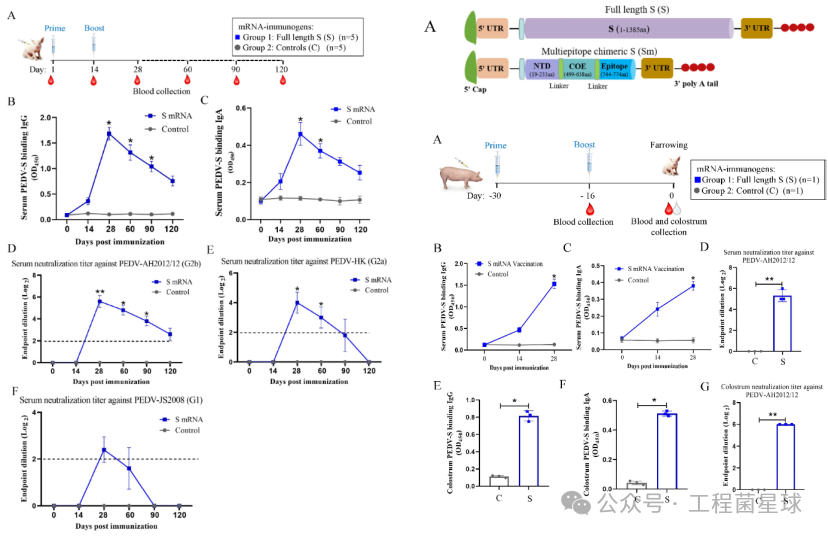
PEDV-S mRNA-LNP 疫苗在仔猪和母猪中均可触发强烈的中和抗体反应
3.3 猪繁殖与呼吸综合征病毒疫苗
猪繁殖与呼吸综合征病毒(PRRSV)是一种高度变异的RNA病毒,感染会引起仔猪呼吸道疾病和母猪繁殖障碍,给养猪业造成巨大经济损失。目前,PRRS的猪感染控制主要依赖于改良活病毒疫苗或灭活病毒疫苗接种。不幸的是,目前可用的疫苗仅提供针对同源毒株的保护,而对在野外传播并不断突变的异源毒株提供弱或没有能力提供交叉保护。这种高度的遗传和抗原多样性是控制PRRS的主要障碍。此外,在广泛使用减毒活疫苗的中国和美国的养猪场中都发现了来自疫苗的PRRSV毒株,引发了人们对现有减毒疫苗安全性的担忧。与减毒活疫苗相比,PRRSV 灭活疫苗安全得多,但接种疫苗的猪对于预防病毒感染效果较差。因此,迫切需要一种安全有效的疫苗来控制PRRSV。
考虑到PRRSV 的抗原和遗传多样性,使用 mRNA 技术的嵌合抗原疫苗方法可能提供一种潜在的解决方案。2019 年,一种含有 PRRSV GP5-Mosaic 序列的候选 DNA 疫苗被证明具有免疫原性,并能诱导猪免受病毒感染。PRRSV 编码区中能够有效引发免疫反应的片段可以通过计算机算法从多种流行毒株中选择出来,然后使用 mRNA 疫苗平台组装成单一疫苗。这种编码合成嵌合抗原的疫苗应该诱导更多样化、更有效、具有更大变异深度的免疫反应。
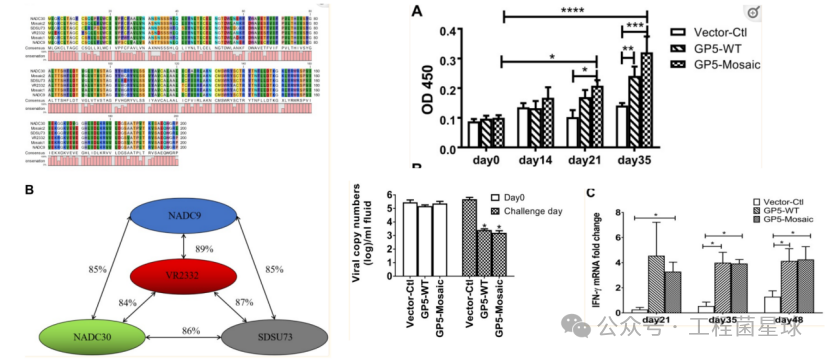
左图:GP5氨基酸序列比对
右图:PRRSV GP5-Mosaic DNA疫苗触发的体液免疫与细胞免疫
3.4 牛呼吸道合胞病毒
牛呼吸道合胞病毒(BRSV)是一种与人呼吸道合胞病毒(RSV)密切相关的肺病毒,是牛呼吸道疾病的常见原因,尤其是犊牛。它是一种负义单链 RNA 病毒,可在细胞质内复制。与其他单链RNA病毒一样,BRSV基因组突变率较高,导致抗原变异较大。最近显示 Prefusion F 免疫奶牛对于预防BRSV感染非常有效,然而,生产预融合构象 F蛋白的困难及其生产成本是蛋白疫苗无法普及农场使用的障碍。爱荷华州立大学兽医微生物学和预防医学助理教授 David Verhoeven 是一位多年来一直致力于疫苗制造的研究员。他正在开发BRSV mRNA疫苗,用于诱导预防BRSV 感染的免疫保护。
四、小结
mRNA技术在兽用疫苗领域拥有巨大潜力,凭借诸优点,可以克服传统疫苗的瓶颈,例如,无感染或毒力回复的风险、可同时免疫多种病原体、设计相对容易,研发速度快,生产成本低等优点。然而,目前,兽用mRNA疫苗的产业化之路才刚刚起步,相关的基础研究也非常薄弱,需要克服的困难还有很多。肌肉内、皮内或皮下注射是mRNA疫苗在人体中的主要递送途径。为了减少疫苗接种的压力、疼痛和成本,非侵入性给药途径,包括口服给药和气雾剂给药,正在成为动物疫苗的首选途径。因此,新载体的设计应有助于提高非侵入性递送途径的mRNA疫苗的功效和稳定性。此外,需要在天然动物宿主中评估 mRNA 疫苗递送引起的不良事件和过敏反应。总的来说,由于mRNA技术的飞速发展,特别是在免疫信息学和体内递送方法领域,低成本、高质量的mRNA疫苗在兽医领域的前景非常光明。

eGFP mRNA和mCherry mRNA在293T细胞中实现高表达
参考文献
[1] 智研咨询.《2023-2029年中国动物疫苗行业市场调查研究及发展前景展望报告》.
[2] Le T, Sun C, Chang J, Zhang G, Yin X. mRNA Vaccine Development for Emerging Animal and Zoonotic Diseases. Viruses. 2022 Feb 15;14(2):401. doi: 10.3390/v14020401.
[3] 杨利敏, 王俊虹, 徐明国, 王虎, 张晓娟, 刘文军, 陈创夫. 猪流行性腹泻mRNA疫苗的制备与免疫原性评价[J]. 生物工程学报, 2023, 39(7): 2624-2633.
[4] Zhao Y, Fan B, Song X, Gao J, Guo R, Yi C, He Z, Hu H, Jiang J, Zhao L, Zhong T, Li B. PEDV-spike-protein-expressing mRNA vaccine protects piglets against PEDV challenge. mBio. 2024 Jan 17:e0295823. doi: 10.1128/mbio.02958-23.
[5] Cui J, O''Connell CM, Costa A, Pan Y, Smyth JA, Verardi PH, Burgess DJ, Van Kruiningen HJ, Garmendia AE. A PRRSV GP5-Mosaic vaccine: Protection of pigs from challenge and ex vivo detection of IFNγ responses against several genotype 2 strains. PLoS One. 2019 Jan 31;14(1):e0208801. doi: 10.1371/journal.pone.0208801.