电解法制烧碱的原料是饱和食盐水,由于粗盐中含有泥沙和Ca2+、Mg2+、Fe3+、SO42- 杂质,不符合电解要求,因此必须经过精制.某校实验小组精制粗盐水的实验过程如下: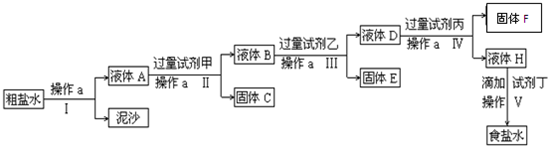
1)操作a的名称是过滤
过滤
,所用玻璃仪器有烧杯、漏斗、玻璃棒
烧杯、漏斗、玻璃棒
;
(2)在Ⅱ步中,加入过量试剂甲后,生成了两种大量的难溶沉淀,则试剂甲为NaOH
NaOH
(填化学式)溶液;
(3)写出固体H所含物质的化学式BaCO3、CaCO3
BaCO3、CaCO3
;
(4)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的;
溶解时:加快溶解
加快溶解
.
过滤时:引流
引流
.
蒸发时:搅拌避免局部受热液体飞溅
搅拌避免局部受热液体飞溅
.考点:粗盐提纯;物质分离和提纯的方法和基本操作综合应用.专题:实验题.分析:流程是操作Ⅰ通过过滤除去不溶性杂质,得到溶液中含有杂质离子Ca2+、Mg2+、Fe3+、SO42-杂质,加入过量试剂甲为氢氧化钠沉淀铁离子和镁离子,过滤得到溶液中含有Ca2+、OH-、SO42-杂质,加入过量试剂乙为氯化钡沉淀硫酸根离子,过滤得到溶液中含有OH-、Ca2+、Ba2+加入过量碳酸钠溶液,除去Ca2+、Ba2+,过滤得到溶液中含有氢氧根离子、碳酸根离子,加入适量盐酸到不再有气体产生得到较纯净的食盐水;
(1)操作a是通过过滤除去不溶性杂质的操作,实现固体和溶液分离的方法是过滤,依据过滤装置回答需要的仪器;
(2)粗盐中含有Ca2+、Mg2+、Fe3+、SO42-杂质,加入过量试剂氢氧化钠后,可以将镁离子以及铁离子沉淀,试剂甲为氢氧化钠溶液;
(3)流程中Ⅳ操作是加入过量碳酸钠溶液用来除去钙离子和过量钡离子,溶液中钙离子、过滤钡离子加入碳酸钠溶液沉淀除去;
(4)溶解是加快溶解,过滤是引流作用,蒸发是搅拌避免局部受热液体飞溅.解答:解:(1)在食盐水中,实现溶液和泥沙难溶物的分离可以采用过滤的方法,故答案为:过滤;
(2)粗盐中含有Ca2+、Mg2+、Fe3+、SO42-杂质,加入过量试剂氢氧化钠后,可以将镁离子以及铁离子形成氢氧化镁和氢氧化铁沉淀,故答案为:NaOH;
(3)氯化钡可以让硫酸根离子形成硫酸钡沉淀,碳酸钠可以让钙离子以及过量的钡离子形成碳酸钙和碳酸钡沉淀,并且碳酸钠必须加在氯化钡之后,在第Ⅴ步中,加入试剂盐酸可以讲过量的氢氧化钠以及过量的碳酸钠除掉;故答案为:CaCO3和BaCO3;
(4)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,软件工程是为了加快物质溶解,过滤是利用玻璃棒引流作用把需呀阿噢过滤的混合物进入过滤器,蒸发过程玻璃棒不断搅拌,避免局部受热引起液体飞溅,故答案为:加快溶解,引流,搅拌避免液体飞溅.点评:本题考查了常见物质的分离方法和提纯,物质分离是现在考试的重点和热点,可以根据所学知识进行回答,难度不大