7 分析步骤
7.1样品前处理
7.1.1方法1(AOAC方法)
准确称取15g(精确至0.01g)均质样品于50mL离心管中,加入15mL 1%乙酸乙腈(4.7),加入提取包P-QuEChERS-AOAC1202(4.6)后剧烈振摇1min,4000r/min离心5min。用一次性注射器(5.7)取1mL上清液(再吸入1mL空气),匀速通过多功能针式过滤器F-QuEChERS-AOAC3202(5.8)至进样小瓶中(使液体逐滴流出),上机测定。
1) 常规水果蔬菜:
采用F-QuEChERS-AOAC3201,内含150mgMgSO4、50mgPSA;
2) 含色素的水果蔬菜:
采用F-QuEChERS-AOAC3206,内含150mgMgSO4、50mgPSA、5mgGCB;
3) 含脂肪和蜡质的水果蔬菜:
采用F-QuEChERS-AOAC3202,内含150mgMgSO4、50mgPSA、50mgC18;
4)含色素和脂肪的水果蔬菜:
采用F-QuEChERS-AOAC3203,内含150mgMgSO4、50mgPSA、50mgC18、5mgGCB。
7.1.2方法2(EN方法)
准确称取10g(精确至0.01g)均质样品于50mL离心管中,加入10mL乙腈(4.1),加入提取包P-QuEChERS-EN1101(4.6)后剧烈振摇1min,4000r/min离心5min。用一次性注射器(5.7)取1mL上清液(再吸入1mL空气),匀速通过多功能针式过滤器F-QuEChERS-EN3102(5.8)至进样小瓶中(使液体逐滴流出),上机测定。
1)常规水果蔬菜:
采用F-QuEChERS-EN3101,内含150mgMgSO4、25mgPSA;
2)含色素的水果蔬菜:
采用F-QuEChERS-EN3106,内含150mgMgSO4、25mgPSA、5mgGCB;
3)含脂肪和蜡质的水果蔬菜:
采用F-QuEChERS-EN3102,内含150mgMgSO4、25mgPSA、25mgC18;
4)含色素和脂肪的水果蔬菜:
采用F-QuEChERS-EN3103,内含150mgMgSO4、25mgPSA、25mgC18、5mgGCB。

7.2标准曲线绘制
取空白试样按7.1处理方法制备空白基质溶液,然后准确量取适量56种和23种农药及其代谢物混合标准工作溶液(4.11),用空白基质溶液稀释配制成浓度为1μg/L、2μg/L、5μg/L、10μg/L、25μg/L、50μg/L、100μg/L、200μg/L的系列基质匹配标准工作溶液,供液相色谱-串联质谱和气相色谱-串联质谱测定。分别以68种农药及其代谢物的定量离子质量色谱峰面积为纵坐标,对应的基质匹配标准溶液浓度为横坐标,绘制标准曲线,求回归方程和相关系数。
7.3测定
7.3.1液相色谱-串联质谱参考条件
液相色谱参考条件
a)色谱柱:XDB C182.1×150mm,3.5μm,或性能相当者;
b)流速:0.4mL/min;
c)流动相:A为5mM甲酸铵水溶液,B为5mM甲酸铵甲醇溶液
d)进样量:10μL;
流动相梯度洗脱程序见表1:
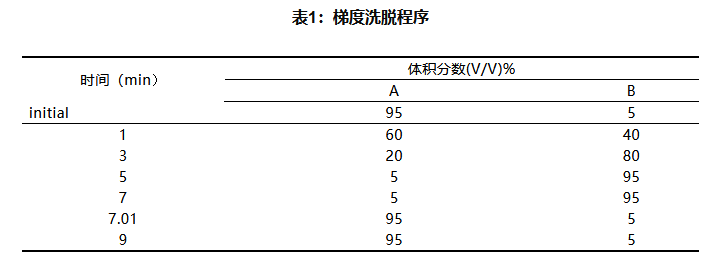
质谱参考条件
a)离子源:电喷雾离子源(ESI);
b)扫描方式:正、负离子扫描;
c)质谱扫描方式:多反应离子监测(MRM)
d)离子源温度:550℃;
e)离子源喷雾电压:5500V;
f)气帘气:30psi;
g)雾化气:60psi;
h)干燥气:60psi;
i)碰撞气:8psi;