内容
一.法规要求
二.分析方法验证
三.分析方法确认
四.分析方法验证和确认总结
一.法规要求:新版GMP(2010年修订)
第二百二十三条 物料和不同生产阶段产品的检验应当至少符合以下要求:
(一)企业应当确保药品按照注册批准的方法进行全项检验。
(二)符合下列情形之一的,应当对检验方法进行验证。
1.采用新的检验方法;
2.检验方法需变更的;
3.采用《中华人民共和国药典》及其他法定标准未收载的检验方法;
4.法规规定的其他需要验证的检验方法。
(三)对不需要进行验证的检验方法,企业应当对检验方法进行确认,以确保检验数据准确、可靠。
法规要求:中国药典(2010年版)范例
1.检验方法和限度。
2.应将该方法与规定的方法做比较试验,根据试验结果掌握使用,但在仲裁时仍以本版药典规定的方法为准。
法规要求:分析方法确认或验证相关指南

二.分析方法验证
分析方法验证的定义;
分析方法验证的目的;
分析方法验证范围;
分析方法验证的时机;
需验证的分析方法类型;
分析方法验证的具体内容;
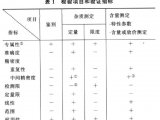
验证检测项目小结;
分析方法验证的方式和步骤;
分析方法验证常见问题;
1.分析方法验证的定义
是根据检测项目的要求,预先设置一定的验证内容,并通过设计合理的试验来验证所采用的分析方法能否符合检测项目的要求。
2.分析方法验证的目的
(1)证明采用的分析方法是科学、合理。
(2)证明分析方法能有效控制药品的内在质量。
♦ 验证过程和结果均应记载在标准起草或修订说明中。
3.分析方法验证范围
(1)适用范围:
化学药品的理化分析方法和仪器分析方法的验证与确认;清洁验证方法的验证。
(2)不适用:
化学药品的微生物方法;生物制品分析方法验证。
4.分析方法验证的时机
(1)建立新的药品质量标准;
(2)药品生产工艺变更;
(3)制剂的组分变更;
(4)对原分析方法进行修订时。
方法验证理由、过程和结果均应记载在药品标准起草说明或修订说明中。
5. 需验证的分析方法类型
(1)鉴别试验;
(2)杂质定量或限度检查(仪器或非仪器检测方法);
(3)原料药或制剂中活性成分以及制剂中选定组分(如,防腐剂等。。。)的定量测定含量测定;
(4)化学药品/中药制剂中其他需控制成分(如,残留物、添加剂等。。。)的测定;
(5)制剂溶出度、释放度等检查;
(6)原料药粒度检测;
6. 分析方法验证的具体内容
(1)专属性;
(2)线性;
(3)范围;
(4)准确性;
(5)精密度;
(6)检测限;
(7)定量限;
(8)耐用性;
(9)系统适用性;