手性γ-氨基丁酸类化合物是合成一些药物的关键结构单元。腈水解酶催化3-取代戊二腈去对称化水解,是合成这类化合物的有效方法。目前,已测试的腈水解酶对3-烷基或3-芳基戊二腈通常生成(S)-构型产物,而(R)-构型产物的对映体过量值较低。定向进化是实现酶立体偏好性翻转的有效手段,但在不损失酶活的基础上实现其立体选择性的翻转仍具挑战性。
中国科学院天津工业生物技术研究所研究员朱敦明、吴洽庆和兼职研究员林建平带领团队,通过对来自Synechocystis sp. PCC6803的腈水解酶(SsNIT)底物结合口袋的镜像分析,发现两个影响立体选择性的关键氨基酸残基W170与V198处于互为镜像位置,分别与底物潜手性碳原子的两个取代基团相互作用,而且它们的体积差别较大。通过置换这两个氨基酸残基的位置,实现了该酶对3-异丁基戊二腈水解反应立体偏好性的翻转。进一步采用定点突变及组合突变,重塑了其底物结合口袋,获得了高立体选择性(>99% ee)及活性的突变体E8。该突变体高效的催化400mM浓度的3-异丁基戊二腈选择性水解,生成(R)-3-异丙基-4-氰基丁酸,分离产率97%,产物ee值大于99%。研究人员探索突变体的底物特异性发现,其对3-烷基及3-芳基取代的戊二腈均实现了立体选择性的翻转,尤其对烷基取代的底物显示出较高的立体选择性。该研究为腈水解酶及其它酶催化对称性化合物去对称化反应的立体选择性改造,提供了新策略和新方法。
相关研究成果以Inverting the enantiopreference of nitrilase-catalyzed desymmetric hydrolysis of prochiral dinitriles by reshaping the binding pocket with a "mirror‐image" strategy为题,发表在Angewandte Chemie International Edition上。天津工生所助理研究员于珊珊、李金龙,副研究员姚培圆为论文的共同第一作者。研究工作得到国家自然科学基金、中科院相关项目、天津市合成生物技术创新能力提升行动项目及“合成生物学”国家重点研发计划专项的支持。
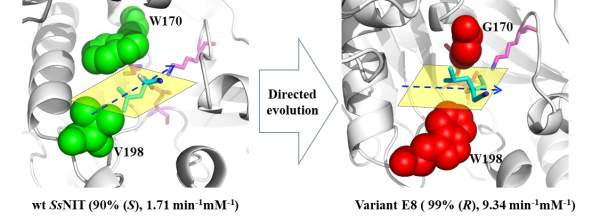
利用镜像策略改造腈水解酶立体偏好性