由于单个细胞几乎是半透明的,显微镜摄像机必须检测通过细胞各部分的光线中极其细微的差别。这些差异被称为光的相位。相机图像传感器受到它们能检测到的光相位差的限制,称为动态范围。
东京大学光子科学技术研究所的副教授Takuro Ideguchi说:“要用同一个图像传感器看到更多细节,我们必须扩大动态范围,这样才能探测到较小的光相位变化。”
研究小组开发了一种技术,通过两次曝光分别测量光相位的大小变化,然后将它们无缝地连接起来,形成一幅非常详细的最终图像。他们将他们的方法命名为自适应动态范围偏移定量相位成像(ADRIFT-QPI),2021年1月的《Light: Science & Applications》杂志发表了他们的研究成果。
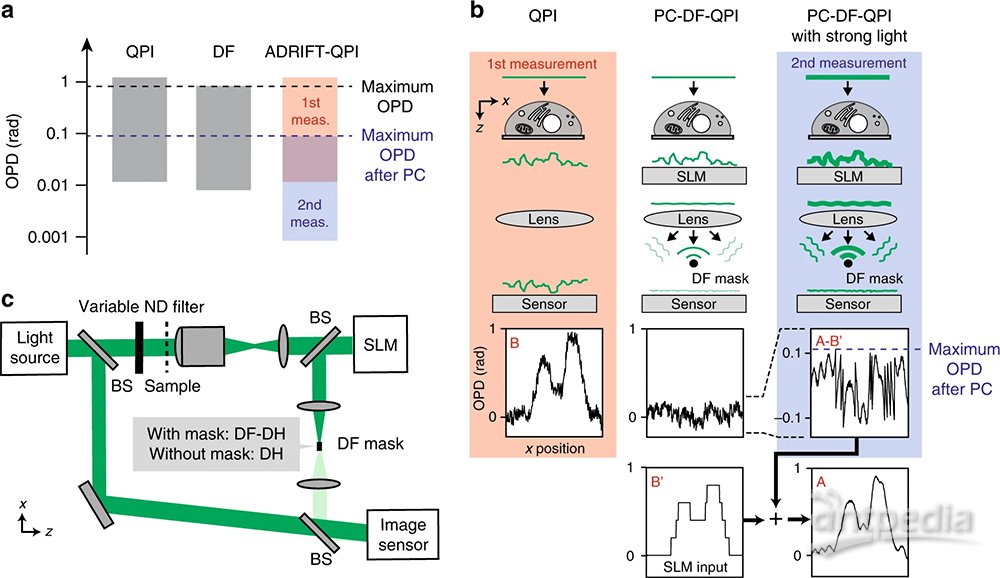
原理:ADRIFT-QPI Fig. 1: Principle of ADRIFT-QPI. 一个相位成像的动态范围:(左)常规QPI,(中心)暗场成像,(右)ADRIFT-QPI。
显着提高定量相位成像(QPI)灵敏度的方案可能有助于使光学成像和传感领域的一系列应用受益。日本东京大学的户田敬一郎及其同事将其方案称为自适应动态范围位移定量相位成像(ADRIFT-QPI)。它通过波前整形“消除”样本引起的大光学相位延迟(OPD),并通过暗场显微镜提高灵敏度来测量剩余的小OPD,从而发挥作用。该团队使用中红外光热QPI测量测试了该方法,并确认灵敏度提高了约6.6倍。
这是一个好消息。Ideguchi说:“我们的ADRIFT-QPI方法不需要特殊的激光、特殊的显微镜或图像传感器,我们的活细胞,不需要任何染色或荧光,光毒性的可能性非常小。”光毒性会杀死细胞,这也是荧光成像的一个诟病。
定量相位成像是将一个平面的光脉冲发送至细胞,然后统一测量光波通过细胞后的相移,计算机分析然后重建细胞内主要结构的图像。Ideguchi和他的合作者之前已经开创了其他方法来增强定量相位显微镜。
定量相位成像是检查单个细胞的有力工具,它能根据光波的变化跟踪细胞的生长速度。然而,由于图像传感器的饱和能力较低,该技术的定量方面具有较低的灵敏度,因此用常规方法不可能跟踪细胞内和周围的纳米颗粒。
而新的ADRIFT-QPI方法克服了定量相位成像的动态范围限制。在ADRIFT-QPI过程中,相机进行两次曝光,生成的最终图像的灵敏度是传统定量相位显微镜图像的七倍。
第一次曝光是通过传统的定量相位成像产生的——一片平的光被脉冲射向样品,并且在光通过样品后测量其相移。计算机图像分析程序在第一次曝光的基础上生成样品的图像,然后快速设计一个能反映样品图像的光波阵面。一个单独的组件称为波前整形设备,然后产生这种“光雕塑”与更高强度的光更强的照明和脉冲它对样品进行第二次曝光。
如果第一次曝光产生的图像是样品的完美表现,那么第二次曝光的定制雕刻光波将在不同的阶段进入样品,穿过样品,然后以平板光的形式出现,使相机只能看到一个黑暗的图像。
“有趣的是:我们抹掉了样本的图像。我们取消了大的结构,这样我们就可以看到小的非常详细,”Ideguchi解释说。
在现实中,第一次曝光是不完美的,所以雕塑光波出现微妙的相位偏差。
第二次曝光揭示了微小的光相位差,这些光相位差在第一次曝光中被较大的差异“冲掉”。由于在第二次曝光中使用了更强的照明,这些剩余的微小光相位差就拥有了更高的灵敏度。
附加的计算机分析重建了样品的最终图像,并根据两个测量结果扩展了动态范围。在概念验证演示中,研究人员估计ADRIFT-QPI产生的图像的灵敏度是传统定量相位成像的7倍。
Ideguchi说,ADRIFT-QPI的真正好处是它能够在整个活细胞中看到微小颗粒,而不需要任何标签或污染。
Ideguchi说:“例如,可以检测到病毒等纳米级粒子或细胞内外移动的粒子发出的小信号,从而可以同时观察它们的行为和细胞状态。”
原文检索:Adaptive dynamic range shift (ADRIFT) quantitative phase imaging







