今年3月,美国临床化学杂志上又出现了Dr
Miller的署名文章“24个血清白蛋白检测程序一致性状态和对医学决定的影响”。这是一篇专门研究常规检测白蛋白未来方向的好文章。一个实验室每天进行的白蛋白检测项次在临床化学中非常大,很少有人去思考这些检测结果的可靠性。以往也曾经报告了染料结合方法BCG与BCP究竟哪一个更好的报告,但都没有向这次的详细深入研究,最后还做出了结论。文章总结认为,临床实验室的常规白蛋白检测,如果依然是染料结合方法原理的,应使用BCP方法;BCG方法应该停用了。
该研究是在Dr Miller的弗吉尼亚州Commonwealth联邦大学病理部、和弗吉尼亚大学病理部进行的。他们收集了无肾衰疾病患者的剩余患者血清(n=50)和肝素血浆(n=48)、和具有肾衰患者的血液透析前的血清(n=53),形成各个混合血清(血浆)。以国际公认的ERM-DA470k/IFCC参考物质,作为白蛋白检测的参考检测标准。对3个免疫化学的、9个BCG的、和12个BCP的方法,检查了这24个市售可用的白蛋白检测程序的一致性和分析性能近期状态。
1、实验结果
1、对ERM-DA470k/IFCC RM白蛋白的回收率。可参见图1。图中每个方法的均值是3个RM在3周内检测综合均值。每个方法均值的扩展的不确定度(k =2)估计为计算SE的2倍。Tina-quate和Immage的免疫化学方法具有的值,在RM靶值不确定度之内(图中的两条横的虚线)。BNⅡ的免疫化学方法具有明显高的偏移。9个BCG方法中的5个回收的RM靶值在它的不确定度之内。有1个BCG方法具有的均值在RM靶值的不确定度之内,但它的不确定度超出了RM的限值。3个BCG方法没有回收到RM的靶值,具有偏低的偏移,从-4.9%~-9.3%。12个BCP中的10个回收RM靶值在它的不确定度之内。2个BCP方法具有的均值在RM的不确定度之内,但它们的不确定度超出了RM的限值。
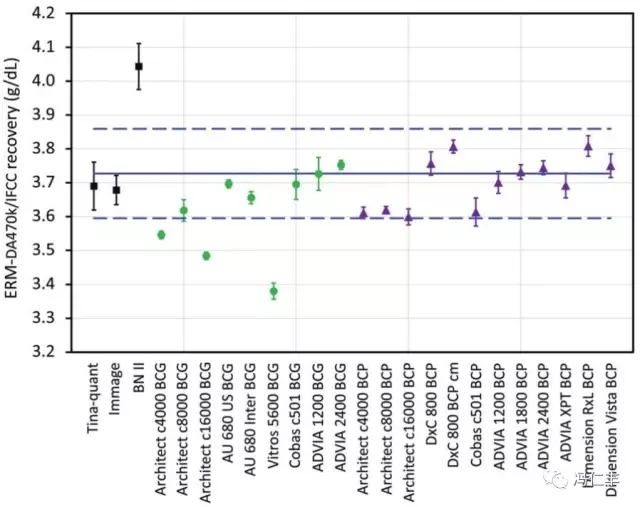
图1、白蛋白的回收率,这是相对于混合的ERM-DA470k/IFCC RM靶值。
图中的实线为混合RM的靶值,虚线为它的不确定度(k =2)。名义化学方法的均值为黑方块;BCG方法为绿圆点;BCP方法为紫三角点。每点的条线表示该方法均值的不确定度(k=2)。
结果
JCTLM列出了血清白蛋白的免疫化学检测,无论是透射比浊或散射比浊的均为参考检测程序(RMP)。在3个免疫化学方法中,Tina-quant被选定为RMP,因为它具有ERM-DA470k/IFCC最佳回收[-0.04g/dl;-1.0%],支持了正确校准的溯源性,它也具有最低的综合随机误差成分。
图2显示了每个检测程序相对于RMP,在非肾病血浆和血清样品中结果差异的图示。所有BCG方法相对于RMP均有高偏移,和具有较BCP方法较高的值。BCP方法的偏移小于BCG方法,并较紧密地聚集环绕在差异为0的周围。在统计上所有检测方法的血浆均值结果偏移显著地较血清高,但BNⅡ和DimensionRxL BCP不是。免疫化学方法的Immage结果相似与Tina-quant,血清样品的平均偏移为0.01g/dl;而BNⅡ的结果偏移为0.26 g/dl,高于其他2个免疫化学方法。
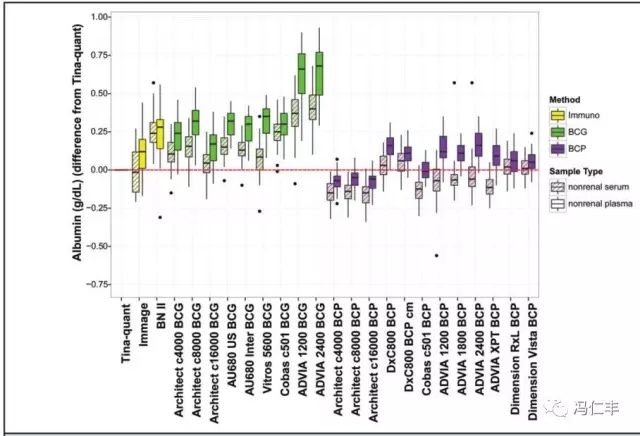
图2、对非肾病血浆和非肾病血清的每个方法相对于Tina-quantRMP的白蛋白结果差异。
每个方块显示了中位数、第25和第75百分位数的值,whisker方块两端的线端代表了第10和第90百分位数值。黑色圆点为超过第10和第90百分位数的值。Tina-Quant的中位数血清为32.8 g/L、血浆为29.5 g/L。
图3显示了非肾病患者和肾透析患者得到的血清样品的白蛋白结果图示。除了Immage、BNⅡ、Vitros 5600 BCG、Dimension RxL BCP、和Dimension Vista BCP,所有检测程序具有的检测结果,肾病透析患者血清较无肾病血清的,在统计上有显著较低的偏移。以往观察中,BCP方法较BCG方法对非肾病患者的血清和血浆具有较低的值(图2),这次也在肾透析患者的血清中观察到(图3)。
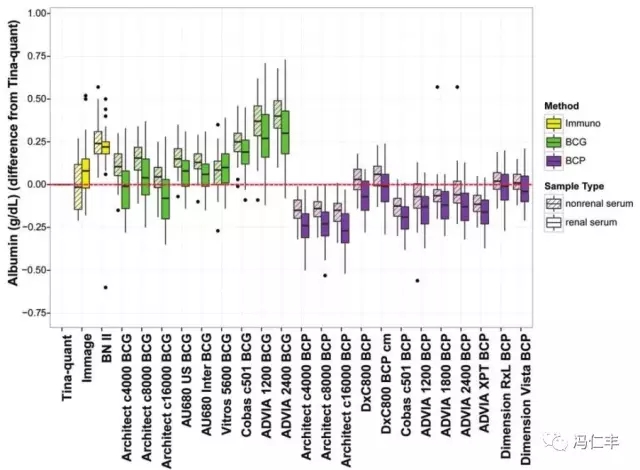
图3、每个方法相对于Tina-quant RMP,对透析患者的血清样品和非肾病血清样品检测的白蛋白结果的差异。Tina-quant的中位数值:肾病样品为34.1g/L,非肾病样品为32.8g/L。
在分析每个检测方法具有的误差因素中,研究采用了生物变异估计。白蛋白的生物变异,个体内CV为3.2%,个体间CV为4.75%,计算为合适的分析性能CV为1.6%、偏移为1.4%;最低的分析性能CV为2.4%;偏移和2.1%。所有检测程序的精密度的检测内和检测间估计分别为2.0%和2.8%或小一些。仅AdviaXPT具有的检测间CV超过了最低的性能要求,22 个方法的16个具有的CV在合适的指标内。位置的影响对所有BCG和BCP方法<2%。Immage和BNⅡ具有位置的影响足够大,因此无法去估计样品特定的影响。对所有其他检测程序的样品位置影响<5%。除了一些例外,随机误差成分很小,所有检测程序均在最低的性能指标内。
主要的误差成分是大多检测程序的偏移。BCG方法的平均偏移范围从1.5%~13.9%,所有BCG方法的偏移在1个或多个浓度均超出了最低性能指标。BCG方法一般均展现了较BCP方法较大的偏移;BCP方法的平均偏移范围为-5.4%~1.2%。12个BCP方法的7个符合偏移在所有浓度下的最低性能指标。对肾病患者的样品,BCP方法一般具有较BCG方法较低的偏移(图3)。肾透析患者样品的偏移,BCG为-2.2%~9.1%;BCP为-7.9%~-0.7%。分析误差成分观察到,如果对3个类型样品分别检查。BNⅡ的免疫化学检测程序与其他2个免疫化学程序无论哪一个相比,在所有样品类型中具有约7%的偏移。
图4显示了BCG和BCP方法相对于RMP的最小和大多偏移的差异点。也展现了未稀释的和稀释的ERM-DA470k/IFCC RM的BCG和BCP结果与RMP结果比较的差异。一般,稀释的参考物质展现了与患者样品BCG结果有不同的关系,但是与BCP和免疫化学方法类似的关系。
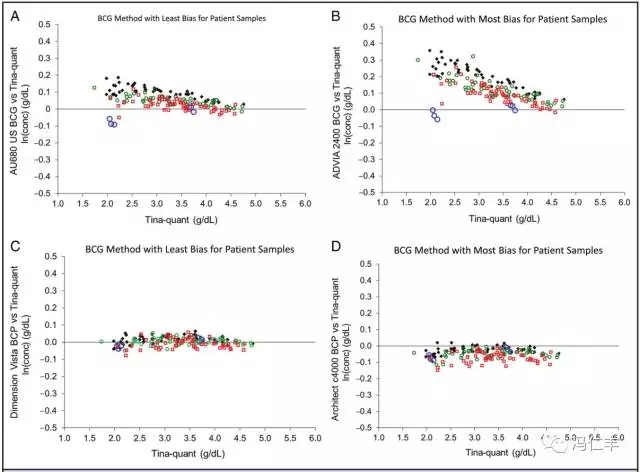
图4、BCG和BCP方法相对于Tina-quant RM的差异点
差异为y轴,以ln浓度表示。ln浓度乘以100%表示了大致上的%CV。(A)为BCG方法具有患者样品最小的整个偏移;(B)为BCG方法具有最大的整个偏移;(C)BCP方法具有患者样品最小的整个偏移;(D)为BCP方法具有最大的整个偏移。菱形(黑色)为非肾病血浆的样品;小圆点(绿色)为非肾病血清样品,方形(红色)为肾病血清样品,大圆点(蓝色)为未稀释和稀释的ERM-DA470k/IFCC。
2、讨论
检验医学溯源性联合委员会(JCTLM)列出了依据免疫检测无论是透射比浊或散射比浊检测免疫复合物的检测原理,均作为血清免疫化学的RMP。ERM-DA470k/IFCC是被列出作为免疫检测校准的批准的RM。我们设定Tina-quant透射免疫化学检测程序作为RMP,去确定检测程序检测和样品类型的相对偏移,因为它对RM具有白蛋白出色的回收率,支持了正确校准溯源性至RM和很小的随机误差成分。在其他2个免疫化学方法间,Immage的散射程序具有类似与Tina-quant的性能特性,而BNⅡ相对于RM值和Tina-quant程序,在所有样品类型中的检测具有显著阳性偏移。这些观察隐含了BNⅡ的校准是不正确的,使用免疫化学检测原理没有确保白蛋白准确的结果,除非验证了校准溯源性。
一般,BCG方法较BCP方法具有较大的偏移。BCP方法相对于RMP的平均偏移较小,比例误差的大小不随浓度而变化。相反,BCG方法相对于RMP的平均偏移较大,并比例误差随白蛋白浓度而异,在较低浓度处有较大的阳性偏移。另外,与BCP方法比较,BCG方法间的差异范围很大,建议BCG方法受样品中其他蛋白或物质较BCP方法,在很大程度上有影响。
依据生物变异的指标在生理上合适的浓度范围内,没有一个BCG方法符合偏移的最低性能指标。12个BCP方法的8个符合了偏移的最低性能指标,那些没有符合的方法也较BCG方法观察到的,一般均有较小的偏移。我们的数据显示了BCP方法对白蛋白有较好的选择性,具有比例偏移;因此,看来可以达到结果的一致性。BCG方法的随浓度变异的偏移和非选择性,隐含了使用BCG技术不能达到一致,所以应在临床实验室中予以淘汰。
使用肝素样品检测,引起了BCG方法错误的结果的观察,以往也已经报告过。本次研究中的所有检测程序,除了Immage散射程序,被美国FDA批准可以使用血清和肝素血浆样品。我们的观察建议,与肝素化样品有关的特异性问题,在近期BCG方法中继续是问题。
24个检测程序中的19个,声明具有校准溯源至ERM-DA470k/IFCC或其前者ERM-DA470血清的RM。看来在实施校准溯源性做法上的差异产生了偏移。但是,从血清与血浆的结果差异、具肾病与非肾病患者的样品结果的差异,也支持了白蛋白方法作为受选择性局限的影响,在样品类型中有差异。
达到血清和血浆白蛋白一致性的结果,使用染料结合技术的将要求指定某个单一试剂类型。我们的数据支持了BCP作为优选的方法,因为它较BCG方法有相对较小的偏移,并在检测的浓度区间内是恒定的,而BCG方法在整个浓度区间内具有非比例的偏移,使得标准化不可能。
所有BCP和9个BCG方法中的6个,在回收ERM-DA470k/IFCC RM的靶值很相似。患者样品和未稀释的和稀释的RM,以免疫化学和BCP方法相对于RMP的结果,具有类似的关系,RM看来适合用于这些方法。但是,稀释的RM的BCG方法的结果,具有值得注意的不同关系。我们不知道厂商在校准溯源性方式上是否使用了稀释的RM,对于BCG方法如果使用稀释的物质是否有互换性的问题。分析证书规定了RM主要用于校准免疫检测的程序,很少包括关于染料结合方法适用性的信息,以及推荐在特定检测程序使用时应确认互换性。因此需要进一步研究确定,RM为染料结合白蛋白检测程序的互换性特性。
白蛋白检测程序偏移的差异,牵连着患者的护理。美国肾病基金会对慢性肾衰的营养指导,推荐对维持肾透析患者常规检测白蛋白。在美国,医疗保险和医疗补助服务中心(CMS),设定了透析患者护理的标准。与美国肾病基金会的导则一致,目标是BCG方法检测的白蛋白浓度须≥ 40 g/L。
2016年,透析中心被预期可对38%治疗的患者,达到白蛋白高于40 g/L。对血清白蛋白<35 g/L的患者,中心必须显示计划改善营养的证据。对于白蛋白低于指导指定值的患者,强化蛋白补充。但补充剂会不利地影响磷、钾、和其他电解质浓度;补充剂的费用和个人时间通常是无偿的,但还没有显示明确改善死亡率的好处还没有显示。在白蛋白检测上缺乏标准化,这样的风险使大量透析患者遭受了未经证实的和昂贵的治疗。
白蛋白检测程序的选择在肾病样品中产生了很大的差异,与本研究的目标相同。要求BCG方法白蛋白≥40 g/L的,使用Advia2400检测中有32%样品达标,但仅13%的样品在使用Architect c16000达标。同样,这些检测程序结果各自的70%和36%,达到或高于35 g/L的目标。很明显,使用固定浓度处的质量目标,对近期白蛋白方法一致性状态是不可行的。
检测程序结果间差异影响的另一个示例是,当使用血清白蛋白计算“纠正的”血清钙浓度时很明显。计算试图考虑钙量差异,因钙与白蛋白结合,由此降低了生物上活跃的未结合钙。这样的计算经常被用于具有低白蛋白的患者,包括具有肝病和肾病及癌症患者。正如Labriola等展现的,若将一个Roche Modular P 的BCG检测程序与Beckman Unicel DxV 800的BCP检测程序比较时,纠正的钙结果产生了钙状态不一致的分类。我们的结果与这些发现是一致的,建议“纠正的”钙将实质上受到方法的影响,不仅是BCG或BCP方法的性质,而且也被某给定的检测程序特定的实施所影响。样品类型也将影响“纠正的”钙。只有实现白蛋白检测一致性,否则白蛋白检测的分析变异还要更多地影响使用“纠正的”钙。与这个评审一致的,美国医疗保险和医疗补助服务中心(CMS)的2016更新版对透析中心的指导,已经以“不可纠正的钙”易于替换了“纠正的钙”词语。
血清白蛋白也用于对终末期的肾病患者的临床决定,患者必须在肾移植和透析间做出选择。该决定有助于使用单一的白蛋白判断限35 g/L。对于患者白蛋白低于该判断限的,肾透析预期1-年存活期将被减少到10%,但在肾移植后的预期存活则影响很小。Emory大学的外科部的网站,提供了该议题的更多信息。白蛋白检测程序的性质会影响许多肾透析的患者,例如,在现有研究中,肾病样品结果以Advia 2400 的BCG检测程序得到≥35 g/L的结果为70%,但以Architect c6000的BCG检测程序,得到≥35 g/L的结果仅36%。
本研究的局限性包括,使用了混合样品,而不是各个患者的样品,因为样品量的限制。混合样品不是各个样品的理想代表。将含有高浓度的白蛋白样品与低浓度白蛋白样品混合时,在高样品存在的白蛋白分子形式为主,存在于任一样品内的干扰物质被稀释了。另一个局限性是,仅将一个检测程序(Tina-quant)列为RMP。有可能,Tina-quant检测程序的样品特定的影响,会混淆我们的观察。另外,检测间的精密度估计来自有限批数的结果。
总之,BCG方法较BCP方法有较大的偏移。另外,BCG方法的偏移随白蛋白浓度而变异;但BCP方法没有。因使用BCG和BCP方法得到的检测间通常差异,以及每个方法的特定厂商实施检测不同,白蛋白浓度的单一决定判断限,看来在患者-护理决定中不合适。使用染料结合方法的白蛋白结果的标准化,将要求接受BCP为优选试剂。
3、结论
在免疫化学、BCG、和BCP方法间的显著差异,影响了血清白蛋白结果的解释。临床对肾病和其他疾病的管理的指导和计算,必须考虑白蛋白检测方法,直至实现一致性。