首先先了解几个术语和定义:
表面等离子共振(Surface Plasmon Resonance,SPR)
一、消逝波
当光从光密介质入射到光疏介质,入射角增加到某一角度,使折射角达到90°时,折射光将完全消失,而只剩下反射光,这种现象叫做全反射。
当以波动光学的角度来研究全反射时,人们发现当入射光到达界面时并不是直接产生反射光,而是先透过光疏介质约一个波长的深度,再沿界面流动约半个波长再返回光密介质。则透过光疏介质的波被称为消逝波。
如下图所示。
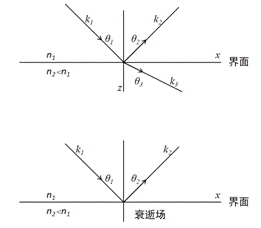
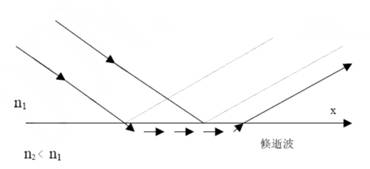
全反射时如图中所示沿X轴方向振幅衰减的一个波,即入射光波在反射面不立即消失,而是投射进入光疏介质一定深度,且振幅在垂直方向呈指数衰减,这种电磁波叫消逝波。
二、等离子波
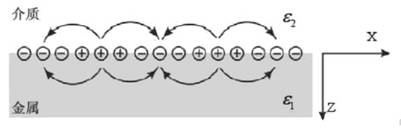
把金属表面的价电子看成是均匀正电荷背景下运动的电子气体,其中正、负带电粒子数目几乎相等,这实际上也是一种等离子体。当金属受电磁干扰时,金属内部的电子密度分布会变得不均匀。因为库仑力的存在,会将部分电子吸引到正电荷过剩的区域,被吸引的电子由于获得动量,故不会在引力与斥力的平衡位置停下而向前运动一段距离,之后电子间存在的斥力会迫使已经聚集起来的电子再次离开该区域。由此会形成一种整个电子系统的集体震荡,而库仑力的存在使得这种集体震荡反复进行,进而形成的震荡称等离子震荡,并以波的形式表现,称为等离子波。
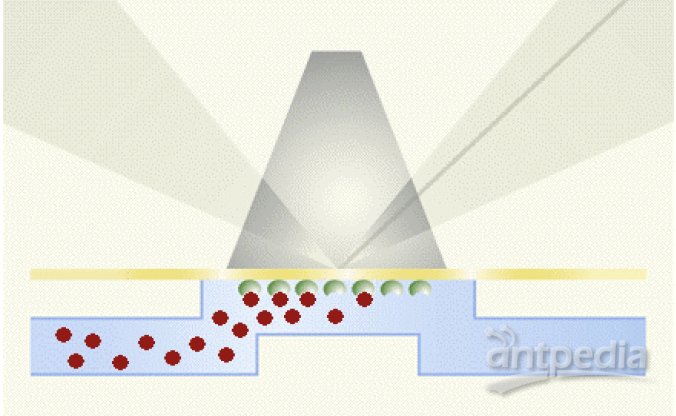
三、SPR光学原理
光在棱镜与金属膜表面上发生全反射现象时,会形成消逝波进入到光疏介质中,而在介质中又存在一定的等离子波。当两波相遇时可能会发生共振。当消逝波与表面等离子波发生共振时,检测到的反射光强会大幅度地减弱。能量从光子转移到表面等离子,入射光的大部分能量被表面等离子波吸收,使反射光的能量急剧减少。
可以从反射光强响应曲线看到一个最小的尖峰,此时对应的入射光波长为共振波长,使反射光完全消失的入射角就是SPR角。SPR角随金膜表面折射率变化而变化,而折射率的变化又与金膜表面结合的分子质量成正比。因此可以通过对生物反应过程中SPR角的动态变化获取分子之间相互作用的特异信号。
SPR生物传感器的光源为偏振光(polarized light),传感芯片(sensor chip)表面镀有一层金膜,实验时,先将一种生物分子(ligand)固定在金膜表面,然后将与之相互作用的分子(analyte)溶于溶液(或混合液)流过芯片表面。SPR检测器能跟踪溶液中的分子与芯片表面的分子结合、解离整个过程的变化,不同角度的反射光的光强被记录后得到角度-光强曲线图,每条曲线的波谷即为该曲线的共振角,共振角对应的角度为共振信号(resonance signal),时间与对应共振信号的曲线即为SPR传感图(sensorgram)。
表面等离子共振生物分子相互作用分析仪(BIACORE)的原理
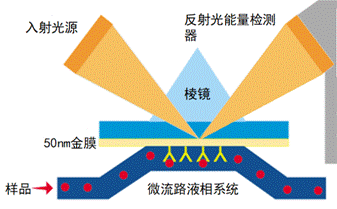
当一束光线通过棱镜射向金属表面,在金属发生全反射现象时,会在金属膜中产生消逝波,消逝波与表面等离子波发生共振时,检测到的反射光强会大幅度地减弱。此时对应的入射光波长为共振波长,对应的入射角为共振角,即SPR角。SPR角随着金属表面折射率的变化而变化,而折射率的变化又与金属表面结合的分子质量成正比。
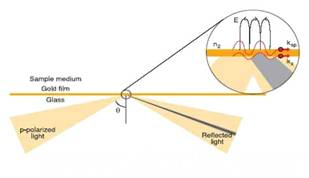
Biacore的核心组件就是由微流路系统,光学组件及金膜芯片组成。金膜芯片上的蛋白和流路中的分子结合有解离的过程中,SPR角就会随之发生变化,检测器检测到这种变化,根据此变化曲线作图分析,可得出分子间的结合常数Ka、解离常数Kd或亲和力常数KD。
以免疫学分析为例,在金膜表面固定某种受体(如抗体)然后流过含相应配体(如抗原)的样品,配体与受体的结合将使金膜与溶液界面的折射率上升,从而导致共振角发生变化。为了表述的方便,共振角(或共振信号)可以用共振单位(resonance units,RU)来表示。对大多数生物分子而言,1000RU大约等于1mm2的面积上有1ng的质量变化,相当于溶液中蛋白浓度为6mg/mL。SPR生物传感器通过检测获得共振角的改变程度,便可以对配体浓度进行定量。
• SPR 是一种折光率传感器,其响应值反映了SPR角度的改变
• 响应信号依赖于芯片表面分子的浓度和温度
• 1 RU 的响应值大致上相当于芯片表面结合物质的浓度改变了1 pg/mm2 (蛋白结合与CM5芯片)
如下图所示。
Biacore的核心组件包括:

SPR生物传感技术的应用领域包括:生物大分子的相互作用;肿瘤研究;免疫学和传染病;神经科学;生物制药;蛋白质组学。
Biacore可研究的生物分子范围包括:蛋白质;DNA/RNA;脂类/脂质体/生物膜;多糖;多肽;小分子;全细胞病毒/微生物。
可分析的对象:
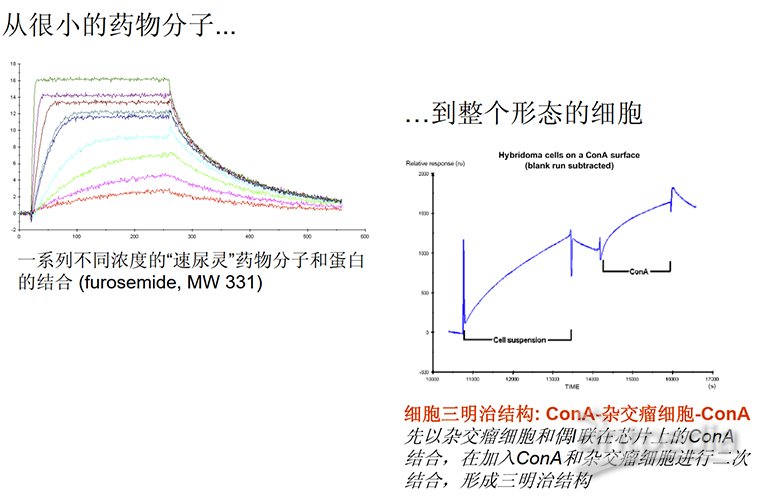
Biacore核心组件

Biacore提供的生物分子相互作用信息包括:
有无结合(Yes or no)
结合的特异性和选择性(Specificity)
两种分子的结合强度-亲和力(Affinity)
结合和解离的快慢和复合体的稳定性-动力学(Kinetics)
功能复合体形成的参与者、协同者和组装顺序(Mechanism)
分子结合的温度与热力学特征(Thermodynamics)
目标分子活性含量的检测(Concentration)
SPR光学组件
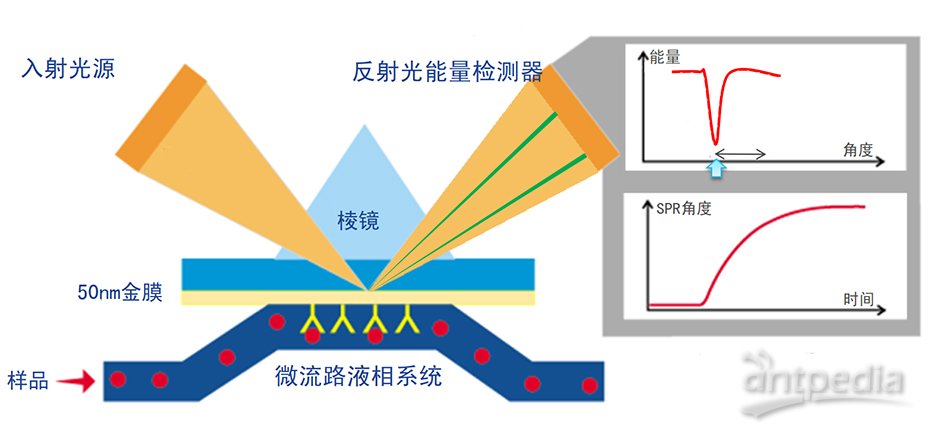
微流控系统(IFC)具有的特性包括:集成化、自动化的微流路控制系统;样品消耗量低;为互相作用分析而设计优化
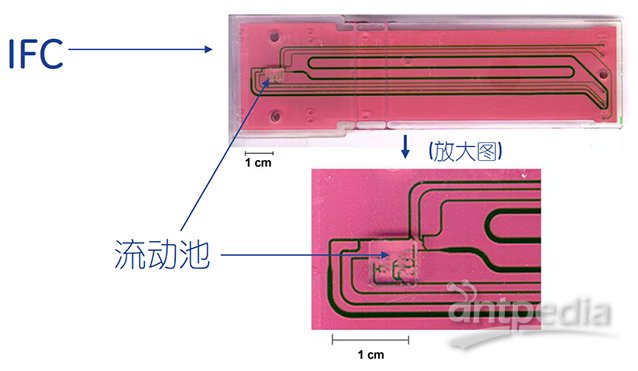
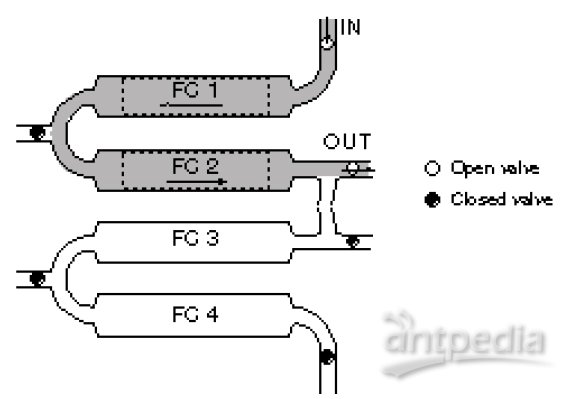
微流控系统(IFC)-流动池的特点为:
IFC上有4个流动池;可选择单独、配对、串联使用。流动池为配对使用进行了优化(Fc1-Fc2,Fc3-Fc4)
传感芯片:
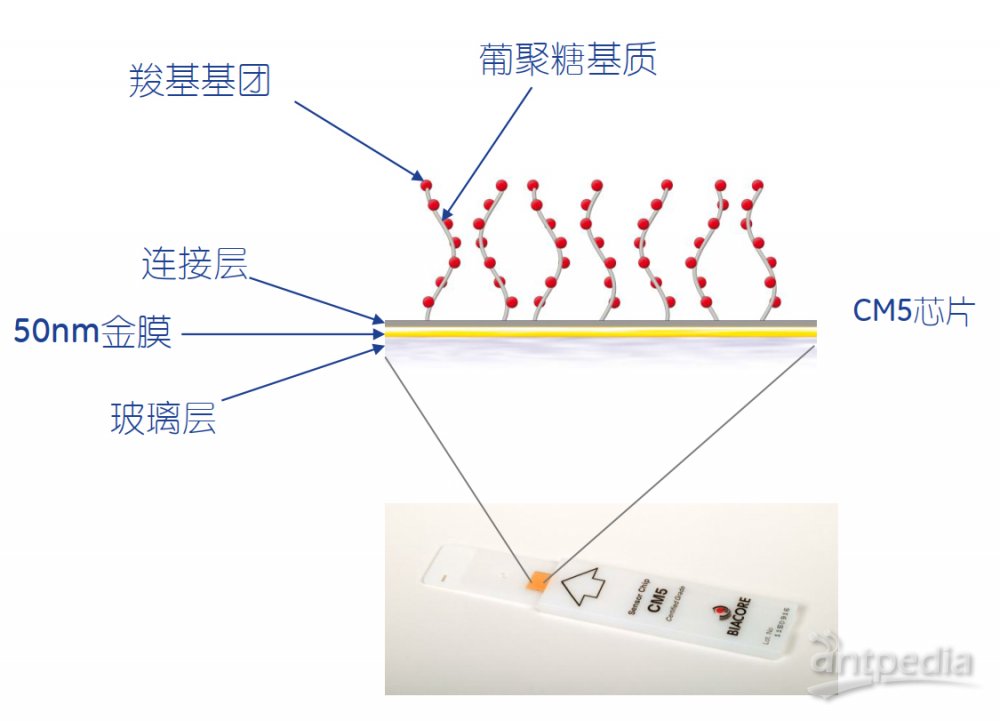
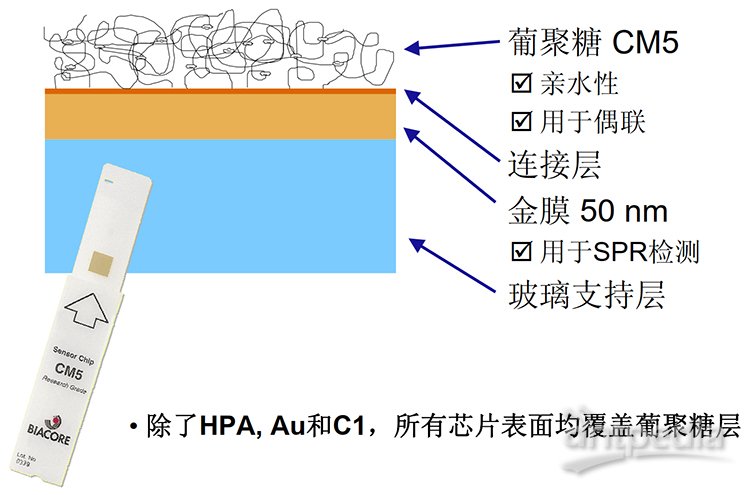
葡聚糖表面的特点:亲水性;温和型:和2%浓度的葡聚糖水溶液环境相似;非特异性结合量低;高结合容量;易于进行共价结合;出色的化学稳定性。
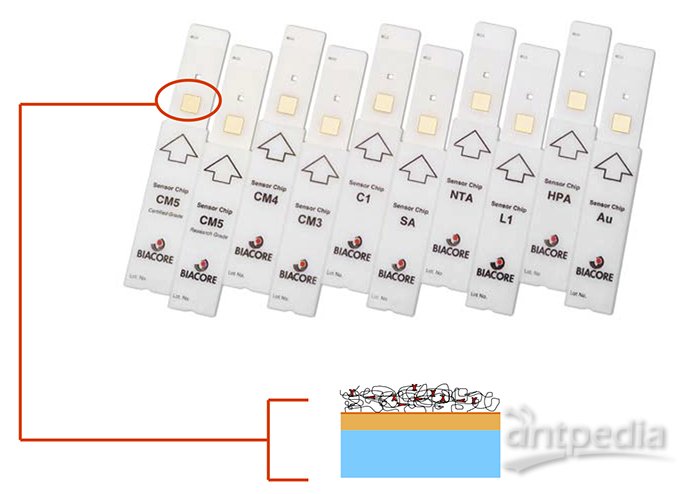
传感芯片的选择:
11种不同的芯片种类
CM5,CM4,CM3:芯片、蛋白、肽段、小分子等
CM7:小分子化合物研究
SA芯片:生物素标记的分子,如核酸、糖类等
Biotin CAP芯片:可逆性生物素捕获芯片心
NTA芯片:His重组蛋白
L1芯片:模拟脂质双分子层环境
HPA芯片:实现膜系统相关的互作分析
C1芯片:研究细胞、病毒等大颗粒分子
Au裸金芯片:客户定制表面(材料、高分子等)
30余种不同的试剂盒及缓冲液产品:
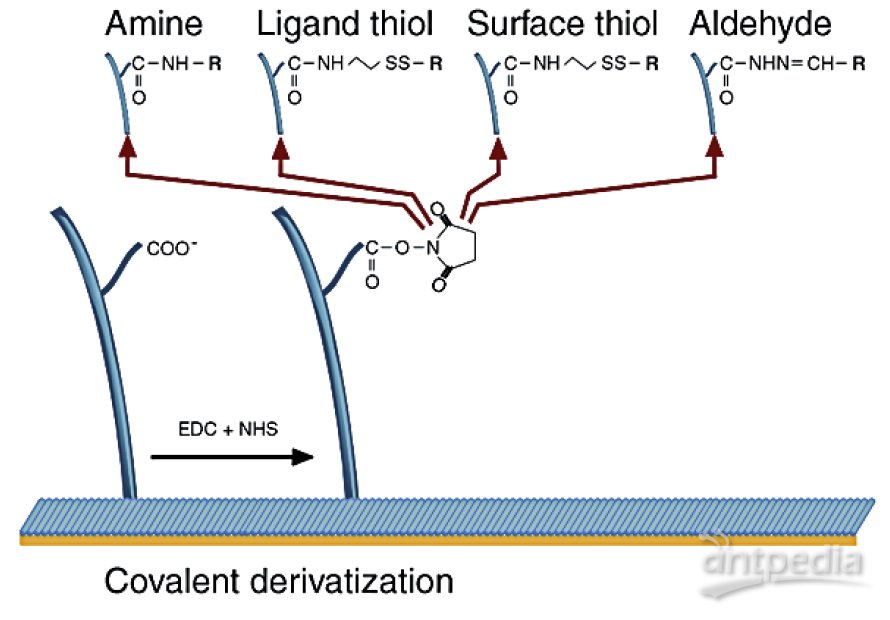
氨基偶联试剂盒、巯基偶联试剂盒;
GST捕获试剂盒 GST重组蛋白分析
NTA捕获试剂盒 His重组蛋白分析
最常用的传感器芯片:
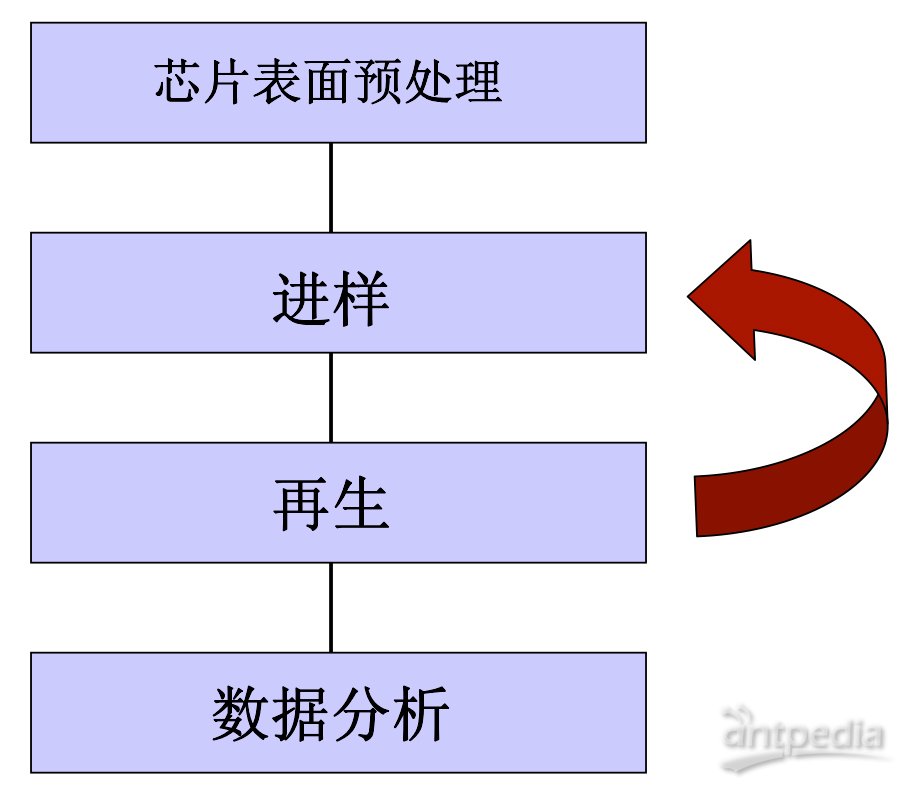
Biacore实验的基本流程
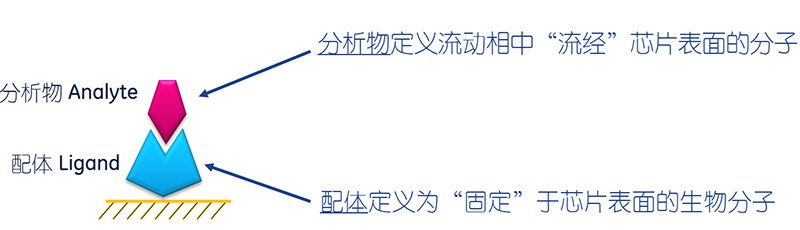
分析物和配体的定义
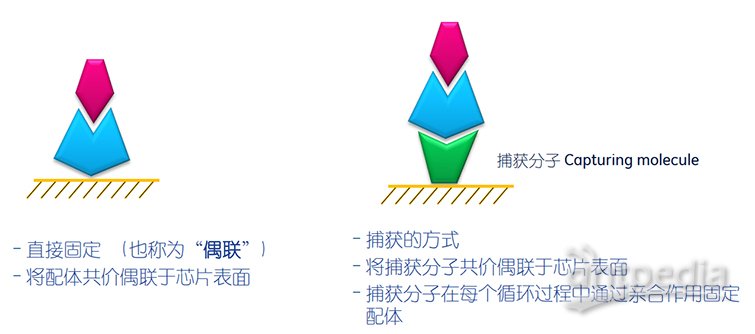
芯片表面预处理 – 偶联/固定配体 (Immobilization)
–什么是固定配体?
–将配体直接(共价)或者间接地 (通过捕获分子) 固定于芯片表面;或称为偶联蛋白:在芯片表面偶联分子Ligand或捕获分子
样品进样(Injection)的过程为:
分析物(Analyte)进样后,以恒定的流速和浓度流过芯片表面
样品中的待分析物与固定在芯片表面上的配体发生结合,芯片表面物质的质量发生改变,仪器记录下对应的响应值(response)的改变
进样结束后,切换缓冲液流过芯片表面,分析物由配体上自发解离,解离的进程由响应值实时监控
芯片再生(Regeneration)的过程为:
将自发解离后仍然结合于配体的分析物彻底洗掉
配体的结合活性必须保留。
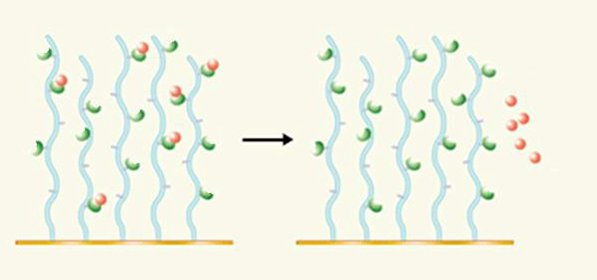
传感图(The sensorgram)
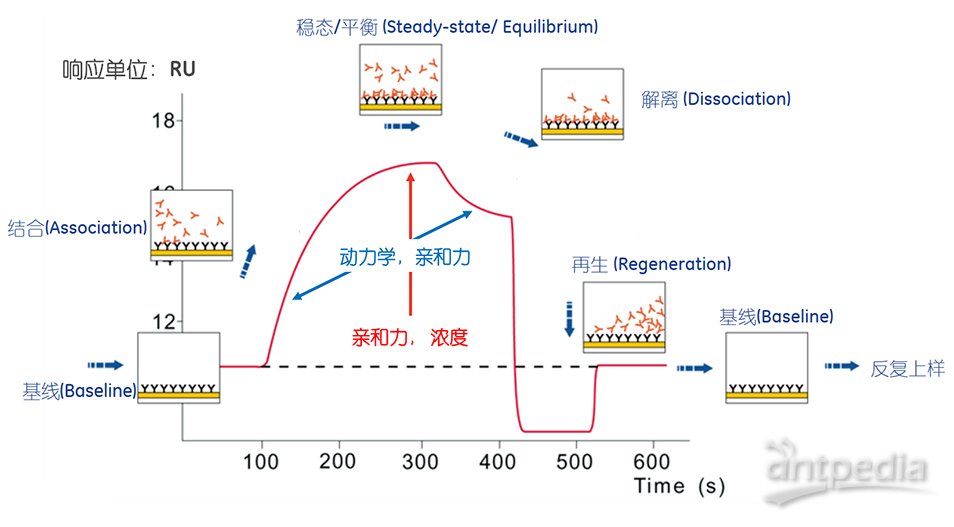
实验设计
选用CM5传感芯片→在金膜表面固定表达纯化后的D结构域蛋白→流过含抗体的样品→抗体与D结构域蛋白的结合将使金膜与溶液界面的折射率上升,从而导致共振角发生变化→检测蛋白与抗体的结合情况。