| 实验方法原理 |
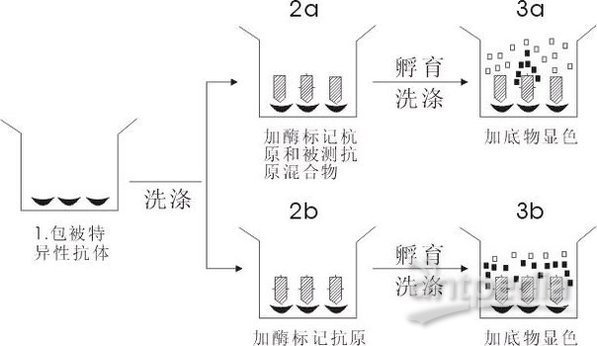
图1:竞争法测抗原示意图
这种方法所测定的抗原只要有一个结合部位即可,因此,对小分子抗原如激素和药物之类的测定常用此法。该法的优点是快,因为只有一个保温洗涤过程。但需用较多量的酶标记抗原为其缺点。 |
|---|---|
| 实验材料 | |
| 试剂、试剂盒 | |
| 仪器、耗材 | |
| 实验步骤 | 一、包被抗体:用包被缓冲液稀释特异性抗体球蛋白至最适浓度(1~10 ug /ml),每凹孔加0.3 ml,4℃过夜,或37℃水浴3小时,贮存冰箱。
二、洗涤:移去包被液,凹孔用洗涤缓冲液(含0.05%吐温-20)洗3次,每次5分钟。 三、分2组,a组加酶标记抗原和被检抗原混合液0.2 ml,b组只加酶标记抗原液0.2 ml,37℃作用1~2小时。(混合液可作成不同稀释度) 四、洗涤:移去包被液,凹孔用洗涤缓冲液(含0.05%吐温-20)洗3次,每次5分钟。 五、加入0.2 ml底物溶液于每个凹孔(OPD或OT),室温作用30分钟(另作一空白对照,0.4 ml底物加0.1 ml终止剂)。 六、加终止剂:每凹孔加2 M H2SO4或2 M柠檬酸0.05 ml。 七、用酶标比色计测定a、b两组OD值,并求出a、b、OD值的差数。 展开 |
| 其他 | 一、影响ELISA的因素
S / X = CV ,CV应低10%,不应大于10~15%。
不论目测或分光光度计测定,均可作一个稀释度或一系列稀释度测定,一般常规诊断只用一个稀释度判断阳性或阴性就可以了,这样比较方便,现在推荐传染病的血清诊断用1:200一个稀释度。有些需要精确定量的,可作一系列稀释度测定。
记录结果有下列几种方法:
1、“+”或“-”:所有超过规定的OD值(如OD,0.4)的标本均属阳性,此规定OD值是根据事先测定大量阴性标本所取得的,此规定值是阴性标本的上限。或者以一组阴性标本OD平均值加2~3个标准差作为阳性阈值。
2、直接以OD值来表示,如0.4、0.7、1.2,OD值越大,阳性反应越强,但此数值是在固定实验条件下得到的结果,而且每次实验都要有参考标本作对照。
3、以终点滴度表示:将标本作连续稀释,最高稀释度能出现阳性反应者(即OD值仍大于阳性阈值,即为该标本的滴度。
4、以“比值表示:求出被检标本的OD值与一组阴性标本OD值的比值,例如为阴性标本的2倍或3倍,即为阳性,比值小于2.1而大于1.5为可疑,<1.5为阴性。
测定标本OD值-空白OD值
阴性对照OD值-空白OD值
如在此测定时以空白校正“O”点。
5、以“单位”来表示:在测定被检标本的同时,再测定一个含已知单位数的阳性参考血清,用不同稀释度作ELISA检测后,以OD值为纵坐标,单位数为横坐标,画出标准曲线。以后可根据被检标本的OD值,从曲线上找出相应的单位数,再乘于血清的稀释倍数,即可得出被检标本的单位数。
作试验时的阴性参考血清最好不要显色,否则会对结果判断带来困难,特别在目测时,当阳性标本OD值>2.0时,应作适当稀释后再作测定。
2. 对使用仪器要求 展开 |