
强生(JNJ)旗下杨森制药近日宣布,已向美国食品和药物管理局(FDA)提交了一份补充生物制品许可申请(BLA),寻求批准Tremfya(guselkumab),用于活动性银屑病关节炎(PsA)成人患者的治疗。在美国,Tremfya已于2017年7月获批,治疗中度至重度斑块型银屑病成人患者。该公司计划在年底向欧洲药品管理局(EMA)提交Tremfya治疗活动性PsA的一份新适应症申请。
此次sBLA,基于2项III期临床研究(DISCOVER-1和DISCOVER-2)的数据。这些研究均显示治疗24周后达到了ACR20缓解的主要终点,研究中观察到的Tremfya的安全性与之前的研究以及Tremfya目前的处方信息基本一致。详细结果将在即将召开的医学会议上公布。
Tremfya是一种抗白介素23(IL-23)p19亚基的人单抗,该药是第一个被批准的选择性IL-23抑制剂。IL-23是一种细胞因子,在多种自身免疫性疾病中发挥了关键作用。目前,Tremfya也正开发用于其他自身免疫性疾病的治疗,包括克罗恩病(IIb/III期)、溃疡性结肠炎(IIb/III期)、化脓性汗腺炎(II期)。Tremfya通过皮下注射给药,治疗斑块型银屑病的用药方案为:在第0、4周分别给药一次,之后每8周给药一次,剂量为100mg。
截至目前,Tremfya已在全球多个国家和地区获得批准。在中国,Tremfya已于今年6月下旬申报上市。值得一提的是,Tremfya还被列入了中国国家药品监督管理局(NMPA)药品审评中心(CDE)发布的《第一批临床急需境外新药名单》,治疗适应症为:红皮型银屑病、斑块型银屑病、脓疱型银屑病、银屑病关节炎、寻常型银屑病。
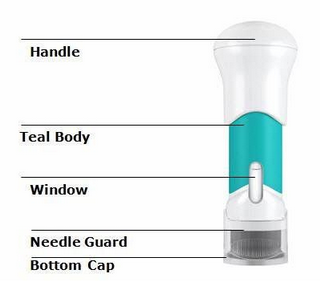
Tremfya新型One-Press单剂量自我注射器
今年2月底,Tremfya新型One-Press单剂量自我注射器获美国FDA批准上市,这是FDA批准的首个提供One-Press(一次按压)患者控制注射器的产品。One-Press是精心为患者设计的:可以舒适地放在手上,提供可控制的注射,并且整个过程中隐藏针头。
One-Press的设计允许患者控制注射的速度和压力,在注射完成时会有一个轻轻的滴答声提示,近99%的患者报告首次注射成功。此外,One-Press还包括一个安全系统,在使用后保护针头。
Tremfya需在医生的指导和监督下使用,经过医生的批准和适当的培训后,患者可以使用Tremfya One-Press自行注射。在临床研究中,患者对Tremfya One-Press的“自我注射满意度”平均评分为9.18分(10分表示“非常满意”),而“易用性”平均评分为9.24分(其中10分表示“非常容易”)。
原文出处:Janssen Submits Application to U.S. FDA Seeking First-in-Class Approval of TREMFYA? (guselkumab) for Treatment of Adults with Active Psoriatic Arthritis
