吸光度与浓度的关系是线性关系。
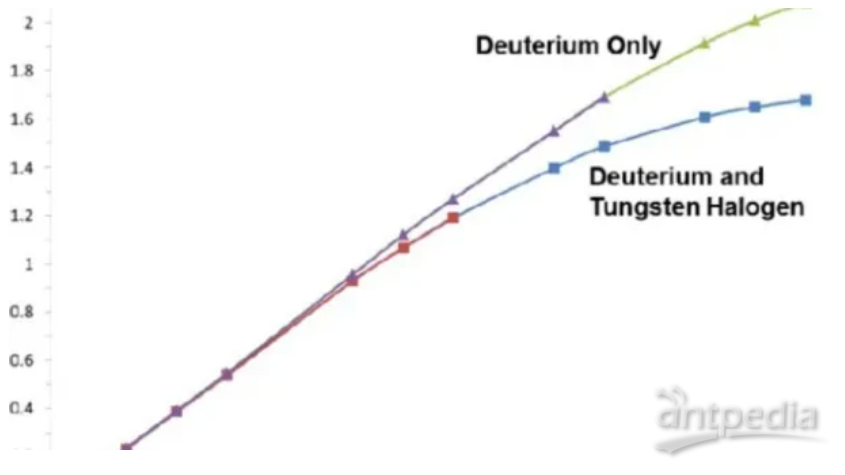
吸光度与浓度的关系是光谱分析中的基本概念,通常遵循比尔-朗伯定律(Beer-Lambert Law)。下面通过解释和表格来展示它们之间的关系。
比尔-朗伯定律描述了单色光通过均匀溶液时,溶质吸收光的程度与溶液的浓度和光程长度之间的关系。该定律表达为:
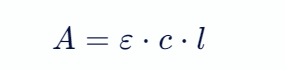
其中:
A 代表吸光度(Absorbance),是无单位量。
ε 代表摩尔吸光系数(Molar absorptivity),单位通常是 L/(mol·cm)。
c 代表溶液的浓度,单位是 mol/L。
l 代表光程长度,即光通过溶液的距离,单位是 cm。
根据比尔-朗伯定律,在固定摩尔吸光系数和固定的光程长度下,吸光度与溶液的浓度成正比。这意味着:
当溶液浓度增加时,吸光度线性增加。
反之,溶液浓度减少时,吸光度线性减少。
| 参数项 | 说明 |
|---|---|
| 吸光度(A) | 溶液中溶质吸收光的程度,依据比尔-朗伯定律与浓度成正比。 |
| 浓度(c) | 溶液中溶质的摩尔浓度,单位通常是 mol/L,直接影响吸光度的大小。 |
| 摩尔吸光系数(ε) | 溶质的特性参数,表明溶质对特定波长光的吸收能力,单位 L/(mol·cm)。 |
| 光程长度(l) | 光通过溶液的路径长度,单位是 cm,与吸光度成正比。 |
| 正比关系 | 吸光度与浓度在固定光程长度和摩尔吸光系数的情况下呈线性正比关系。 |
| 应用 | 利用这一关系可以进行定量分析,通过测量未知溶液的吸光度来计算其浓度。 |
| 实验条件 | 实验操作中需控制入射光的波长、溶液的温度和光程长度等条件以遵循比尔-朗伯定律。 |
| 限制 | 定律假设溶液中无相互作用且溶质完全溶解。在高浓度或含有悬浮颗粒的溶液可能不适用。 |
综上,吸光度与浓度之间的直接关联性使得比尔-朗伯定律成为光谱分析中定量测定的基础。通过适当的校准和严格控制实验条件,可以准确地使用吸光度来测定溶液中的溶质浓度。在实际分析过程中,需要注意控制各种实验条件,以确保结果的准确性。
