病例资料
患者女,51 岁,因“发热2 月余,左侧腰痛3 天”入院。
患者2 月前无明显诱因出现发热,体温多不超过38℃,下午及傍晚明显,伴双下肢肌痛,间中伴畏寒、鼻塞、流涕、咳嗽、咳痰,当地拟诊“上呼吸道感染”予抗感染治疗后咳嗽、咳痰好转,仍有发热、鼻塞、流涕。
再次就诊诊断“鼻窦炎伴鼻息肉”,行“鼻息肉摘除术+多个鼻窦开放术”。
术后病理示:慢性鼻窦炎并炎性息肉形成。
术后鼻塞、流涕好转,但仍反复发热,多在37~39℃,先后予“左氧氟沙星、特治星+拜复乐”等抗感染治疗2周效果欠佳。3天前无明显诱因出现左侧腰部胀痛不适,伴面色苍白,
查:WBC 13×109/L,NEUT 84.7%,Hb 50 g/L,PLT 322×109/L,CT示:双肾实质出血,左肾包膜下出血、积血,脾脏增大,腹膜后淋巴结肿大,腹腔积液,予“输血”等治疗后,为进一步诊治入住我院。
起病以来,精神一般,胃纳较差,睡眠差,夜尿稍增多,尿量1500~2500 ml,大便干结,体质量下降7 公斤。否认高血压、肾炎、糖尿病病史。
入院查体:T:38℃,P:116次/分,R:18次/分,BP:149/93 mmHg。结膜苍白,左下腹轻压痛,脾肋下2 cm可及,质软,左肾区叩痛(+),余无异常。
入院查血常规示:WBC19.1×109/L,NEUT87.7%,Hb 80 g/L,PLT 392×109/L,Scr 277.0 μmol/L,BUN20.5 mmol/L,HCO3-19.7 mmol/L,Alb 28.0 g/L,ALT 32 U/L,AST 28 U/L,CHOL 3.69 mmol/L,LDH 401U/L,C3 1.0 g/L,超敏C 反应蛋白(HsCRP)205.6 mg/L。
尿常规:PRO 微量,尿RBC 30 个/μl,尿WBC 58 个/μl。PT 17.9 s,Fib 7.66 g/L,APTT 57.6 s,PTA 58%,INR 1.48,D⁃二聚体>20 μg/ml,RF:199 IU/ml,ESR:140 mm/h,ASO 423 IU/ml,HBsAg(-),狼疮四项、ENA 系列、ANCA 均为阴性,coombs’试验阴性,G6PD、AFP、CEA、甲状腺功能均未见异常,抗心磷脂抗体阴性,尿渗透压377 mOsm/L,骨髓涂片未见异常,血培养、尿培养、骨髓培养均为阴性,结核抗体(-)。
入院后予“美罗培南”抗感染、补充白蛋白、输浓缩红细胞、新鲜冰冻血浆、补充维生素K1、静滴凝血酶原复合物(康舒宁)等治疗,患者仍发热,体温波动于39~40℃。
入院第6 天突发右侧腰痛,血常规示WBC 22.1×109/L,NEUT 88.7%,Hb 57g/L,PLT 342×109/L。
双肾B 超示:右肾114 mm×80 mm,皮质11 mm,左肾123 mm×90 mm,皮质12 mm,双肾周血肿,右肾不排除活动性出血可能。
腹部增强CT 示:左肾实质及包膜下出血,左肾体积显著增大;右肾实质出血,右肾体积稍大;双侧肾周渗出、炎症。见图1。
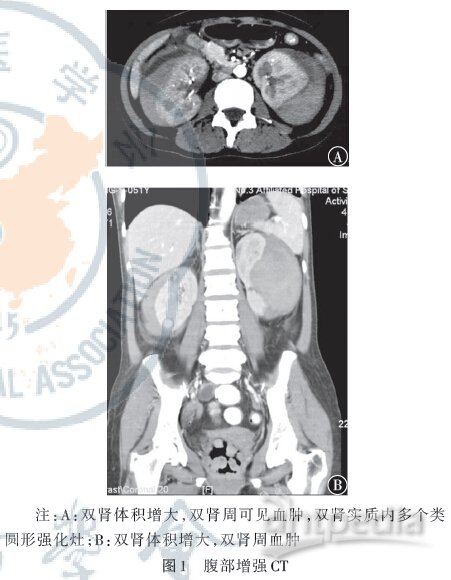
诊断:介入血管科及风湿科会诊,考虑血管炎引起肾出血可能性大。
治疗:予甲强龙(0.5g/d)+丙种球蛋白(20 g/d)冲击治疗3 d后,患者体温降至正常,右侧腰痛减轻,后继续予甲强龙40 mg/d,CTX 1.0 g/月静脉滴注治疗。
经上述治疗,患者病情稳定,精神睡眠好转,复查Hb 维持在83 g/L,Scr108μmol/L,HsCRP 45 mg/L,凝血功能恢复正常,床边B 超示双肾血肿无明显增大,三周后复查双肾CT 示血肿吸收变小。目前该患者在门诊随诊治疗。
讨论
结节性多动脉炎(PAN)是中等或小血管坏死性血管炎,机体各器官均可受累,最常受累的器官包括皮肤、肾脏、胃肠道和周围神经,其临床表现无特异性,包括发热、体质量下降、贫血、腹痛等消化道症状以及心血管系统改变。若肾脏受累主要表现为蛋白尿、血尿、管型尿,也可表现为高血压或急性肾衰竭。
实验室检查急性期可见白细胞、中性粒细胞升高;CRP、ESR升高;C3下降、RF阳性;ANA、ANCA阴性;约1/3患者HBSAg(+),合并肝功能异常。
由于病灶呈节段性分布,活检阳性率低。血管造影或影像学检查发现广泛动脉瘤或者动脉串珠样改变是PAN 最具诊断价值的发现。PAN 主要累及动脉,很少累及静脉,逐步形成微动脉瘤,没有肉芽肿性炎症,无相关抗体(ANCA、anti⁃GMB)。
根据1990年美国风湿病学学会(ACR)的分类标准,该患者出现肌痛、体质量下降、血压升高、肾脏损害,CT+增强提示动脉呈瘤样扩张,考虑诊断PAN成立,予激素冲击、丙种球蛋白和环磷酰胺治疗后病情稳定好转。该患者存在凝血功能异常且有明确的肾脏出血,故没有肾穿刺活检。
自发性肾脏出血(spontaneousrenal hemorrhage,SRH)分包膜下和肾周出血两种,典型的临床表现一般有上腹或腰肋剧痛、腹部肿块及内出血三大症状,肉眼血尿不常见,多与原发病或集合系统累及有关。
自发性肾脏出血的病因包括①肾实质病变:见于肾肿瘤,常见是肾癌;②良性肿瘤如错构瘤,还有肾动脉瘤、肾血管畸形,肾动脉栓塞、肾动脉周围炎、肾动脉粥样硬化、肾静脉栓塞形成;③肾囊肿、肾感染、肾结核以及异体移植肾等。
国外学者报道肾出血最常见的原因是肾细胞癌和错构瘤,治疗主要以手术切除患肾或栓塞治疗。我国学者报道与国外相似。Zapzalka 等发现PAN 大约80%累及肾动脉,出血时需要栓塞治疗。
国内虽曾报道一例ANCA(+)、抗MPO 抗体(+)的PAN 并肾周血肿。本例患者ANCA(-)、凝血功能异常,造成诊断上的困难。凝血功能异常导致的出血临床主要表现为静脉穿刺点出血不止、皮肤瘀斑、肉眼血尿、阴道出血等。该患者通过激素和丙种球蛋白治疗后,肾出血停止,凝血功能恢复正常。
因此肾脏出血考虑是PAN 所致动脉瘤破裂所致,凝血功能异常为肾脏出血后的继发性改变。PAN 的特点是主要累及动脉,很少累及静脉,逐步形成微动脉瘤,动脉瘤破裂导致出血。CT和选择性肾动脉造影是确定出血范围和检查病因最有价值的辅助检查,可以避免不必要的栓塞或肾脏切除。
因此,当肾脏出血时,我们除了考虑肿瘤等原因外,尚需注意PAN 可能,以免误诊。PAN 若未经治疗,预后差,死亡率高,如能规范治疗,5年生存率在90%左右,因而早诊断、早治疗对改善预后非常重要。