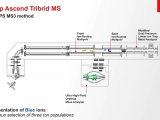
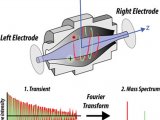
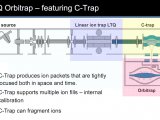
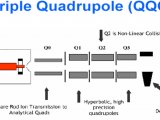
近日,国家药典委员会公示的《元素杂质通则》草案(以下简称“草案”),提出了多种元素杂质的测定方法,包括电感耦合等离子体质谱法(ICP-MS)、电感耦合等离子体原子发射光谱法(ICP-OES)、原子吸收分光光度法(AAS)、X射线荧光光谱法(XRF)等。
草案中对仪器分析参数的选择和设置提供了详细的指导,强调了根据仪器制造商的说明书或操作指南进行优化的必要性。草案特别强调了分析方法验证的重要性,要求通过验证来证明方法满足预期的质量控制目的。验证内容涵盖专属性、线性及范围、准确度、精密度、定量限与检测限、耐用性等多个方面,确保了测定方法的科学性和有效性。
草案提出了系统化的元素杂质风险评估程序,包括潜在元素杂质的识别、来源的考察、以及对药品中潜在元素杂质水平的影响因素的评估。这一程序的建立,有助于制药企业更全面地理解和控制药品中的元素杂质。
此外,草案中定义了元素杂质控制的阈值,即元素杂质PDE值的30%作为控制阈值,用以判断药品中的元素杂质是否需要额外的控制。这一阈值的设定,为药品中元素杂质的控制提供了明确的标准。
我委拟制定元素杂质通则。为确保标准的科学性、合理性和适用性,现将拟制定的元素杂质通则公示征求社会各界意见(详见附件)。公示期自发布之日起一个月。请认真研核,若有异议,请及时在线反馈,并附相关说明、实验数据和联系方式。来函需打印后加盖公章,个人来函需打印后本人签名,并邮寄至我委通讯地址。
公示期满未回复意见即视为对公示标准草案无异议。
联系人:徐昕怡、朱冉
电话:010-67079522、010-67079581
通信地址:北京市东城区法华南里11号楼 国家药典委员会办公室
邮编:100061

公示稿
附件1