助力 COVID-19 疫苗开发
在 Wave 25 中的 Vero 细胞培养
自 2019 年末至今的新型冠状病毒(COVID-19)肺炎疫情出现以来,全国各地人民,不论身处何地,从事什么职业,都积极投身到防护抗疫的工作当中来。尤其是令人尊敬的医学工作者和科研人员们,夜以继日,争分夺秒,拼尽全力,希望能加快结束疫情的进程。
疫情当前,越来越多的创新药企投入到新冠肺炎疫苗的研究开发工作当中来。2 月 10 日,中国疫苗行业协会官方微信发文称,已有 18 家会员单位正在开展新冠肺炎疫苗的研制工作。病毒毒株在实验室中使用 Vero 传代细胞系的成功分离,为后续病毒分析提供了重要科学支撑,为预防用新冠病毒疫苗及抗病毒药物的开发奠定了坚实基础。
介绍
Vero 细胞最初起源于非洲绿猴肾,已知对多种病毒如 SV40、 SV-5、 麻疹病毒、虫媒病毒、呼吸道肠道病毒、风疹、猿腺病毒、脊髓灰质炎病毒、流感病毒、副流感病毒、牛痘病毒等都敏感。对于体外扩增冠状病毒,如严重急性呼吸道综合症(SARS),中东呼吸道综合症(MERS),以及 COVID-19,Vero 都是我们首选的细胞,且被广泛应用于针对相应疾病的疫苗开发 [1]。
作为贴壁细胞,Vero 细胞需要生长于一定的表面,在小规模状态下可以用 T 型培养瓶、滚瓶或细胞工厂来进行培养,但是对于未来需要放大到上百升甚至上千升的疫苗生产来说,这些方法便会受到占地空间,人工成本,无法控制培养参数等条件的极大制约,尤其是污染对生产带来的巨大损失是企业无法接受的。
随着一次性技术的发展,越来越多企业考虑将 Vero 贴附在微载体上,并在一次性生物反应器中进行培养。一次性波浪式反应器 Wave 相比前面提到的开放式培养环境更加安全;相比于不锈钢或玻璃罐则无需清洗和灭菌,具有安全快速,操作便捷的优势。缩短研发及生产时间在抗击这场疫情中显得尤为重要。
本文介绍了如何通过 Wave 一次性生物反应器进行生产流感病毒 [2],对目前的 COVID-19 疫苗研发和小规模生产具有很好的借鉴意义。
内容概要
材料和方法
01
Vero 细胞在 T 型瓶中的培养
细胞系:Vero 细胞,来源 ATCC (Nr. CCL81)
先将 Vero 细胞解冻并在 T 型瓶中进行培养,使用 HyCloneTM VaccineXpress 无血清培养基,细胞接种密度为 4 × 104 cells/cm2,培养条件为 37°C, 5% CO2 对传代维持培养,先使用 PBS-EDTA 洗涤细胞, 然后加入 TrypLE™ Select 或 Accutase 重组蛋白酶解离细胞。
细胞贴附微载体扩增和接毒均在 WAVE 中进行。
02
微载体准备
在硅化玻璃容器中加入 Cytodex-1 微载体进行溶胀,使用 PBS 洗涤 3 次,然后 121°C 高压灭菌 15 分钟。将灭菌完成的微载体用培养基洗涤后转移到 WAVE 一次性反应袋子中。
03
WAVE 生物反应器培养
准备好 10L 的 Cellbag 细胞培养袋,加入上述培养基的同时添加三种补料:Pluronic®F-68, soy peptone (Fluka), soybean-derived trypsin inhibitor (Sigma-Aldrich; 1 mg/mL in PBS)(WAVE 为非介入式搅拌,剪切力低于搅拌罐,仍需要加入这些物质来保护细胞),然后加入准备好的微载体使其终浓度为 3 g/L 进行平衡。
最终培养体积定为 2L,培养条件为 37°C, pH 7.2, 5% CO2,DO 通过 WAVE 自控,细胞接种密度 4 × 105 cells/mL。
为了使 Vero 细胞更好的贴附在微载体上扩增,我们对摇摆参数进行了摸索:
1. 间歇培养模式 6 小时 (16 rpm/4.5° for 2 min, then 0 rpm/0° for 18 min),为了使细胞更好扩增,静止 2 小时后再转移到连续培养模式 11 rpm/4.5°;
2. 间歇培养模式 6 小时 (16 rpm/4.5° for 2 min, then 0 rpm/0° for 8 min),为了使细胞更好扩增,静止 2 小时后再转移到连续培养模式 11 rpm/4.5°;
3. 一直使用连续培养模式 11 rpm/4.5°;
4. 一直使用连续培养模式 12 rpm/5°;
5. 先使用连续培养模式 12 rpm/5°,24 小时后将摇摆速度提升至 14 rpm。
我们发现间歇培养模式会使细胞贴附效果更好 [3], 而连续培养模式则使细胞贴附更加均匀。这里我们选用第(5)种摇摆参数。
04
病毒扩增
病毒为 Influenza A/Solomon Islands/3/2006 (H1N1) IVR145 WHO,创建 virus stock,通过半数细胞感染剂量 (TCID)50 测得其滴度为 106.9。优化得到的感染条件为 TOI, 48 小时,感染时细胞密度为 1.1 × 106 cells/mL;TOH, 72 小时;感染时 trypsin 浓度为 12.5 µg/mL ,病毒稀释比例 1:1000,MOI 计算为 0.004,温度为 37°C。
实验结果
通过对补料条件的优化,我们最终选择了 0.2% Pluronic F-68、0.3% 大豆蛋白胨和 20 mg 胰蛋白酶抑制剂。
图 1. 培养 48 小时后对 Vero 细胞形态进行观察(A)不加补料;(B)加入上述补料
图 2. 添加上述补料对细胞扩增的影响情况
对 WAVE 培养情况进行取样观察,48 小时 Vero 细胞基本已经扩增且均匀布满 Cytodex-1 表面:
图 3.(A)培养 5 小时后;(B)培养 48 小时后
病毒侵染后细胞病变结果(CPE)如下图所示,72 小时被侵染的细胞完全脱离微载体并裂解:
图 4.(A)侵染 24 小时后;(B)侵染 72 小时后
TCID50 结果如图:
图 5. 在 WAVE 一次性生物反应器中做的 7 个不同批次的 TCID50 结果 (TOH 72 h)
同时,我们在病毒侵染后的不同时间取样测试血凝素 HA,通过 Biacore 分析 [4];感染效价通过 TCID50 方法分析。感染峰值较早,出现在感染后的 72 小时。而 HA 浓度则在这几天内缓慢增加:
图 6. HA(通过 Biacore)和 TCID50 动力学分析·
总结与讨论
本文通过 WAVE 一次性生物反应器实现了流感病毒在 Vero 细胞的体外扩增,对当下 COVID-19 疫苗研发和小规模生产具有一定借鉴意义。
通过 WAVE 实现的病毒增殖可以快速的放大到更大规模的搅拌式生物反应器上,而且无需担心污染风险,大大缩短了疫苗研发及生产时间。
使用 HyCloneTM VaccineXpress 无血清培养基获得了较好的实验效果并且能够避免人用疫苗法规的监管风险。
我们对 WAVE 反应器上诸多的培养参数进行了优化,包括如何降低剪切力,如何使 Vero 细胞更好的贴附在微载体上扩增等。
另外我们通过 Biacore 对病毒抗原(HA 为例)以及通过 TCID50 对效价进行了动力学分析,优化的 TOH 基于侵染后能够较早的达到感染峰值,对于裂解疫苗和亚单位疫苗,感染活性是不相关的,因此我们可以晚些收获以获得最大量的病毒抗原。
虽然本文没有对放大效果进行分析,但是 WAVE 已经帮助许多家企业的项目成功放大至 50-2000L 规模的一次性生物反应器。最后我们总结一个简明的病毒增殖流程示意图:
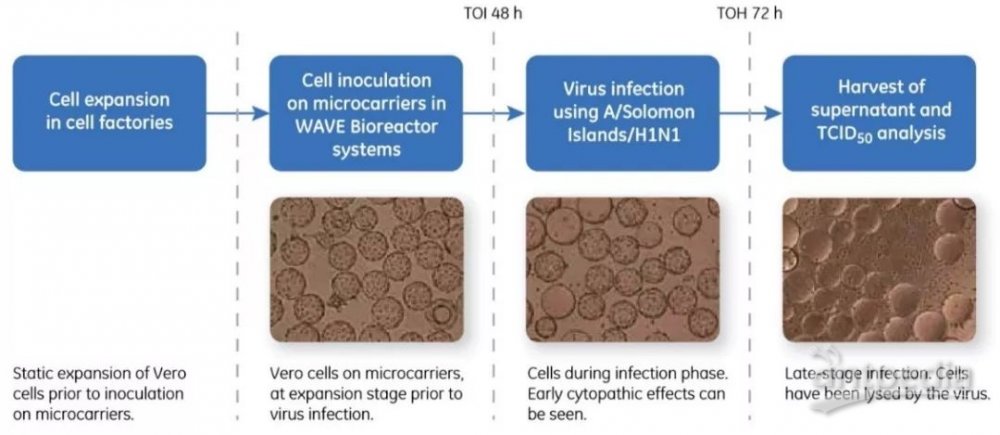
图 7. 在 WAVE 一次性生物反应器中通过 Vero 细胞增殖流感病毒的示意图
助力疫苗开发 我们在行动
为助力 COVID-19 疫苗开发,在各省市道路还在管制的情况下,我们多方协调,快速响应,紧急将机器运送到大江南北,完成安装并远程培训,全力支持新冠疫苗项目开发。
众志成城,齐心抗疫。
相信春天就在不远处。
参考文章
[1]. History and Characterization of the Vero Cell Line - A Report prepared by CDR Rebecca Sheets, Ph.D., USPHS CBER/OVRR/DVRPA/VVB for the Vaccines and Related Biological Products Advisory Committee Meeting, OPEN SESSION www.fda.gov pdf (2000).
[2]. Propagation of influenza virus in Vero cells using Cytodex™ microcarriers in WAVE Bioreactor™ systems, GE Healthcare, 28-9992-69, Edition AB (2012).
[3]. Application note: Vaccine process development using Cytodex microcarriers in WAVE Bioreactor systems, GE Healthcare, 28-9576-34, Edition AB (2010).
[4]. Application note: Biacore biosensor assays for quantitation of influenza virus and HCP, GE Healthcare, 28-9771-57, Edition AB (2010).