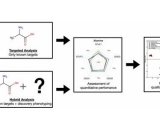
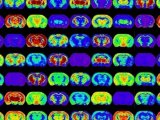
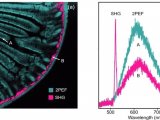
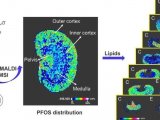
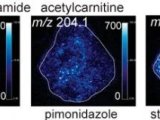
介绍了一种质谱成像定量的模拟组织模型制备方法。在组织匀浆中加入系列已知浓度的分析物标准,将它们分装到模具中并快速冷冻。模拟组织核冷冻切片后置于有组织切片样本的同一载玻片上进行成像和定量。在这个过程中,样本组织和模拟组织经历了质谱成像相同的制备条件。采集成像数据后,由已知浓度分析物的每个模拟组织的平均强度信号生成标准曲线。该标准曲线可用来计算组织中的目标分析物含量。组织模拟样本建立校正曲线,考虑了基质抑制和分析物提取效率的影响。
放射自显影(QWBA)是广为使用的获取药物组织分布信息的主要方法。然而,生成的分布图像代表了各成分放射性强度的总和,包括母体药物、代谢物、降解产物和杂质的各种组合,这使得了解生化途径和机制受到很大限制。在过去十多年中,质谱成像在分析药物组织分布方面显示出越来越大的优越性,其特点是测量分子特征的质荷比(m/z)和强度,不需要同位素标记,可使用有限组织样本,单个实验可同时得到母体药物、代谢物和内源性分子的组织分布情况。质谱成像虽然功能强大,但其定量效果受很多因素的影响。和其它质谱分析一样,如不使用参照标准,测量的离子强度就不能直接与绝对量相关联。这是因为分析物信号强度受到包括萃取效率、电离效率、基质抑制等因素的影响。此外,一些独特的因素如组织微环境的完整性、离子化前没有色谱或样品净化使MALDI质谱成像的定量变得更加复杂。从细胞水平看,组织是一个非常复杂的体系,相邻区域可能由不同类型的细胞构成,他们表达的分子成分可以有很大差异。在一些已报道的MALDI质谱成像的药物定量方法中,描述了在对照样本的组织表面点加系列浓度的标准品来建立校正曲线。第一种方法是把标准品直接加到玻片上的组织基质替代物中,需定量的样本也在玻片上。这个过程虽然简单,但没有考虑组织中待测物的基质抑制和提取效率。
第二种方法是把标准品加到对照组织切片上,这考虑了基质抑制,但忽视了组织中待测物的提取效率。
第三种方法是GSK的Stephen Castellino小组提出的,用添加已知浓度标样的组织匀浆作为参照标准来建立标准曲线。这样做的优点是基质抑制和待测物提取和实际样本接近,得到的定量结果更准确,缺点是要精心设计的模拟组织制备过程。
 该模拟组织模型的设计目标是尽可能接近给药组织的真实情况,校正分析物提取和离子抑制的差异对信号强度的可能影响。该模型的优点之一是灵活设计,其中匀浆核的数量、组织类型、标准品数量、浓度范围等都可以按需要调整。建立模拟模型的操作步骤包括选取模拟组织和确定样品量、组织匀浆、准备模具、配制标准品和匀浆加标、制备模拟组织核和模拟组织核切片。按照美国FDA生物分析方法验证指南,模拟组织模型由六个浓度水平的加标匀浆和一个用于评估检测能力的非加标匀浆。校准曲线应至少有七个点,包括空白。其它六个点应该均匀分布并覆盖预期的浓度范围。包括空白可以更准确地评估检测能力,如空白限(LoB)和检测限(LoD),提供了电路和化学噪音和组织基质的背景干扰情况。 以上内容源自:1. A mimetic tissue model for the quantification of drug distributions by MALDI imaging mass spectrometry. Anal Chem. 2013;85(21):10099-106 M. Reid Groseclose, Stephen CastellinoDOI: https://doi.org/10.1021/ac400892z
该模拟组织模型的设计目标是尽可能接近给药组织的真实情况,校正分析物提取和离子抑制的差异对信号强度的可能影响。该模型的优点之一是灵活设计,其中匀浆核的数量、组织类型、标准品数量、浓度范围等都可以按需要调整。建立模拟模型的操作步骤包括选取模拟组织和确定样品量、组织匀浆、准备模具、配制标准品和匀浆加标、制备模拟组织核和模拟组织核切片。按照美国FDA生物分析方法验证指南,模拟组织模型由六个浓度水平的加标匀浆和一个用于评估检测能力的非加标匀浆。校准曲线应至少有七个点,包括空白。其它六个点应该均匀分布并覆盖预期的浓度范围。包括空白可以更准确地评估检测能力,如空白限(LoB)和检测限(LoD),提供了电路和化学噪音和组织基质的背景干扰情况。 以上内容源自:1. A mimetic tissue model for the quantification of drug distributions by MALDI imaging mass spectrometry. Anal Chem. 2013;85(21):10099-106 M. Reid Groseclose, Stephen CastellinoDOI: https://doi.org/10.1021/ac400892z2. Revised Preparation of a Mimetic Tissue Modelfor Quantitative Imaging Mass Spectrometry. Protocol Exchange 24 August 2018. Jeremy A. Barry, M. Reid Groseclose, Donna D.Fraser, Stephen Castellino
DOI: https://doi.org/10.1038/protex.2018.104