生物被膜(Biofilm)

图 1. 细菌生物被膜示例。金黄色葡萄球菌细胞(球体)包裹在其分泌的聚合物基质中的电镜图[1]
生物被膜(Biofilm)是指附着于有生命或无生命物体表面,由细菌及其分泌的糖、蛋白质和核酸等多种基质组成的群落,是造成病原菌持续性感染、毒力和耐药性的重要原因之一。生物被膜基质由多糖、核酸、脂类、磷壁酸或蛋白质组成的胞外聚合物(extracellular polymeric substances,EPS)构成(图1)。
EPS 基质有助于逃逸宿主免疫反应,还可以使抗生素抗性提高多达1000 倍。除了会导致人牙菌斑和龋齿、慢性感染以及食物中毒等,生物被膜还和大部分的牲畜疾病有关,也同工业空气和水处理系统的污染有关。因此,开发治疗或预防生物被膜的药物至关重要。
多功能 EPS 基质在生物被膜形成初期的菌体定殖、被膜发育和成熟、及其毒力基因表达的整个生物被膜发育周期都必不可少(图2)。由于基质复杂的物理、化学和生物学特性,常规的抗菌方法并不适用于生物被膜菌感染的控制,而需要多靶点或联合治疗。
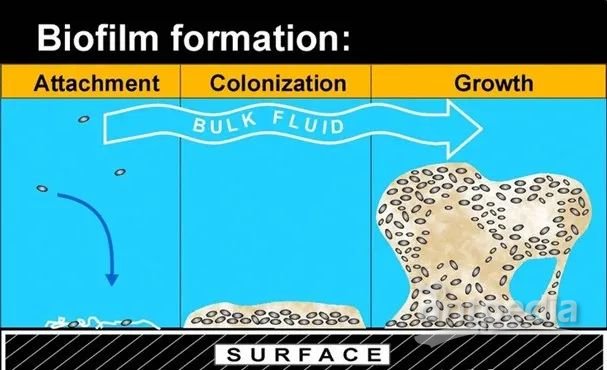
图2. 生物被膜形成过程[2]
最新研究:“天然抗生素”- 穿心莲内酯有效
抑制念珠菌生物被膜的形成
念珠菌的感染威胁生命,特别是其发病率和死亡率很高,作为真菌生物念珠菌也可以形成生物被膜,而且它们对常规治疗的抵抗力与生物被膜的形成密切相关。因此,开发新的方法来研究念珠菌生物被膜和确定新的治疗策略可以产生更好的临床效果。
来自西班牙的科学家首次将Agilent xCELLigence RTCA系统应用到评估真菌生物被膜的实时检测,测试了临床上使用的两组常规抗真菌药物-唑类和棘白菌素对念珠菌的敏感性[3]。结果证明现有的抗真菌药物虽然能阻止念珠菌生物被膜的形成,但是一旦被膜形成,目前的抗真菌药物都很难清除。

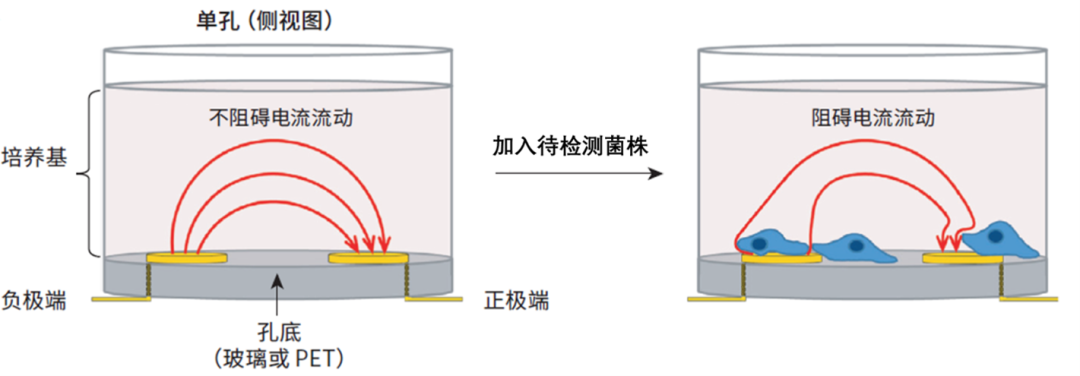
图3. xCELLigence RTCA基于阻抗检测生物被膜原理图。RTCA检测板E-Plate单孔侧视图,在没加入待测菌情况下,电极间的电流自由通过并形成电回路。加入待测菌后由于生物被膜的形成并黏附到电极上,阻碍电流的流动,从而检测到生物被膜的形成与扩大过程的高灵敏读数[1]。
随后,科学家又评估了被誉为天然抗生素的穿心莲内酯的抗生物被膜的效果,从阻抗和扫描电镜等多个角度都证明了穿心莲内酯以剂量依赖的方式强烈抑制了所有测试菌株的生长并抑制了念珠菌属生物膜的形成(图4)。另外,穿心莲内酯也能有效地清除已成熟的测试菌的生物被膜(图5),同时几乎杀死了全部包埋在生物被膜中的菌体。表明作为天然抗生素的穿心莲内酯对治疗真菌生物膜相关的感染具有很大的潜力,基于体外结果,未来也将会进行体内实验,评估其抗感染治疗效果。
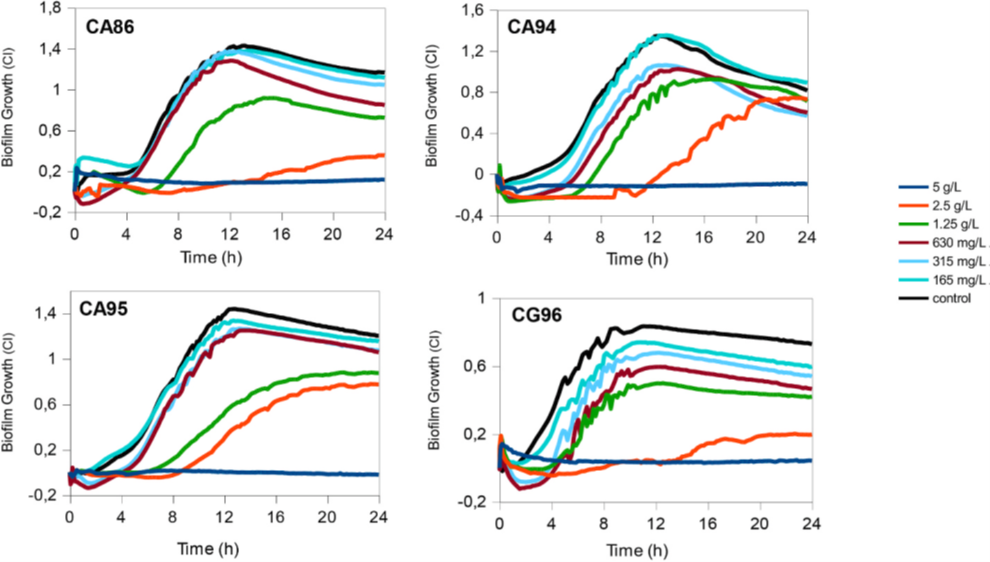
图4. 穿心莲内酯阻止念珠菌生物被膜的形成(同时加入)
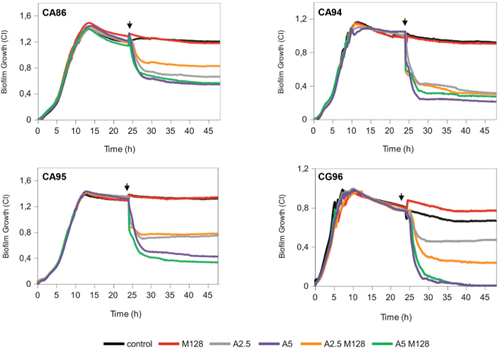
图5. 穿心莲内酯能清除已成熟念珠菌生物被膜(箭头处加入穿心莲内酯)

图6. 处理的24h后的白色念珠菌菌株CA86生物膜的扫描电镜(SEM)结果

应用简报
Agilent xCELLigence RTCA检测平台一直被广泛用于真核细胞的检测,其应用范围包括肿瘤药物发现,免疫疗法效力评估和毒理学研究等。但随着近年来越来越多的研究发现微生物在E-Plate上生长会导致阻抗信号增强,并与其他生长动力学检测结果一致。因此基于阻抗的RTCA很适合应用于生物被膜的研究。区别于传统的结晶紫比色法,RTCA可以实时动态的检测生物被膜形成过程。另外,无人值守的检测过程可以减少人为操作带来的实验误差,在病原菌研究时可以避免过多的暴露。因此,Agilent xCELLigence RTCA检测平台为细菌和真菌等生物被膜的研究提供一个完美的检测工具。

文献列表
Reference
1. Agilent application note: 利用细胞阻抗技术研究细菌生物被膜
2. Lewandowski, Zbigniew & Boltz, Joshua. (2011). Biofilms in Water and Wastewater Treatment. 10.1016/B978-0-444-53199-5.00095-6.
3. Karygianni L, Ren Z, Koo H, Thurnheer T. Biofilm matrixome: extracellular components in structured microbial communities. Trends in Microbiology, 2020, 28(8): 668–681.
4. Žiemytė, M., Rodríguez-Díaz, J. C., Ventero-Martín, M. P., Mira, A., & Ferrer, M. D. (2023). Real-time monitoring of biofilm growth identifies andrographolide as a potent antifungal compound eradicating Candida biofilms. Biofilm, 5, 100134.