2022-8-17 00:17

自1986年第一个治疗性单克隆抗体(mAb)获批以来,mAbs已经成为发展最快的药物。超过80种mAb药物已被批准用于治疗,目前还有更多的mAb正在开发中。对mAbs药物开发至关重要的是对其分子量大小和电荷变异体进行表征。分子的异质性会影响mAb药物的稳定性、有效性和安全性。
传统方法表征分子量大小异质性是通过十二烷基硫酸钠聚丙烯酰胺凝胶电泳(SDS-PAGE)。然而,SDS-PAGE具有操作繁琐和重复性差的缺点。十二烷基硫酸钠-毛细管凝胶电泳(CE-SDS)作为一种高分辨率、高精确度和高度自动化的分析方法,在分析mAbs时,其精确度、线性、重复性和分辨率方面远远优于SDS-PAGE。
CE-SDS可以实现非糖基化重链(NGHC)的精确定量。抗体药物的NGHC直接影响其生物功能。NGHC含量是抗体药物质量控制的一个关键指标,CE-SDS方法比SDS-PAGE有更好的分辨率来量化NGHC。
根据ICH(国际人用药品注册技术协调会)指导原则,2018年,全柱成像毛细管等电聚焦电泳(icIEF)技术已经被中国食品药品鉴定研究院(NIFDC)联合国内8家不同公司,共计10个实验室进行了联合验证(Gang, Wu, Chuanfei, et al. Interlaboratory Method Validation of icIEF Methodology for Analysis of Monoclonal Antibodies[J]. Electrophoresis, 2018.),用以定量监测和表征电荷异构体,但CE-SDS尚未进行。为了满足制药行业对CE-SDS方法标准化的需求,并方便不同品牌毛细管电泳设备(CE)和不同实验室之间的方法转移和方法重现,2021年NIFDC进行CE-SDS方法联合验证,涉及13家公司的13个实验室,使用四种不同型号毛细管电泳设备。该验证遵循ICH指导原则,利用一种商业mAb药物,考察验证仪器的精密度、线性、定量限和准确度等内容。
表1. 该项研究参与者和仪器型号

四种类型仪器的电泳图见图1。所有电泳图都含有明确的峰,还原状态下的轻链(LC)、非糖基化重链(NGHC)和重链(HC),同时还观察到五个杂质峰(标记为P1-P5)。在非还原条件下的电泳图中,除主峰外还观察到六个尺寸异构体相对应的峰(标记为P1-P5,在一些运行中还观察到P6)。然而,在四种类型仪器的电泳图中没有观察到比P1-P6更多的杂质峰。杂质的一致性在四种类型的仪器中显现出来。
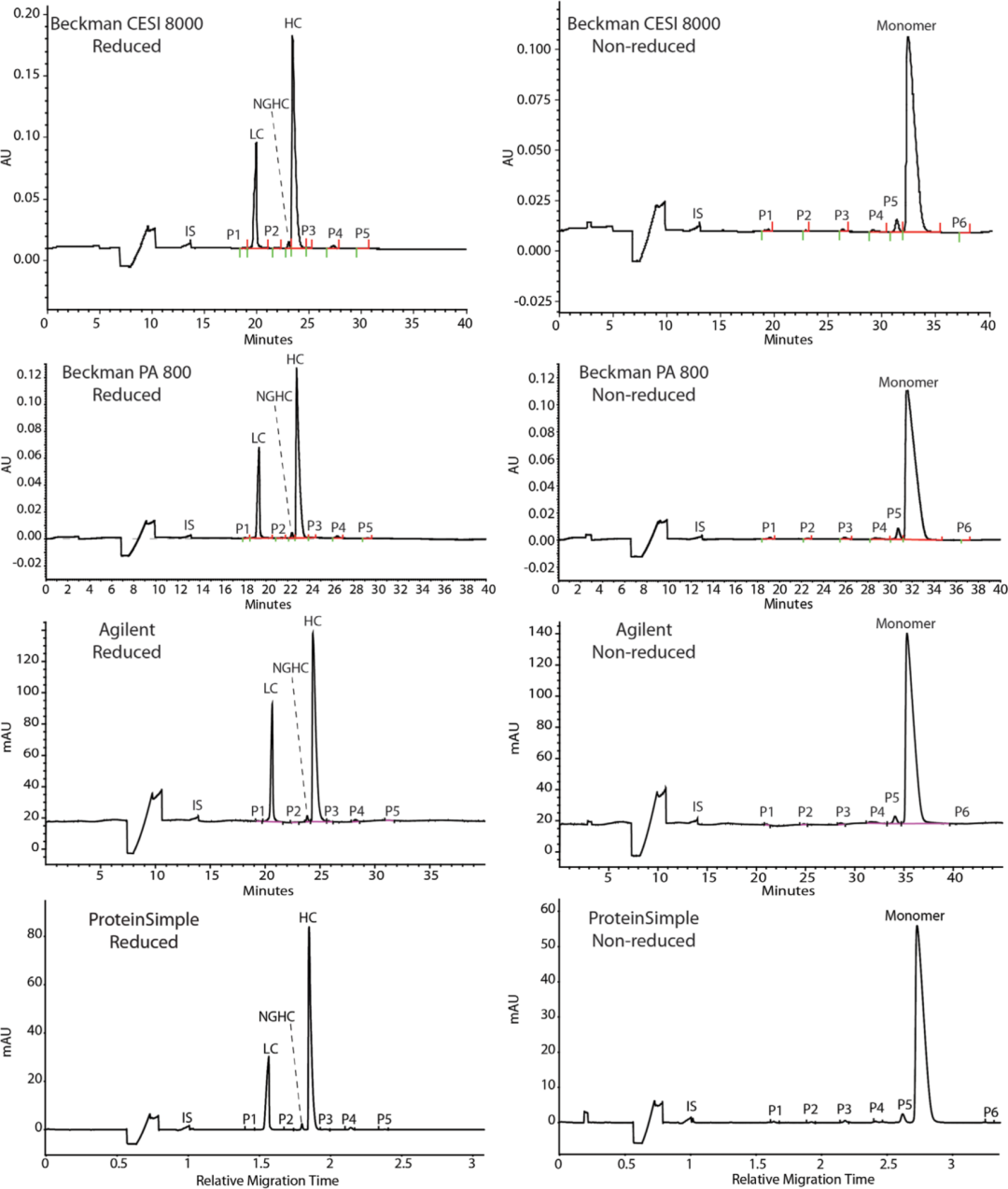
图1. 四种类型仪器电泳图
重复性
分为进样精密度和样品制备重复性。进样精密度主要反映了仪器和方法中使用的试剂的变化。而样品制备重复性除了反映仪器的变化外,还反映了操作者误差的差异。如图2和图3所示,当排除CE9这个异常值后,两组数字有相同趋势(95%置信区间)。在进样精密度方面,12台仪器的杂质百分比范围为3.5-4.6%,单体95.5-96.5%,NGHC 1.0-1.3%,LC+HC总计97.5-98.0%;而在样品制备重复性方面,12台仪器的杂质百分比范围为3.4-4.3%,单体95.7-96.6%,NGHC 1.0-1.3%,LC+HC总计97.3%-98%。这些数值表明,在该方法中操作者的误差影响最小。
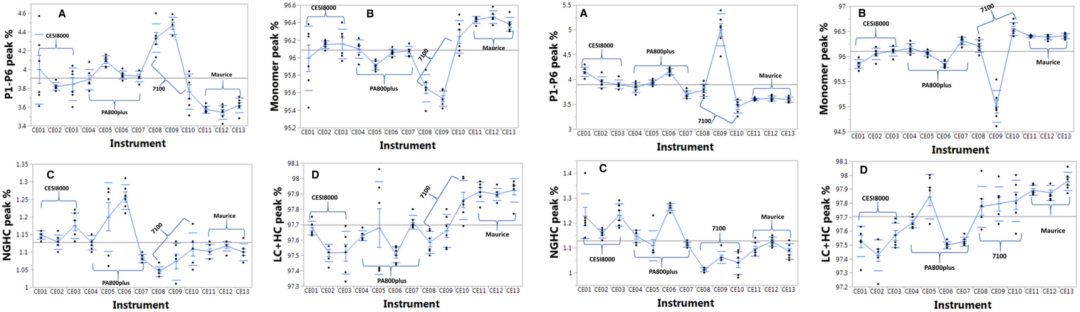
图2左. 13台仪器在非还原和还原条件下的进样精密度;
图3右. 13台仪器的样品制备重复性
批间精密度
每个实验室进行3天实验。在样品制备后,在不同日期使用不同的毛细管,每天进样一次。结果见图4。该测试反映了仪器在多天内的变化。12台仪器(CE9仍是一个异常值)的测试变化范围与重复性测试相同:在95%的置信区间内,12台仪器的杂质百分比范围为3.5-4.3%,单体95.7-96.7%,NGHC 1.0-1.3%,LC+HC总计97.2-98.0%。

图4. 13台仪器的批间精密度
准确度
在0.5、0.75、1.00(目标样品浓度)、1.25和1.50 mg/mL五种不同的样品浓度下,测定了四种成分的回收率,即非还原条件下的杂质(P1-P6峰)和单体;还原条件下的NGHC和LC+HC总量。对于所有仪器来说,四种成分的三次进样(N=3)回收率都在预先设定的回收率标准(83-117%)之内,除了CE4,其回收率在总蛋白浓度为0.5mg/mL时为81%,而且只在非还原条件下。该方法对其预期的应用目标来说是准确的。见图5

图5. 在非还原和还原条件下,13台仪器样品中四种成分的回收率
线性
对于非还原和还原条件下的主要成分(单体和LC+HC总量),所有仪器的R2对于LC+HC来说都>0.94,对于单体来说>0.96。对于次要成分,它们的R2比主要成分小,这是预料之中的。见表2和表3
表2. 单体和杂质(P1-P6)在非还原条件下的线性拟合

表3. HC+LC总量和NGHC在还原条件下的线性拟合
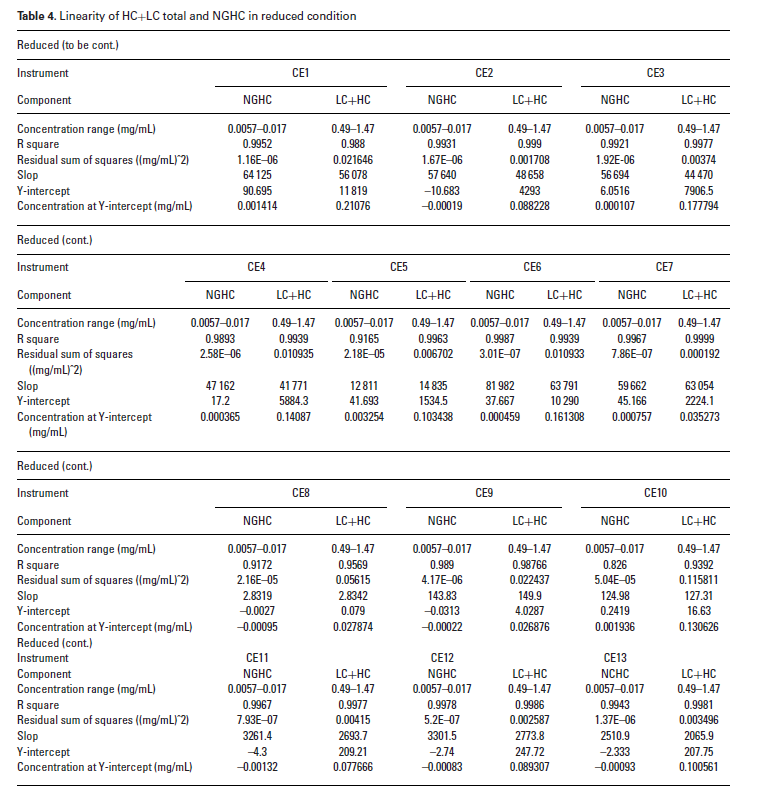
定量限
13台仪器中每台仪器在非还原和还原条件下的LOQ,如表所示,在非还原CE-SDS中为0.46%,在还原CE-SDS中为0.14%。见表4
表4. 13台仪器在非还原和还原条件下的LOQs

样品稳定性
样品在非还原和还原条件下被变性,在仪器的样品盘中存放24小时。除了CE4在非还原条件下24小时后显示出较高的杂质峰面积百分比外,所有仪器在0小时和24小时之间的四个组分峰面积百分比的差异都在重复性测试结果的范围内。见图6

图6. 样品中四种成分的溶液稳定性
结论
研究结果证明,CE-SDS方法符合其预期的应用目的--对于mAb治疗药物的纯度和大小异质性特征检测,该研究的结果减轻了CE-SDS方法开发和方法转移的负担,因为使用任何一种仪器的CE-SDS方法都呈现出预期的重现性、准确性和LOQ。

Maurice全自动蛋白质表征系统采用免组装毛细管卡盒设计与创新性实时全柱成像等电聚焦专利技术,同时具备CE-SDS和iCIEF两种检测模式,双模式符合2020版中国药典。
领域:抗体药物,生物制药/仿制药