拓展单细胞研究的视野
timsTOF SCP 用于定量单细胞生物学研究,具有无偏、深度单细胞 4D-Proteomics™、免疫肽组学、表观蛋白质组学和 PTM 分析,以补充 scRNA-seq。扩大单细胞研究的视野。
重新定义单细胞蛋白质组学
发现真正的蛋白质组异质性
TimsTOF SCP亮点
超高灵敏度
新颖离子源几何形状的突破性设计,可将离子转移率提高 5 倍并具有超高稳定性。
数据完整性
数据独立采集-平行累积连续碎裂 (dia-PASEF) 突破了可重复量化的极限,为大规模研究细胞异质性铺平了道路。
采集速度
高采集速度与 dia-PASEF 灵敏度相结合,可在短液相色谱 (LC) 运行中进行分析,而无需对极低样品量进行色谱稀释。
稳健性
捕获离子迁移谱 (TIMS) 的双正交反射可实现对数千个样品的常规操作,而无需清洁仪器。
TimsTOF SCP特点
从单细胞
质谱蛋白质组学研究细胞异质性和生物学的先进离子光学和 PASEF已成为了解生物功能和疾病机制的现代研究的主要内容。看似同质的健康或患病组织由具有多种不同蛋白质组的细胞组成。破译每个细胞中蛋白质组的挑战——细胞异质性——是充分理解其功能的关键。
timsTOF SCP 提供了一个彻底改进的离子源概念。并行串行累积碎裂(PASEF®) 获取方法,它提供了极高的速度和灵敏度,以处理单个细胞的蛋白质组或少数形态或功能相似的细胞中的翻译后修饰。


timsTOF SCP 具有改进的离子源几何结构,包括 1 毫米毛细管识别,可将离子转移到额外的高压级离子漏斗和 8 级差动抽真空系统中,从而使离子传输率提高五倍。
更大口径的毛细管产生超高灵敏度,额外的正交离子反射和后续漏斗提供了一个单独的、差分泵阶段,保持了 timsTOF 仪器系列所期望的系统稳健性。
timsTOF-SCP改进了离子向源的传输,同时增加了更高压力的真空级,保持了稳定性。这使得离子电流几乎提高了5倍。当结合以100nl/min流速运行的Evosep One-whister方法和dia-PASEF方法时,灵敏度比以前使用Evosep One的高流量结果提高了约100倍。这使得在真正的单细胞水平上的无偏蛋白质组学具有良好的重现性、稳健性和每细胞约1500个蛋白质的首次覆盖率。
捕集离子淌度 (TIMS) 首先是一种气相分离技术。除了高效液相色谱 (HPLC) 和质谱之外,这还通过增加分离维度解决了样品复杂性,提高了峰容量和化合物表征的可信度。
同样重要的是,TIMS 设备还可以积累和富集给定质量和迁移率的离子,从而实现灵敏度和速度的独特提高。
使用双 TIMS 技术可以实现接近 100% 的占空比,促进前部的离子累积,而后部的离子则根据其淌度顺序释放。平行串行积累碎片的过程(黑豹®) 启用碰撞横截面 (CCS) 分析。
启用 CCS 的分析开辟了许多进一步的分析可能性,从化合物鉴定的更大确定性到可靠的库匹配和大型数据集中的较低错误发现率 (FDR)。

除了无偏的真正单细胞蛋白质组学应用外,timsTOF SCP 还为涉及从蛋白质组中富集肽的工作流程提供出色的灵敏度。免疫肽组学研究始于从血浆或组织中纯化免疫肽。
由于免疫肽在这些样本中的丰度相对较低,因此 timsTOF SCP 非常适合用于发现新抗原的免疫肽组学,其中可用材料有限,例如在针活检中。timsTOF SCP 还具有彻底改变磷酸化蛋白质组学用于研究癌症信号通路的敏感性。
肽离子使用捕集离子淌度 (TIMS) 进行分离,洗脱 (~ 100 ms) 并在四极杆飞行时间 (QTOF) 中检测,生成 TIMS MS 热图。在 PASEF ®方法中,使用相同的 TIMS 分离,四极杆在洗脱过程中分离特定离子种类并立即转移到下一个前体。母谱和碎片谱按迁移率值对齐。
并行累积串行分段 (PASEF ® ) 技术实现了 >100 Hz 的测序速度。使用 PASEF ® 可以通过多次选择低丰度肽段来提高它们的 MS/MS 质谱图质量。
PASEF ®:完美适用于鸟枪法蛋白质组学
由 PASEF ®驱动的 timsTOF SCP提供 >100 Hz 的测序速度,而不会降低灵敏度或分辨率。这是通过将四极杆分离质量窗口与来自 TIMS 漏斗的特定肽包的洗脱时间以及碰撞池中的碰撞能量同步来实现的。

timsTOF SCP好处
timsTOF SCP 允许以超过 100 Hz 的测序速度和不折不扣的蛋白质组学深度分析数百个样本,样本量最少(<200 ng)。这改变了蛋白质组学的研究方式,但增加的数据需要更高水平的数据分析。
数据分析是许多工作流程中的常见瓶颈。现代分析方法导致 timsTOF SCP 生成数百行数据。Bruker 引入了实时数据库搜索功能——实时并行数据库搜索引擎 (PaSER),消除了这一障碍。使用 PaSER,LC-MS 运行一完成,结果就可用——有效地运行和完成。
开放文件数据格式允许研究人员直接使用原始数据并使用他们选择的行业领先软件。
Bruker 的 MaxQuant 软件已适应管理保留时间、离子迁移率、质量和信号跨越空间中的 4 维 (4D) 特征强度。这有利于肽、蛋白质和翻译后修饰的鉴定和定量。
PEAKS Studio 将 de novo 测序与传统数据库搜索相结合,并针对处理 timsTOF 原始数据进行了优化。
timsTOF SCP应用
支持 CCS 的分析用于可靠的识别
timsControl 允许定制 dia-PASEF 窗口方案以专注于感兴趣的离子。调整质量隔离宽度、TIMS 范围和循环时间允许 dia-PASEF 适应不同的色谱方法。
将 Evosep One 系统上的低流量液相色谱与 Whisper 与 dia-PASEF 对 timsTOF SCP 的高灵敏度相结合,从 500 pg 细胞消化物中鉴定出 2000 多种蛋白质,从 250 pg 中鉴定出 1500 种蛋白质,证明了分析所需的灵敏度真正的单细胞蛋白质组学。从 250 pg 中鉴定出的蛋白质涵盖了大约 4 个数量级的丰度范围,从而能够在单细胞水平上进行定量蛋白质组分析。

了解 TME 及其浸润的免疫细胞可以被认为是影响疾病进展、治疗反应和患者存活的关键步骤。由于其高灵敏度,timsTOF SCP 能够在通过激光捕获显微切割 (LMD) 从 FFPE 组织样本中切除的细胞上获得足够的蛋白质组深度。典型的工作流程如右图所示。

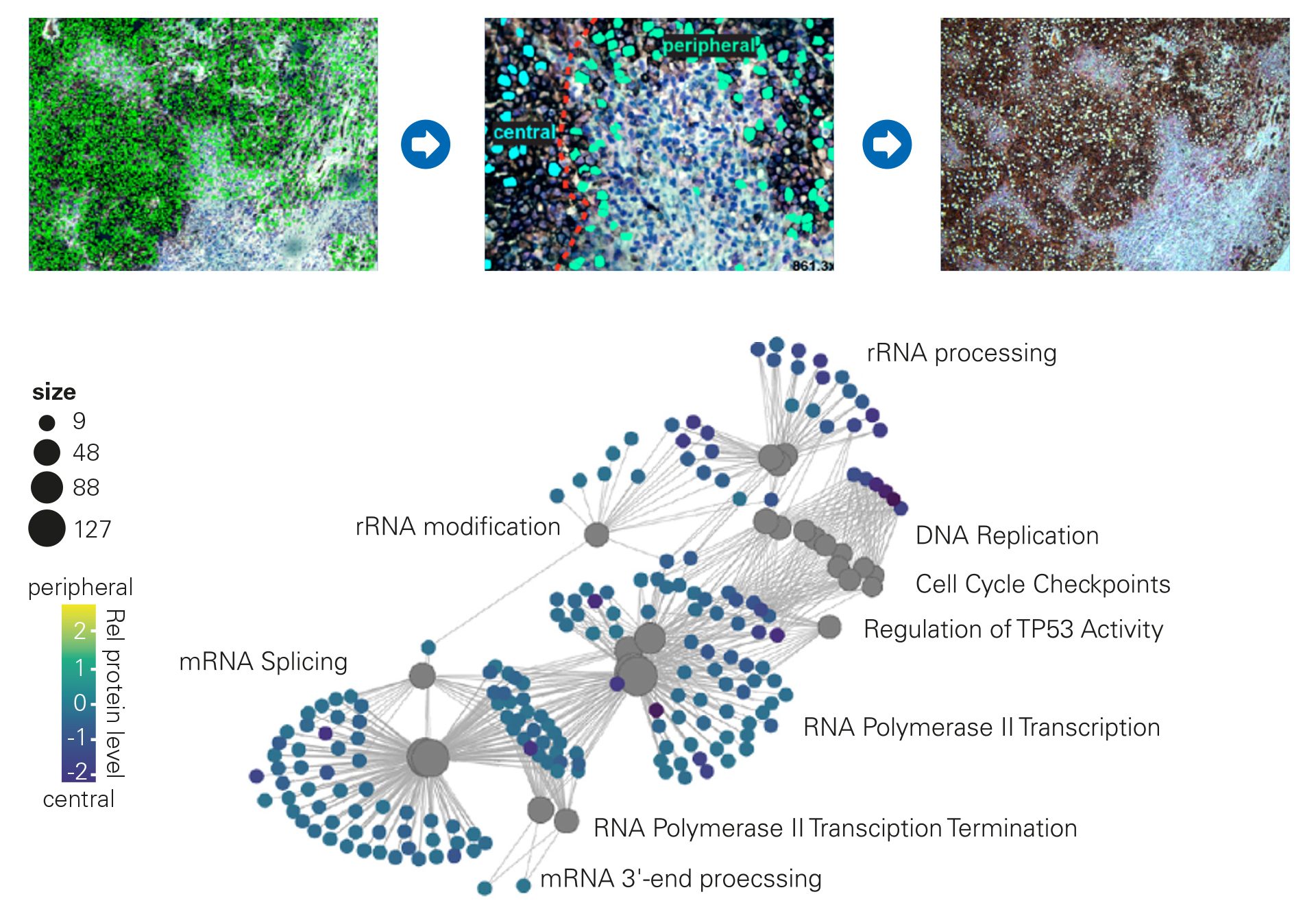
细胞标记物用于识别肿瘤块中的黑色素瘤癌细胞以及与基质密切相关的那些细胞,以便随后通过 LMD 和 timsTOF SCP 仪器上的无偏 4D 蛋白质组学分析分离这两个群体。
主要发现:富集分析揭示了中枢和外周黑色素瘤细胞之间差异调节的蛋白质,具有疾病亚型指导临床决策的潜力。
结果由 Matthias Mann 教授提供(doi:https : //doi.org/10.1101/2020.12.22.423933)
证言
“我一直说单细胞蛋白质组学在我有生之年不会发生,但我很高兴被证明是错的”
Matthias Mann教授,博士,德国马丁斯利德马克斯普朗克生物化学研究所蛋白质组学和信号转导系主任