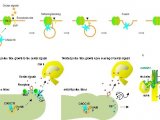
实验概要
了解Nif对花粉管微丝骨架介导的胞吞、胞吐作用的调节作用。
主要试剂
FM4-64 (Molecular Probes,Inc. Eugene,OR)用DMSO溶解,配制成200µM的母液,-20℃避光保存。
主要设备
摇床
激光共聚焦显微镜(ZEISS,META550)
JEM-1230电子显微镜(JEOL Ltd. Tokyo,Japan)
实验材料
白皮松花粉
实验步骤
1. 材料培养
分别称取10mg白皮松花粉,置于以下两种培养基,25℃条件下摇床(120rpm)暗中培养72h。培养基中所含DMSO浓度低于1%,该浓度对于花粉萌发和花粉管生长无影响。
1) 15%蔗糖 0.01%H3BO3 0.01%CaCl2 (CKM)
2) 15%蔗糖 0.01%H3BO3 0.01%CaCl2 250µM Nif
2. FM4-64的装载及共聚焦显微镜观察
取不同培养基72h的白皮松花粉管溶液200µl,加入5µl FM4-64母液,立即混匀,此时FM4-64的终浓度为5µM。孵育10s后,将材料滴于载玻片上,立即在激光共聚焦显微镜下观察,激发波长488nm,发射波长是514nm,连续采集图像。上述操作在黑暗或弱光条件下进行。
3. 胞吞作用能量依赖性检测
标准培养基培养72h的花粉管,首先用500µM叠氮化钠处理10min,随即用上述相同浓度的FM4-64标记,按上述操作进行。
4. FM4-64专一性膜质标记检测
培养72h的白皮松花粉管用FM4-64标记,1min后用25%(W/V)的山梨醇处理10min,使花粉管发生细胞质壁分离,激光共聚焦显微镜下观察并采集图像。
5. 电镜观察
1) 培养72 h的白皮松花粉管用0.1M磷酸缓冲液(pH 7.2)过滤冲洗,收集
2) 立即用2.5%戊二醛固定4h;固定液用0.2M磷酸缓冲液(pH 7.2)配制,并加入2%(w/v)蔗糖。
3) 0.1M磷酸缓冲液冲洗3-5次,每次0.5 h;
4) 1%锇酸再固定4h
5) 0.1M磷酸缓冲液冲洗3-5次,每次0.5 h;
6) 系列乙醇脱水,环氧丙烷过渡,Spurr树脂包埋;
7) LKB-V超薄切片机切片,切片厚度为75 nm;
8) 2%醋酸双氧铀(w/v)染色40 min;0.5%柠檬酸铅隔绝空气染色30 min;
9) JEM-1230电子显微镜80kV下观察、拍照。
6. 花粉管微丝的标记
应用不同浓度Nif处理的花粉管在新鲜配制的4%多聚甲醛(50mM Pipes buffer,pH 6.9)固定1h,固定时同时抽气几分钟。用50mM Pipes buffer洗涤三次,花粉在含有1%果胶酶和1%纤维素酶的50mM Pipes buffer37℃下孵育15min。用50mM Pipes buffer洗涤三次后,样品再用1%Triton -100室温孵育40min。50mM Pipes buffer洗涤三次后,样品用0.2 nM phalloidin-TRITC溶于PBS (pH 6.9) buffer暗处理1 h。滴入50%甘油(含抗荧光淬灭剂),用指甲油封片。在激光共聚焦显微镜下,Ar/Kr激光,激光波长515nm。每个样品取20-30个不同光学切片扫描,最后将所有光切面的图象叠加成像。