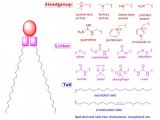
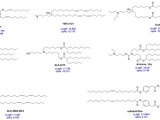
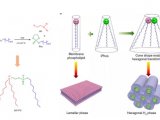
与传统药物相比,纳米药物具有独特的优势,全面、科学、合理地表征纳米药物,制订合适的药品质控指标,建立相应的检测方法是一项非常重要的工作。本文讨论了其中的两个重要参数:粒度及粒度分布、药物载体的包封率以及相应的检测方法。
纳米微粒的粒子尺寸已接近光的波长,纳米微粒有大量的界面或自由表面,表面有很强的活性,可产生特殊的光学、热学、力学和磁学特性,同时纳米微粒间存在着或强或弱的相互作用。
纳米药物不是传统的分子药物(Molecular Medicine),而是颗粒药物(Particles Medicine)。与传统的分子药物相比,纳米药物的最大优点在于:容易进入细胞而实现高效;可链接或载带的功能基团或活性中心多;便于生物降解或吸收;易于实现药物的缓控释放等功能。因此,纳米药物主要用于:⑴改善难溶性药物的口服吸收;⑵靶向和定位释药(targeting drug system,TDS);⑶药物控释;⑷生物大分子的特殊载体等。
目前的纳米药物可分为两类:全新的纳米药物和纳米载体。全新的纳米药物是指直接将原料药物加工成的纳米粒,纳米载体系指溶解或分散药物的各种纳米粒,如纳米脂质体、聚合物纳米囊、纳米球、聚合物胶束等,是利用纳米技术改良的传统分子药物。纳米药物的分析集中在结构和性质的表征,如粒度及粒度分布、分散性、分散稳定性、表面电性能、表面成分及价态、表面自由能和结构等,了解纳米药物的结构和性质,有利于探索它们的生物特性和药理药效学机理。
新药物载体和药物新剂型纳米载体的分析和质量控制不同于它们的前体药物,由于药物颗粒的直径及其分布与药效、药物载体的性质、分布与疗效、药物载体的载药量、包封率、给药剂量、给药方式等都密切相关,因此,须对药物粒径及粒度分布,药物载体性质、载药量和包封率等进行分析和控制。此外,某些特殊的纳米药物如放射性纳米药物的活度等也需进行控制,对纳米药物药理学和药代动力学的研究需采用更高选择性和灵敏度的分析方法。
本文仅讨论其中的两个重要参数:粒度及粒度分布、药物载体的包封率以及相应的检测方法。
粒径及分布
纳米药物制备的关键是控制粒子的大小和获得较窄且均匀的粒度分布,减少粒子团聚现象,保证用药有效、安全和稳定。因此,纳米粒径及其分布是表征纳米药物的最重要的指标参数,也是纳米药物的研发和质量控制中的重要内容之一。
以下介绍了几种应用广泛、比较准确、实用的纳米粒度测量方法。
X射线小角散射法
X射线小角散射法(SAXS)是利用X射线小角散射效应测定纳米颗粒粒度分布的一种有效方法,其相关理论、实验技术和数据处理方法已臻成熟,现已制定了国际技术规范和国家标准。它一般可以测定颗粒尺度为1~300 nm 的超细颗粒的粒度分布,也可以测量无机、有机溶胶以及生物大分子粒度;但不适合于有微孔存在的颗粒以及不同材质组成的混合颗粒。
X射线散射法小角的原理是:当一束极细的X射线穿过纳米粉末层时,经过颗粒内电子的散射,就会在原入射X射线束周围的0~2小角区域内分散开来,其散射强度分布与颗粒的粒度分布相关。若假定试样中的粒度分布是连续的,可以用一种连续的分布函数来表达其粒度的分布。
光子相关光谱法
光子相关光谱法(Photon Correlation Spectroscopy, 简称PCS)又称为动态光散射法,是近年来用于纳米粉体粒度测试的新方法。光子相关光谱法是测量亚微米及纳米颗粒粒度的有效方法,其测量原理基于颗粒的布朗运动。悬浮液中的颗粒由于受到周围进行Brownian 运动的分子的不断撞击,不停地进行随机运动。在激光的照射下,在一定角度下,运动颗粒的散射光也将产生随机的波动。波动的频率与颗粒的大小有关,颗粒越小,波动涨落越快。因此,这种波动包含颗粒的粒径信息。
PCS相比于电镜法的最大优点是可获得精确的、统计的粒径分布,但对于固体,必须是将其制成分散度良好的悬浮液,因此对待测纳米粉体的分散是准确表征纳米粉体粒度的前提。
此外,表征分散体系稳定性的重要指标是Zeta电位,由于带电微粒吸引分散系中带相反电荷的粒子,离颗粒表面近的离子被强烈束缚着,而那些距离较远的离子形成一个松散的电子云,电子云的内外电位差称为Zeta电位。只有Zeta电位在±30 mV以外,体系才是稳定的,颗粒不容易团聚。