本周,素有“科学界奥斯卡”之称的“科学突破奖”(Breakthrough Prize)公布了一年一度的获奖名单。其中,华盛顿大学(University of Washington)蛋白质设计研究所的David Baker教授成为生命科学奖项的四位获奖人之一。

David Baker教授(图片来源:HHMI官网)
Baker教授是人工设计蛋白领域的领军人物,他开发了一种计算机技术,可以创建出自然界中从未见过的蛋白质。而这些具有全新结构的人工蛋白质,有望为影响人类健康的疾病带来新的治疗方法。
近日在顶尖学术期刊《科学》上,Baker教授的研究团队带来了一项新成果:他们设计的蛋白质可以对抗新冠病毒!在培养的人类细胞中,有一款候选蛋白质药物显示出的抗病毒活性,可与目前已知的强效中和抗体相媲美。
我们现在知道,新冠病毒的表面有许多刺突蛋白(Spike protein),这是它们感染人体细胞的关键。刺突蛋白通过其受体结合域(RBD)与人体细胞表面的ACE2受体相互作用,然后进入细胞。因此,干扰这种相互作用,是阻止新冠病毒感染细胞的一种重要策略,起到治疗甚至预防性保护的作用。
在Baker教授的主导下,第一作者Longxing Cao博士与同事们设计了与新冠病毒刺突蛋白紧密结合的小型蛋白。

设计思路的艺术呈现:用计算机构建的小型蛋白结合新冠病毒表面的刺突蛋白,干扰病毒的感染机制(图片来源:参考资料[2];Crdit:UW Medicine Institute for Protein Design)
研究人员采用了两种设计策略,一种是先用计算机生成小蛋白骨架结构,以此为基础整合ACE2受体的片段,提高亲和力;另一种方法,则是在蛋白骨架上对接病毒RBD,识别全新的结合模式,从头开始设计完全合成的蛋白质。
据研究小组介绍,他们在计算机上设计了超过200万个候选的结合蛋白,随后生成了118000多个新蛋白,在实验室中进行了测试。

两种设计策略的示意图(图片来源:参考资料[1])
研究结果发现了10种设计蛋白,可以在100pM~10nM的范围内结合新冠病毒RBD,在体外细胞实验上显示出良好的抑制活性(IC50在24 pM ~ 35 nM)。其中,活性最强的一种抗病毒蛋白由第二种策略产生,即通过全新方式结合RBD。研究人员将其命名为LCB1,其IC50为0.16 ng/ml。按质量计算,LCB1的效力是迄今为止报道的最有效的单克隆抗体的6倍。
“尽管还需要进行广泛的临床试验,但我们相信,这些计算机创建的抗病毒药物中有一些富有前景,它们可以像单克隆抗体一样阻止新冠病毒感染,而且还更容易生产,也更加稳定,因而有望减少对于冷藏的需求。”Cao博士说道。

本研究第一作者Longxing Cao博士(图片来源:参考资料[3];
UW Medicine Institute for Protein Design)
研究团队还进一步通过低温冷冻电镜,验证了新的抗病毒蛋白与RBD相结合时的三维结构,确认其与计算设计模型非常接近。
Baker教授评论说:“我们成功地从头开始设计了高亲和力的抗病毒蛋白,进一步证明了计算蛋白设计可用于创建有前途的候选药物。”
正如科学突破奖的宗旨所言,“支持科学家们致力于解决最重大和最基本的科学问题”,这项新的研究成果也让我们看到,极具创新的蛋白设计方法正在为治疗新冠病毒病提供新的起点。我们也期待科学家们的不断创新具有更广泛的应用,最终帮助我们攻克诸多影响人类健康的疾病。
参考资料
[1] Longxing Cao et al., (2020) De novo design of picomolar SARS-CoV-2 miniprotein inhibitors. Science. DOI: 10.1126/science.abd9909
[2] Antiviral proteins block coronavirus infection in the lab. Retrieved Sep. 11, 2020, from https://www.ipd.uw.edu/category/coronavirus/
[3] Scientists design proteins that could keep coronavirus from spreading COVID-19. Retrieved Sep. 11, 2020 from https://www.geekwire.com/2020/scientists-design-proteins-keep-coronavirus-spreading-covid-19/
一般人对科学家的形象都是,不修边幅,勤勤恳恳在实验室里,受得住寂寞,耐得了无聊。
可是你曾想到,生物实验也可以通过电脑游戏来实现。
David Baker say,of course yes, just foldit!
这个号称解开蛋白折叠奥秘的男人,专注于蛋白设计的科学家,会有什么样的精彩故事呢?
大家都知道,于谦老师有三大爱好,抽烟、喝酒、烫头。
Baker老师也有三大爱好,爬山、玩游戏和发CNS。
第一,爬山探险,不多说直接上图为证。从2013年(可能更早)开始,几乎每年攀登一次雪峰。


二,玩游戏。亲手设计了蛋白折叠游戏“Foldit”,下载地址:https://fold.it/portal/,感兴趣的可以下载玩一玩。游戏界面是这样子的,
就问你炫酷不炫酷。玩到最后还发了篇nature,这些民科级别的游戏玩家,做梦也没有想到自己还能登顶nature。
游戏界面是这样的


最后设计出来的蛋白,还有自然界不存在的结构

实验室的主页也是这么炫酷。光看2019年已经发遍了CNS,还不止一篇。羡慕嫉妒恨吧,没办法人家就是这么牛。
baker为啥可以在蛋白人工设计领域这么厉害呢,究其原因,就是他设计了一个蛋白结构设计算法,Rosetta。以此算法为基础设计出了一大批新蛋白。

首先,构建酶催化模型。其次,搜索与和比对,并进行整合。再次,优化酶的结构与结合力。最后,在大肠杆菌表达并筛选出具有一定功能的新酶。
最后,baker老师在TED演讲的时候,指出人工蛋白设计的五大方向:
设计新型疫苗
设计包含有非天然氨基酸的蛋白质
设计先进的药物输送载体
设计智能疗法
开发高性能生物材料
所以,想为科研做贡献么?下载Foldit吧,玩游戏就可以了。蛋白设计的明天就看你喽!
在我们学习生化的时候,我们都记得这样一句话,蛋白质设计是世界性难题,事实上,这个难题,正逐步被华盛顿大学美国科学院院士David Baker所打破,
尤其是这次这篇工作,直接设计了2万多个多肽,通过酵母展示和高通量测序技术进行富集,并展现了相应的功能,选择了很多高活性的多肽药物,可以有效地阻断流感病毒。
有且只有用“震撼”二字来形容读这篇文章的感受。
我们来看看他们干了什么。
按照我们通俗的理解,设计蛋白是一个难事儿,寻找短的多肽也是一件难事儿,而David Baker则一口气设计的数万种片段。

具体来说,他们瞄准两个不同的蛋白靶点,流感病毒HA,以及神经毒素BoNT,围绕这两个靶点,产生了4000多种蛋白骨架,然后依赖这些模板,根据Rosetta蛋白质设计软件,最终分别设计了7000多和3000多具体的蛋白序列。
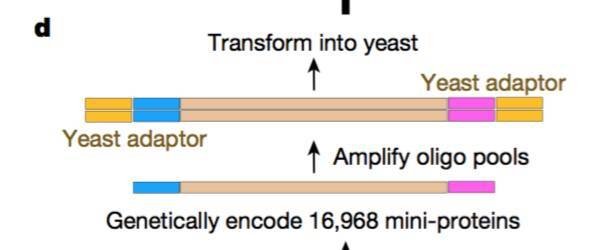
然后将这些文库序列合成在酵母上,进行展示。

经过进一步的优化后,最终科学家们通过表达一些多肽,验证相应的功能。

通过三维结构解析,可以看到与预测的模型非常吻合,同时有非常强的稳定性。