阿尔茨海默病 (AD) 的特征是进行性突触功能障碍、神经元死亡和脑萎缩,伴有淀粉样蛋白 β (Aβ) 斑块沉积和脑组织中过度磷酸化的 tau 神经原纤维缠结积聚,这些都会导致认知功能丧失。众所周知的 AD 致病基因(包括 APP、PSEN1 和 PSEN2)中的致病突变会损害多种途径,包括蛋白质加工、轴突运输和代谢稳态。
2021年8月31日,中国科学院昆明动物研究所姚永刚及罗荣灿共同通讯在Signal Transduction and Targeted Therapy(IF=18.19)在线发表题为“A novel missense variant in ACAA1 contributes to early-onset Alzheimer’s disease, impairs lysosomal function, and facilitates amyloid-β pathology and cognitive decline”的研究论文,该研究通过全基因组测序鉴定了汉族 AD 家族中乙酰辅酶 A 酰基转移酶 1 (ACAA1) 基因的错义变体 rs117916664 (c.896T>C, p.Asn299Ser [p.N299S]),并验证了其与独立队列中的早发家族性 AD。
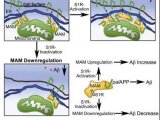
进一步的体外和体内证据表明,ACAA1 p.N299S 通过干扰其酶活性、损害溶酶体功能、加重 Aβ 病理和神经元丢失而导致 AD,最终导致小鼠模型的认知障碍。该研究结果揭示了过氧化物酶体介导的溶酶体功能障碍在 AD 发病机制中的基本作用。

阿尔茨海默病 (AD, MIM: 104300) 是一种毁灭性的神经退行性疾病,它以不断增加的速度折磨着大部分老年人群。突触功能障碍、神经元丢失、淀粉样斑块(主要成分β淀粉样蛋白 (Aβ) 肽)、tau 包裹体(主要成分过度磷酸化 tau)、脑萎缩和认知障碍是 AD 的病理和临床特征。越来越多的证据表明遗传和环境因素都会影响 AD,据估计其遗传力非常高(高达 0.79)。 参与 Aβ 产生的基因,如 APP(Aβ 前体蛋白)、PSEN1(早老素 -1) 和 PSEN2 (Presenilin-2),在三十多年前被确定为某些早发性家族性 AD (EOFAD) 病例的致病基因。然而,这些致病基因的大多数致病突变以常染色体显性方式出现,仅发生在低比例(<5%)的 AD 患者中。
已经表明 AD 是多基因的,具有许多因果和/或风险基因仍有待确定。基因中已报道了 40 多个经过充分确认的 AD 风险位点晚发型 AD 的全组关联分析 (GWAS),其中 APOE e4 等位基因是最有影响的因素。这些 GWAS 基因座中的大多数是位于非编码基因组区域的常见单核苷酸多态性,具有未知注释和小到中等的影响大小(优势比 [OR]<1.2)。事实上,只有 16% 的总 AD 表型变异归因于这些 GWAS 中。涉及多种途径的 50 多个位点/基因,包括内吞作用、胆固醇和脂质代谢、突触功能、树突和轴突运输、Aβ 和 tau 加工以及小胶质细胞和骨髓细胞功能,与 AD 相关,表明 AD 是一种全身性疾病。有多项关于 AD 发病过程中代谢功能障碍的报告。
在这项研究中,报道了一种与 EOFAD 相关的罕见功能丧失变异,rs117916664( p.Asn299Ser [p.N299S]),在过氧化物酶体 ACAA1(乙酰辅酶 A 酰基转移酶 1)中。ACAA1 p.N299S 导致 ACAA1 酶功能丧失并损害溶酶体功能,扰乱全局基因表达模式,影响细胞功能,并控制人类 AD 中的表达网络。ACAA1 p.N299S 在 AD 小鼠模型中的过表达促进了 Aβ 病理学并加剧了神经变性。该研究结果表明 ACAA1 p.N299S 显著加重 Aβ 病理和 Aβ 介导的神经变性,支持 ACAA1 功能丧失作为 AD 发展的危险因素的作用。
参考消息:
https://www.nature.com/articles/s41392-021-00748-4