T细胞介导的抗肿瘤免疫在宿主抵抗癌症的过程中起着核心作用。然而,癌细胞可以与肿瘤免疫微环境共同进化,并发展不同的策略来躲避T细胞的免疫破坏。由于各种T细胞抑制信号,例如CTLA-4和PD-1/ PD-L1,肿瘤浸润性T细胞常常表现出功能障碍,无法清除癌细胞。抗CTLA-4和抗PD-1/PD-L1抗体作为免疫检查点阻断(ICB)疗法,在部分癌症患者中产生了显着的临床益处和持久的应答,但仍有许多癌症患者无法从中获益。要充分发挥免疫治疗的潜力非常具有挑战性。
近期,德克萨斯大学MD Anderson癌症中心余棣华教授团队在Cancer Cell上发表文章,他们展开了一个“简单问题”的研究:常用药物会影响癌症患者对ICB疗法的应答吗?
在回顾性地分析了ICB治疗期间服用不同常用药物的患者后,他们惊喜地发现,组胺受体H1(HRH1)特异性抗组胺药(H1抗组胺药或第二代抗组胺药)可显着改善临床疗效。这就提出了一个有趣的问题:通常用于治疗过敏症状的抗组胺药是如何影响抗肿瘤免疫的?
利用癌症基因组图谱(The Cancer Genome Atlas,TCGA)和其他公开的癌症患者数据,研究小组发现,肿瘤中HRH1的高表达与T细胞功能障碍的标志物、对检查点抑制剂的不良反应和较差的生存结果相关。
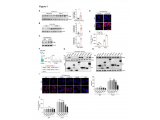
根据观察到的相关性,研究人员尝试阐明HRH1及其配体组胺对免疫应答的可能贡献。他们发现这两种蛋白质在肿瘤微环境中升高,但似乎不是来自同一来源。HRH1不存在于癌细胞中,但在肿瘤微环境中的某些类型肿瘤相关巨噬细胞(TAM),尤其M2型巨噬细胞中高度表达,有助于免疫抑制。相反,癌细胞似乎是患者样本中检测到的组胺水平升高的主要来源。
在临床前模型中,通过基因敲除或抗组胺治疗阻断巨噬细胞上的HRH1会降低TAM的免疫抑制活性,导致T细胞活化增加和肿瘤生长抑制。
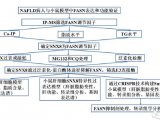
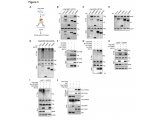
研究人员进一步探索了TAM中的HRH1如何影响T细胞活性。机制研究证明,阻断HRH1活性会使巨噬细胞上一种T细胞活化的V结构域免疫球蛋白抑制剂(VISTA)的表达减少。此外,阻断HRH1引起基因表达的广泛变化,导致TAM由抑制免疫的M2型逐渐转向能促进炎症的M1型。这些或许是抗组胺药物发挥作用的原因。
关于VISTA的发现值得关注,它已经是肿瘤学的热门靶点。去年,达特茅斯学院的一个研究小组曾报告,当T细胞表达高水平的VISTA时,会限制新T细胞的激活,这反过来会抑制对癌细胞的免疫应答。目前抗VISTA抗体正在进行实体瘤治疗的临床试验。
最后,研究小组还验证了靶向HRH1可以增强临床前模型中检查点阻断的应答,并检测了患者血浆组胺水平与其对免疫治疗反应的相关性,数据支持过敏反应或癌细胞释放的组胺减弱了免疫治疗的应答,而这可以通过抗组胺药来挽救。