一、操作资料
1、检验药品
(1)检验药品的名称 盐酸普鲁卡因。
(2)检验药品的来源 市场购买或送检样品。
(3)检验药品的规格、批号、包装及数量 根据药品包装确定,并记录有关情况。
2、质量标准
(1)检验依据 《中国药典》(2010版)二部793页“盐酸普鲁卡因”:本品为4-氨基苯甲酸-2-(二乙氨基)-乙酯盐酸盐。按干燥品计算,含C13H20N2O2 • HCl不得少于99.0%。
(2)含量测定 取本品约0.6g,精密称定,照永停滴定法[《中国药典》(2010版)附录Ⅶ A],在15~25℃,用亚硝酸钠滴定液(0.1mol/L)滴定。每1mL亚硝酸钠滴定液(0.1mol/L)相当于27.28mg的C13H20N2O2 • HCl。
(3)《中国药典》(2010版)附录Ⅶ A 永停滴定法用作重氮化法的终点指示时,调节R1使加于电极上的电压约为50mV。取供试品适量,精密称定,置烧杯中,除另有规定外,可加水40mL与盐酸溶液(1→2)15mL,而后置电磁搅拌器上,搅拌使溶解,再加溴化钾2g,插入铂铂电极后,将滴定管的尖端插入液面下约2/3处,用亚硝酸钠滴定液(0.1mol/L或0.05mol/L)迅速滴定,随滴随搅拌,至近终点时,将滴定管的尖端提出液面,用少量水淋洗尖端,洗液并入溶液中,继续缓缓滴定,至电流计指针突然偏转,并不再回复,即为滴定终点。
二、操作过程
1、仪器、试药准备及试液的配制
1)仪器的准备
永停滴定仪、电子或分析天平(感量0.1mg)、托盘天平、酸式滴定管(25mL)、烧杯、量筒(50mL)等。
2)试药的准备
盐酸、亚硝酸钠、溴化钾;盐酸普鲁卡因。
3)试液的配制
(1)盐酸溶液(1→2)取盐酸50mL,加水稀释至100mL,即得。
(2)亚硝酸钠滴定液(0.1mol/L)
①配制:取亚硝酸钠7.2g,加无水碳酸钠(Na2CO3)0.10g,加水适量使溶解成1000mL,摇匀。
②标定:取在120℃干燥至恒重的基准对氨基苯磺酸约0.5g,精密称定,加水30mL与浓氨试液3mL,溶解后,加盐酸(1→2)20mL,搅拌,在30℃以下用本液迅速滴定,滴定时将滴定管尖端插入液面下约2/3处,随滴随搅拌;至近终点时,将滴定管尖端提出液面,用少量水洗涤尖端,洗液并入溶液中,继续缓缓滴定,用永停法指示终点。每1mL亚硝酸钠滴定液(0.1mol/L)相当于17.32mg的对氨基苯磺酸。根据本液的消耗量与对氨基苯磺酸的取用量,算出本液浓度,即得。
如需用亚硝酸钠滴定液(0.05mol/L)时,可取亚硝酸钠滴定液(0.1mol/L)加水稀释制成。必要时标定浓度。
2、检验过程
1)检验步骤
(1)取本品0.54~0.66g,精密称定,加水40mL与盐酸溶液(1→2)15mL,然后置电磁搅拌器上,搅拌,再加溴化钾2g,插入铂-铂电极后,将滴定管尖端插到液面下2/3处,在15~25℃,用亚硝酸钠滴定液(0.1mol/L)迅速滴定,随滴随搅拌。至近终点时,将滴定管尖端提出液面,用少量水淋洗滴定管尖端,洗液并入溶液中,继续缓缓滴定,至电流计指针突然偏转,并不再回复,即为滴定终点。每1mL亚硝酸钠滴定液(0.1mol/L)相当于27.28mg的C13H20N2O2 • HCl。
(2)平行测定两份并计算本品含量,两次平行结果的相对偏差不得超过0.2%,取其算术平均值为测定结果。
2)讨论
本品具芳伯氨基结构,在盐酸存在下,能定量地与亚硝酸钠产生重氮化反应。依此,用已知浓度的亚硝酸钠滴定液滴定(用永停法指示终点),根据消耗的亚硝酸钠滴定液的浓度和毫升数,可计算出药物的含量。
三、检验结果
1、结果计算
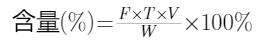
式中 T——滴定度,mg/mL
V——试验消耗亚硝酸钠滴定液的体积,mL
F——亚硝酸钠滴定液浓度校正因子,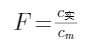
W——供试品的取样量,g
2、结果判定
(1)结果判定依据 按干燥品计算,含C13H20N2O2 • HCl不得少于99.0%。
(2)判定原则 如果含量计算结果在规定的范围内,则该项检查判为“符合规定”。
3、检验原始记录
4、检验报告书
