暴发性紫癜(purpura fulminans,PF)症候群又称坏疽性紫癜、坏死性紫癜、出血性紫癜,是临床上少见但病情凶险的血栓性出血性疾病。PF多见于儿童,临床特点:疾病发展迅速,紫癜对称分布,主要表现是全身皮肤大面积坏死,可累及深部肌肉组织,脏器受累时易出现多器官功能障碍综合征(multiple organ dysfunction syndrome,MODS)等严重并发症,病死率及致残率极高。广州市红十字会医院烧伤整形科近期收治了1例成人PF并发MODS致大面积皮肤深度坏死的病例,现报道如下。
患者男,18岁,因“发热伴进行性全身瘀斑并发大面积皮肤坏死”在外院治疗14d后转入广州市红十字会医院。患者发病前1天无明显诱因情况下出现发热,体温达40℃,无伴寒颤,无咳嗽咳痰,自行到药店购买氯芬黄敏片服用,症状未见缓解后到当地某医院就诊。
实验室检查:白细胞计数(WBC):2.0×109/L,血小板计数(PLT):156×109/L,肥达氏反应(-)。予以头孢他啶2.0g、利巴韦林0.5g静脉滴注及口服布洛芬缓释片后体温逐渐下降至正常,但回家后前额、面部出现少许散在、大小不一的紫黑色瘀斑,在用药后6h瘀斑范围逐渐扩大至颈部及胸部并融合成片,用药后12h瘀斑由颈部、胸部迅速扩散至全身。瘀斑压之不褪色,伴发热、神志模糊、烦躁不安,即收入广州市第八人民医院重症加强护理病房(intensive care unit,ICU),当时患者血压不能测出、脉搏细弱、指端冰冷、呼吸困难,出现休克表现。
当地医院拟诊:(1)感染性休克;(2)弥散性血管内凝血(disseminated intravascular coagulation,DIC);(3)流行性出血热。
实验室检查:WBC:32.26×109/L,中性粒细胞比例:91.6%。凝血功能:凝血酶原时间:27.6s,凝血酶时间:41s,纤维蛋白原:0.51ng/L。肾功能:肌酐:272μmol/L,血尿素氮(BUN):11.2mmol/L。白蛋白:20g/L,球蛋白:16g/L。谷丙转氨酶:61U/L,谷草转氨酶:152U/L。心肌酶:磷酸肌酸激酶同工酶(CK-MB):71.4ng/mL,肌酸激酶(CK):1208U/L,乳酸脱氢酶(LDH):401U/L。胸片:双肺叶弥漫性渗出。痰培养:产碱假单胞菌(+),流行性出血热抗体(-)。
患者收入ICU后迅速出现循环呼吸衰竭,并肾功能衰竭。血肌酐由入院时的272μmol/L迅速上升至入院后第4天的最高值:519μmol/L。氮质血症进行性加重,BUN由入院时的11.2mmol/L上升至入院后第5天的54.18mmol/L。患者在早期出现MODS,经气管插管接呼吸机辅助通气、纠正感染性及低血容量性休克、应用血管活性药物、输血小板、连续肾脏替代疗法(continuous renal replacement therapy,CRRT)等治疗后,患者全身瘀斑未进一步扩大,生命体征平稳,呼吸功能逐渐改善,循环趋于稳定,肾功能逐渐恢复。
入院第13天复查相关检查结果:WBC:11.5×109/L,中性粒细胞比例:90.7%,血红蛋白(HGB):66g/L,PLT:163×109/L。凝血功能:凝血酶原时间:14.9s,凝血酶时间:13.0s,纤维蛋白原:5.29ng/L。肾功能:肌酐:88.7μmol/L,BUN:14.77mmol/L。心肌酶:CK-MB:71.4ng/mL,CK:1208U/L,LDH:401U/L。各检查指标未见明显异常。患者对外界刺激能正常反应,有咳嗽反射、自主呼吸,拔除气管插管。但患者全身皮肤瘀斑逐渐变黑,形成黑色焦痂,皮肤大面积坏死感染。
创面培养结果提示:革兰氏阳性球菌。需进一步行手术切痂植皮治疗。请烧伤整形科会诊后考虑诊断:PF伴发大面积皮肤坏死,转烧伤整形科治疗。
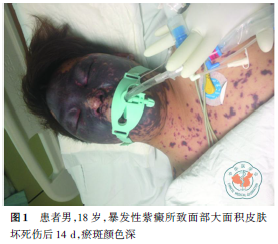
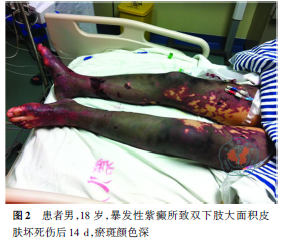
患者既往体健,否认“肝炎”、“结核”等传染病史,无不良嗜好,无毒物接触史,无家族遗传病史。入广州市红十字会医院时患者神志清楚,呼吸平稳。全身瘀斑未进一步扩大,但瘀斑颜色较前加深,面部、躯干前侧、双上肢、臀部、双下肢大片瘀斑(图1、2),面积约54%总体表面积(total body surface area,TBSA),创面基本结痂,呈紫红至黑色,少部分脱落,有渗液,臀部、双大腿内侧、双小腿大面积痂皮质地坚硬,伴腥臭味,双小腿环形焦痂,张力稍大,四肢末梢皮肤温暖,脚趾皮肤呈暗红色。
入院后予创面清创半暴露包扎,外涂磺胺嘧啶银粉保痂抗感染,静脉注射用亚胺培南西司他丁钠+奥硝唑氯化钠抗感染治疗。入院后第2天出现消化道应激性溃疡出血,解柏油样便3~4次/d,数次大便隐血试验(+~+++),予以抑酸剂奥美拉唑静脉推注及白眉蛇毒血凝酶静脉滴注止血,4d后隐血转阴性。入院第4天,血培养结果:奇异变形杆菌及摩根氏菌(+),根据药敏结果将抗生素调整为注射用亚胺培南西司他丁钠+万古霉素,加强抗感染治疗。
于入院第4天即伤后17d行“左臀部及双下肢切痂植皮术”,术中发现手术区创面均为全层皮肤坏死,皮下脂肪液化,双小腿胫骨前肌、趾长伸肌、腓骨长肌等深部肌肉坏死,双小腿创面较深,予以切开双小腿肌膜减压,清除部分坏死肌肉组织,以异种猪皮覆盖双小腿及左臀部较深的创面,双小腿填充碘纺纱加强引流,余创面自体皮移植。
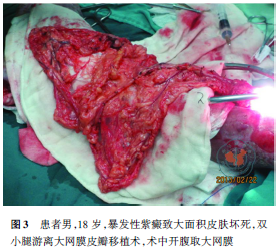
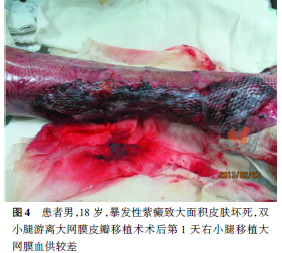
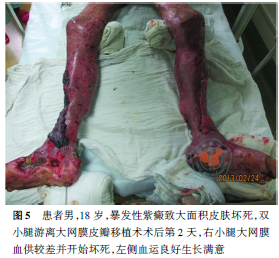
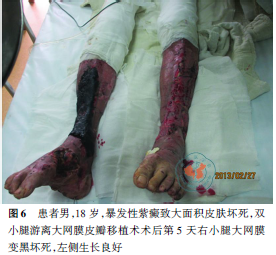
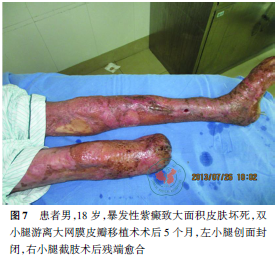
伤后23d行“双上肢、右臀部切痂植皮术”术中同样发现为全层皮肤坏死,切痂至深筋膜层,行自体网状皮移植,术后双上肢及臀部皮片生长满意,创面大部分愈合。伤后31d及38d均行“躯干及臀部清创植皮术”,术后躯干及双上肢大部分创面愈合。双小腿创面广泛累及深部肌肉组织,坏死面积较大:胫前肌缺损,双小腿胫骨外露,骨膜坏死,骨皮质发黑,胫前动脉缺如,胫后动脉及肌间动脉正常。鉴于患者双小腿创面特点,于伤后52d为其行开腹取胃大网膜做双小腿游离大网膜皮瓣移植。术前行超声检查大网膜面积及其血供情况,术中开腹取胃大网膜(图3),沿双小腿创面上方分离胫前动脉及静脉,将其与大网膜动静脉吻合,大网膜覆盖创面后在大网膜表面植大张打孔刃厚皮,并暴露手术区,持续予以0.9%氯化钠溶液静脉滴注保持湿润。术后患者左小腿大网膜皮瓣生长满意。右小腿大网膜血供较差逐渐坏死溶解(图4~6),其胫骨外露,右足踝关节结构破坏,关节腔形成窦道,由于创面暴露范围较大,难以有效的覆盖,骨结构大片变性坏死,并发创周软组织感染及骨髓炎,患者全身炎症反应明显,予以截除右小腿中下段,术前充分完善影像学检查,尽量降低截肢水平位,术后患者右小腿残端闭合良好,但患者并发左侧胫腓骨骨髓炎,持续高热,保守治疗效果欠佳,为避免病情进一步恶化,予以行“左胫骨开窗引流术”,予以持续冲洗及负压引流1个月余,患者病情控制,复查影像学检查见炎症明显控制,患者生命体征平稳,之后行清创植皮术封闭创面,左小腿保留克氏针固定踝关节予以出院。术后5个月左小腿创面基本封闭,踝关节外侧残留窦道,右小腿残端愈合良好(图7)。
讨论
PF并非是一种独立疾病的简称,而是临床上一系列相关症状的总称。主要包括大面积紫癜、皮肤坏死及肢体坏疽、脏器功能损害等。PF多发于儿童,在成人中较为少见,发病机制尚未明确。从分子生物学角度分析认为其发病与蛋白C、蛋白S缺陷有关,也有认为是感染性疾病时,高热、脓毒血症、细菌内外毒素等损伤血管内皮细胞,引起DIC;也有认为某些致敏因素如药物等使机体发生变态反应,血管内皮细胞损伤而致DIC,血管阻塞、渗出,最终皮肤发生大片瘀斑以致坏死并导致脏器出血及诱发MODS等。本病的内科治疗以抗感染、液体复苏、激素冲击及生命支持治疗为原则,外科治疗包括一期清创、筋膜切开、植皮、截肢,二期松解肌肉挛缩、治疗残肢溃疡,及时外科清创对降低病死率、致残率至关重要,PF可引起筋膜室综合征、并发横纹肌溶解,导致器官功能恶化。
本病例中患者出现PF的原因可能与患者前期呼吸道病毒感染有关,也可能与患者服用非甾体抗炎药诱发的变态反应有关。患者病情发展迅速,早期表现类似过敏性紫癜,但皮损范围迅速扩大并逐渐融合,部分发展为深部软组织的坏死。全身皮肤坏死面积达54%TBSA,皮损程度大部分为类似Ⅲ度烧伤,双小腿甚至达Ⅳ度。患者早期在广州市第八人民医院治疗期间,出现DIC,大量消耗血小板及凝血因子,大面积小血管的闭塞加重了组织的缺血坏死,经大量输注血小板纠正凝血功能障碍,大剂量激素冲击疗法使逐渐纠正。
本例患者病情进展迅速,很快发展为MODS,早期诊断较为困难,只能予以呼吸循环支持等对症治疗。患者早期发生DIC使双小腿深部毛细血管堵塞,而导致深部肌肉缺血坏死,加之局部渗出物积于组织间隙,进而并发双小腿筋膜室综合征。但由于早期患者一般情况较差,难以耐受手术打击,所以以优先抢救生命、恢复脏器功能等治疗为主,但同时错过了创面处理的最佳时机,导致创面坏死感染加重。患者一般情况稳定后,大面积坏死感染创面的处理成为主要内容,这也是本病例的主要特点。
术中发现它不同于普通的出血性紫癜的皮损表现,其皮损特点为大面积暗红色的皮损融合成片而不是以散在的出血点分布,并且组织坏死不局限于皮肤及皮下,而是存在大片肌肉组织的出血、缺血及继发性坏死。这也就加大了后期的创面处理难度,常规的削痂、皮片植皮手术难以取得理想的治疗效果。在后期的切削痂植皮手术过程中,笔者根据患者皮肤坏死的程度及结合病程的不同阶段制定不同的手术方案。早期的2次手术旨在尽快清除坏死组织,封闭创面,改善全身情况,降低感染风险。基底较好的创面植自体皮片,基底较差的予以异种或异体皮覆盖,为下次手术做好创面床的准备。
中期开始视创面情况,选择基底较好的创面分次行自体皮移植。患者双小腿坏死面积较大且累及深部肌肉,早期为控制感染也将截肢作为备选手术方案。双小腿早期因DIC致肌肉深部毛细血管堵塞导致组织缺血坏死,并由于局部组织水肿导致其筋膜室压力增大,这在一定程度上加重组织坏死。双小腿创面普通皮片移植难以存活,又由于肌肉组织坏死面积较大,取临近带蒂皮瓣方案也不可行,患者因为全身创面面积较大,其他部位也无完整的游离皮瓣可取,充分权衡后为患者做了取胃大网膜做游离皮瓣移植于双小腿,即保留大网膜动静脉移植与双小腿后运用血管外科微创技术重建大网膜血供,并在大网膜表面做自体网状皮片移植。
目前自体大网膜移植技术被广泛应用于各种难愈性创面的修复,其特点主要有:(1)大网膜切除后能够快速有效建立侧枝循环;(2)在腹腔外血管再生能力强;(3)本身血供丰富。
本例患者术后左小腿大网膜皮瓣成活,右小腿未能成活,逐渐坏死溶解。目前分析出现此结果的原因,除了手术本身的技术原因外还存在另外一个不可忽视的因素:本例患者采用的是开放式的开腹取大网膜的术式,大网膜取下后处于一个离体的状态,离体后有数小时的双小腿创面床准备的等待时间,手术过程中因条件有限也是先行左侧小腿大网膜移植及血管吻合,从而进一步导致移植于右侧小腿的大网膜离体时间增长,也就是说大网膜的离体时间过长有可能影响手术效果,这样的话就可以猜想如果在大网膜取下后两侧小腿立即同时做血管吻合的情况下两侧的手术效果能否尽可能一致,或者说可以在取大网膜的时候不选择开腹这种创伤较大的手术方案,选择在腹腔镜微创技术下分次取大网膜,以保障大网膜取下后能够在第一时间内重新建立血供。
患者在病程后期出现过1周左右的与进食相关的剧烈呕吐(患者在休息状态下未见消化道的任何不适症状,进食后数分钟内可出现剧烈呕吐),症状持续1周余(期间停用所有静脉用药以排除药物性呕吐),之后患者症状逐渐自行缓解。目前不排除是因大网膜切除后所致的胃肠功能紊乱而导致的。患者后期出现双小腿骨髓炎,以持续发热、高血象为表现,MRI提示:右小腿中下段骨髓炎。
右踝关节结构完全破坏,骨结构坏死严重,神经血管缺失,保守治疗效果欠佳,之后予以截除右小腿中下段。左小腿骨髓炎开窗引流,持续负压吸引1个月余,并置入克氏针固定踝关节。左小腿骨髓炎予以持续冲洗及负压引流1个月余,患者骨髓炎症状得到控制,最后行植皮术封闭创面。
虽然PF起病突然,发展迅速,累积器官广泛,早期处理起来相对比较被动,但是起病初期的早期认识、早期诊断、早期治疗至关重要,可以阻断一系列并发症的发生,有效降低致残率和病死率。在大面积PF的后期治疗中,大面积坏死皮肤肌肉组织的处理尤为重要,如何降低机体的感染风险,如何提高皮片或皮瓣的成活率等问题决定着病情的最终转归。