近日,湖南大学谭蔚泓院士团队与浙江大学医学院附属第一医院黄河教授团队开发了一种基于核酸适体的质谱流式技术,用于单细胞的细胞表面蛋白分析,旨在为疾病的精准分子分型提供一个新的平台技术。该方法不仅能够实现培养细胞的分子分型和分类,还能结合机器学习,实现临床样本亚型的分类。该方法极大地扩展了核酸适体的应用领域,并为疾病的分类和诊断提供了新方法。
背景介绍:
高度异质性是恶性肿瘤的重要特征,同一疾病的不同亚型可能对临床治疗有着完全不同的反应。因此,疾病的精准分子分型对其诊疗研究具有重要意义。虽然基因组测序和转录组测序已经成为最常用的分类策略,但它们无法提供蛋白质的表型和功能数据。单细胞水平的膜蛋白分析将为疾病分型提供重要信息。流式细胞术提供了高通量的单细胞测量技术。然而,由于荧光光谱重叠问题,限制了荧光流式细胞术的多元分析能力。质谱流式作为一种先进的替代方法,具有信号重叠小和细胞背景噪声低等优点,已展现出在一次实验中同步测量超过40个细胞参数的能力。尽管质谱流式技术在多路复用单细胞分析中的巨大潜力,但其在肿瘤分类中的潜力受到识别探针种类不足的限制。
核酸适体作为一种新型的识别配体,具有特异性高、合成简单、免疫原性低、修饰方便等优势。此外,以完整的活细胞为筛选对象,可以通过Cell-SELEX(指数富集配体进化技术)获得大量能够特异性识别细胞膜蛋白标志物的核酸适体。
本文亮点:
基于以上研究背景,湖南大学谭蔚泓院士团队联合浙江大学医学院附属第一医院黄河教授团队设计、合成了一种由二乙烯三胺五乙酸(DTPA)基元组成的聚合物,用于螯合多个金属离子。然后,选择了一系列识别不同细胞表面生物标志物的核酸适体,每个适体分别与螯合了不同金属离子的聚合物偶联(Apt-MICP)。最后,评估了基于Apt-MICP的细胞表面蛋白分析在培养细胞和临床样本中用于血液恶性肿瘤(HM)精确分类的潜力(图1)。
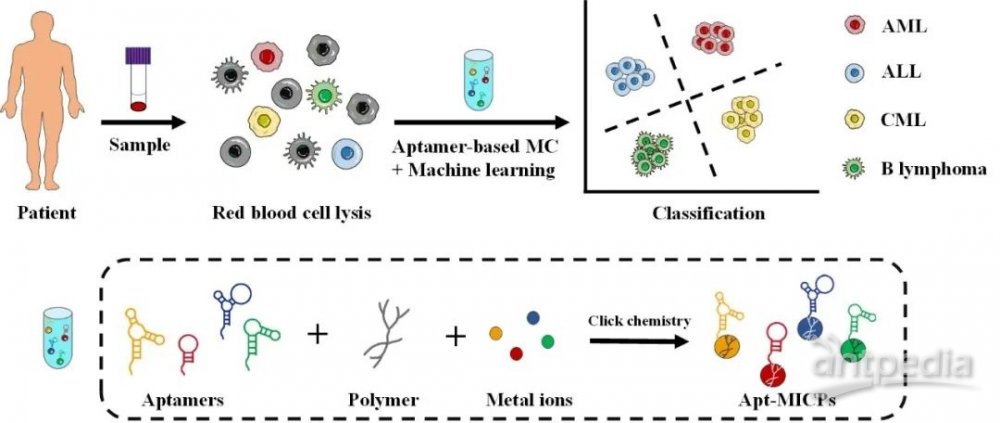
图1. 基于核酸适体的质谱流式分析技术用于血液恶性肿瘤的分子分型
作者首先对聚合物进行了设计与合成,并通过点击化学将其与核酸适体相连(图2a)。利用琼脂糖凝胶电泳和高效液相色谱对产物进行表征,证明了sgc8c-MICP的成功合成(图2b,c)。同时,在核酸适体上修饰上荧光基团,利用荧光流式验证了sgc8c-MICP仍然能够靶向CEM细胞,而不会结合Ramos细胞(图2d,e)。
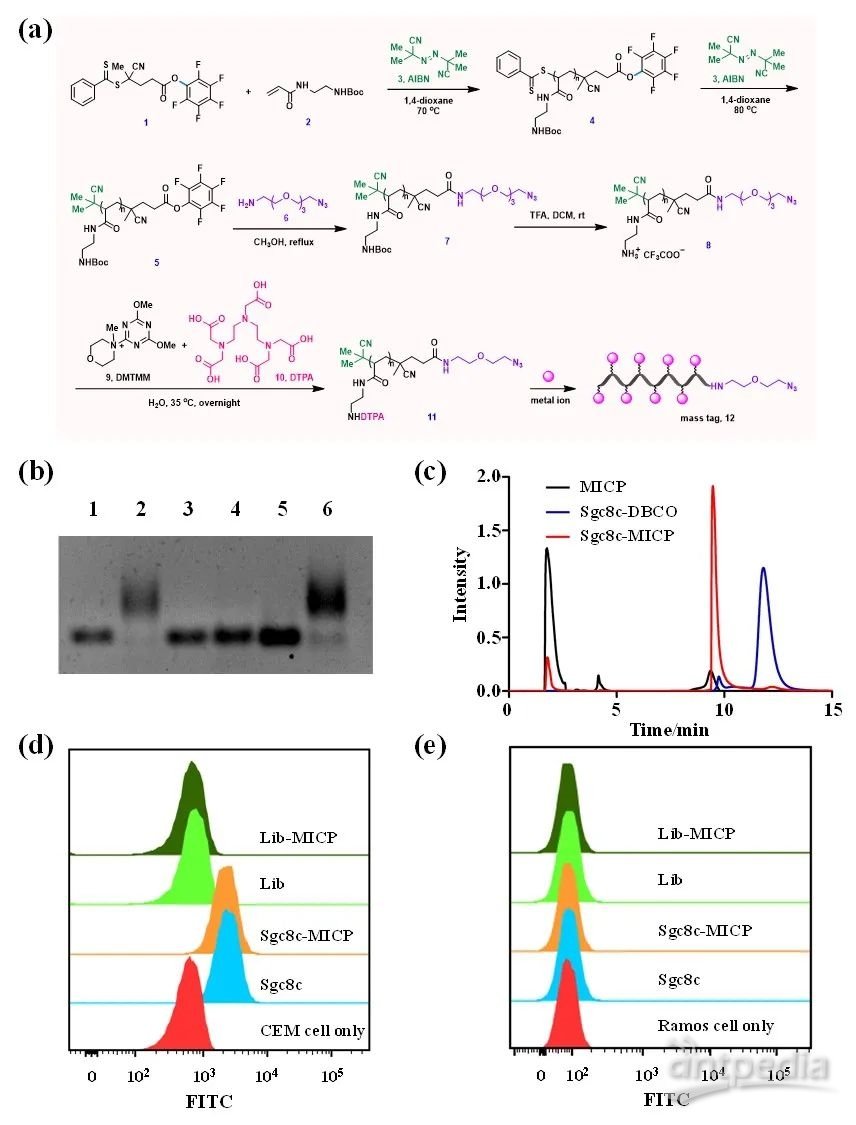
图2. sgc8c-MICP的合成与表征
在证明了该策略的有效性之后,作者挑选了15条相关的核酸适体,将其连接上螯合了不同金属离子的聚合物,得到15条Apt-MICP。将15条核酸适体联用,依次对8种血液恶性肿瘤细胞系进行结合,通过质谱流式进行分析。将得到的结果进行归一化,并用热图进行展示(图3a)。利用viSNE降维分析方法对分型结果进行分析,实现8种细胞的区分(图3b)。结合无监督的主成分分析方法,实现血液恶性肿瘤细胞系更精确的区分(图3c)。
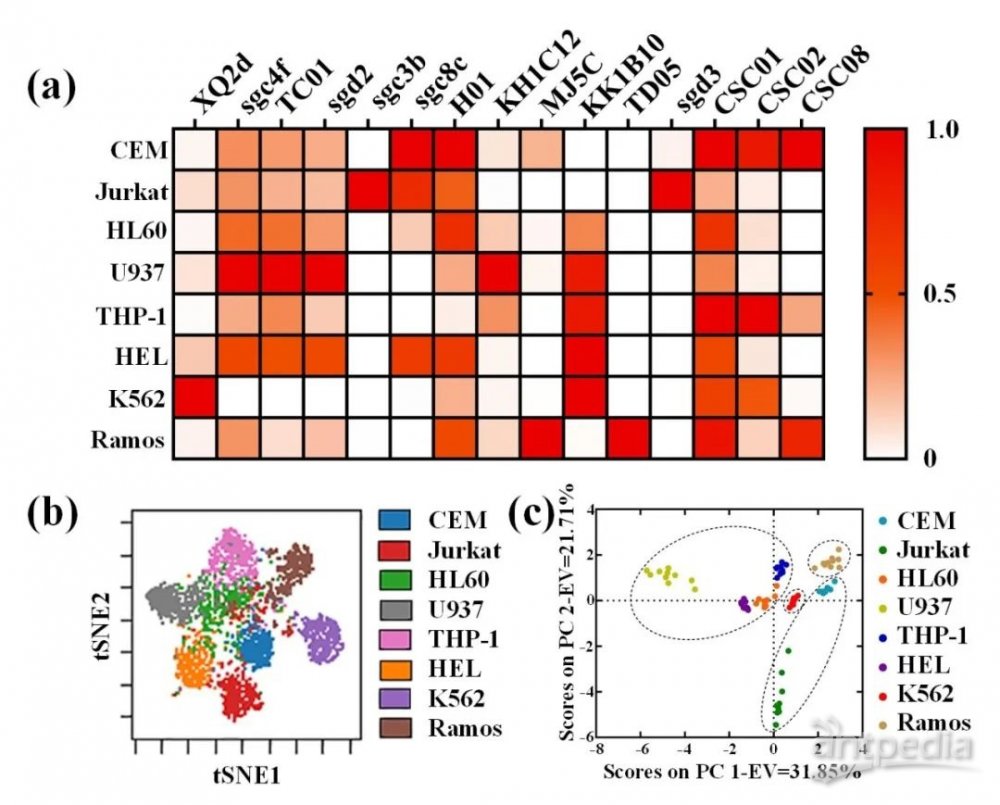
图3. 血液恶性肿瘤细胞系的细胞表面特征分析及分类
利用上述合成的15条Apt-MICP,结合五种相关的抗体,实现了31例血液恶性肿瘤临床样本(包括AML、ALL、B淋巴瘤以及CML四种亚型)的分子分型(图4a)。由于临床样本的异质性高,作者利用机器学习的方法进行PLS-DA建模,并成功将四种亚型的样本区分开来(图4b),总体准确率达到了100%(图4c)。
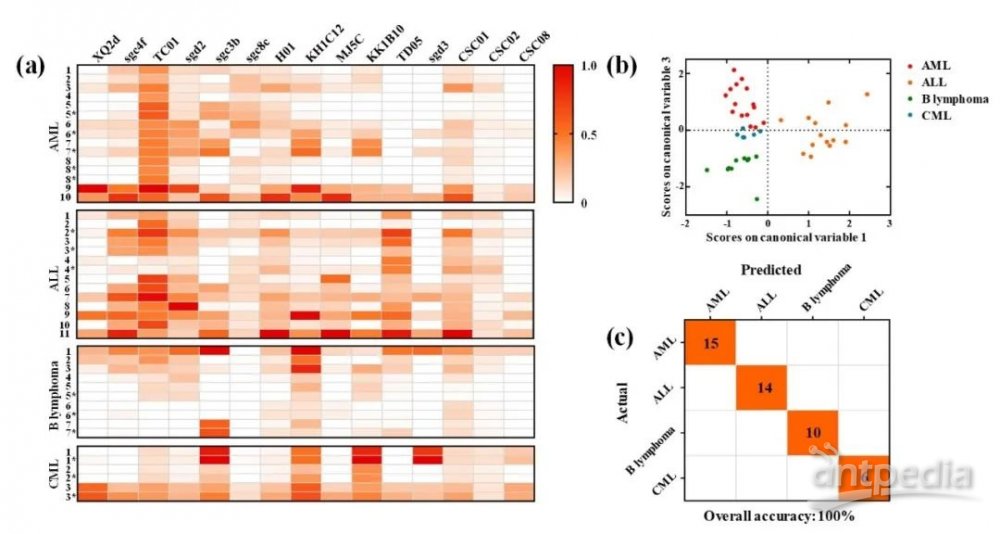
图4. 临床样本训练集的分子分型和分类
为了进一步验证该模型的有效性,作者又收集了15例临床样本,得到了分子图谱(图5a)。将分型结果输入到模型当中,实现对每个样本亚型的判定,总体准确率达到了80%(图5b)。
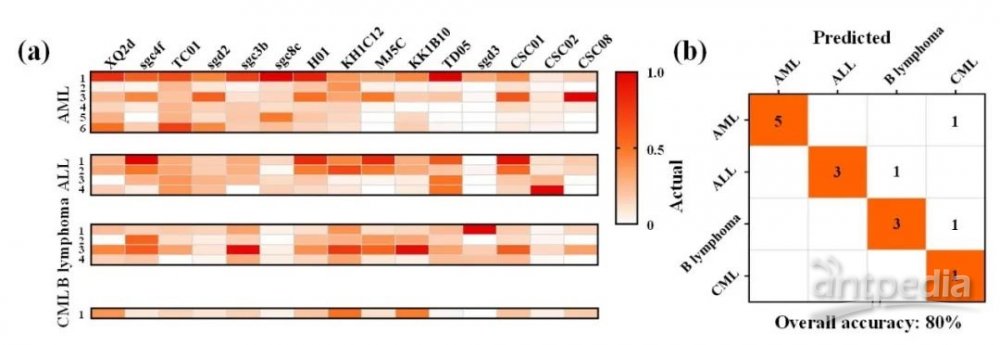
图5. 临床样本测试集的分子分型和分类
总结与展望:
综上所述,该研究开发了一个基于核酸适体的质谱流式检测平台,用于精确的癌症分类。作者合成了一系列核酸适体-金属标签探针,并证明了它们在细胞类型特异性结合以及质谱流式检测方面的良好性能。通过用15个核酸适体探针分析细胞表面特征,可以很好地区分8个HM细胞系。此外,通过结合机器学习(PLS-DA),对HM临床样本的四个亚型构建了一个高质量的分类模型,在训练集中分类总准确率为100%,在测试集中分类总准确率为80%。基于这些结果,基于核酸适体的质谱流式平台有望在其他疾病的分类和诊断中得到广泛应用。该工作以Research Article的形式发表在CCS Chemistry。
文章详情:
Aptamer-based cell-surface profiling with single-cell resolution enables precise cancer characterization
Liujun Xu†, Yawei Feng†, Tong Wang, Shenhuan Li, Kangli Xu, Yue Sun, Yi Luo, Yishan Ye, Yan Miao, Yun Dong, Zhenzhen Guo, Qing Zhang, Benshang Li, He Huang*, Xue-Qiang Wang, Liping Qiu and Weihong Tan*
Cite this by DOI: 10.31635/ccschem.023.202302825
文章链接:https://doi.org/10.31635/ccschem.023.202302825