
无菌检查法系用于检查药典要求无菌的药品、医疗器具、原料、辅料、及其他品种是否无菌的一种方法。若供试品符合无菌检查法的规定,仅表明了供试品在该检验条件下未发现微生物污染。
1
无菌检查法的概念与基本要求
药品无菌标准是国家对药品生产的卫生法规。它对药品生产企业、药物研发机构的文明生产、现代化管理及保证药品的卫生质量,保证人民的健康起着重要的促进作用。无菌检查法目的在于保证无菌检查的药品安全。因此凡用于确定要求无菌的药品、原料、辅料及要求无菌的其他品种在出厂前均应进行无菌检查,它是保证药物制剂质量的重要措施。[1]
《中国药典》从1953年版开始就收载该项检验内容,并且方法学不断完善。它在保证人民用药安全方面有着十分重要的意义。据统计,《中国药典》(2005年版)共有238个单列品种规定要进行无菌检查。所以无菌检查是药品卫生学检验最早的项目和各国药典最早收载的检验内容,上世纪初就列入要求项目。[2]
2
国内外相关技术方法对比
国际上《美国药典》、《欧洲药典》无菌检查法已通过ICH完成协调,《中国药典》2020年版无菌检查法与他国药典的各项主要参数也基本一致,尚存的主要差异是在整合过程中基本求同存异的考虑,具体差异点见表1。鉴于欧美药典与中国药典的差异,产品在进行中美双报时需要分别开展方法适用性试验及检测。[3]
表1 无菌检查法-药典传统方法差距分析
3
现阶段都有哪些检测方法
目前对于无菌检查的实验方法包括:
01 直接接种法
即取规定量供试品接种硫乙醇酸盐流体培养基(FTM)和胰酪大豆胨液体培养基(TSB)中。生物制品无菌检查时硫乙醇酸盐流体培养基(FTM)和胰酪大豆胨液体培养基(TSB)接种的瓶或支数为2:1。除另有规定外,每个容器中培养基的用量应符合接种供试品体积不得大于培养基体积的10%,供试品检查时,培养基的用量和高度同方法适用性试验。[1]

02 薄膜过滤法
无菌检查使用薄膜过滤法时,应保证滤膜在过滤前后的完整性。水溶性供试液过滤前应先将少量的冲洗液过滤,以润湿滤膜。油类供试品,其滤膜和过滤器在使用前应充分干燥。为发挥滤膜的最大过滤效率,应注意保持供试品溶液及冲洗液覆盖整个滤膜表面。冲洗过程中可适度振摇,以避免滤器侧壁的样品残留。其他步骤应与方法适用性检查相同。[1]
03 无菌快速检验方法
无菌检查快速检测法包含两种,一种为基于生长代谢的检测方法,该检测方法中又分为ATP 生物发光检测技术、CO2检测技术、电阻抗检测技术;
另一种是基于细胞的检测方法,该检测方法中分为荧光染色技术和流式细胞技术。具体如下:[3]
基于生长代谢的检测方法
ATP 生物发光检测技术
样品经过薄膜过率器过滤后,在营养丰富的平板上培养。培养过程中微生物细胞产生ATP,荧光素酶催化ATP依赖的荧光素氧化脱羧反应发光。当所有反应成分都过量时,产生的光信号与ATP的释放量成比例。因此ATP生物发光能有效地指示微生物是否存活。该技术可以将无菌检查的培养时间缩短至5天。
CO2检测技术
大多数微生物在生长过代谢过程中会产生CO2,通过在培养体系中加入能与CO2结合发光或产生颜色变化的物质,检测培养物中荧光强度或检测颜色变化,可以在较短的时间内获取微生物的生长繁殖信息,从而判断培养体系中是否存在活的微生物。
电阻抗检测技术
微生物的生长将带弱电的大分子 (如多聚糖)代谢为带强电的代谢小分子产物(如有机酸等)。随着微生物的不断繁殖,带电的产物不断富集,直至最终到达检测器的检查阈值。
基于细胞的检测方法
荧光染色技术
采用薄膜过滤法将微生物截留于膜表面,用活体底物标记捕获的细菌,在具有代谢活性的微生物细胞质中,非荧光的底物被水解酯酶切断,释放出荧光发光物质。仅有细胞壁完整的活体微生物有能力在检测中保留标记物。通过激光检测器自动扫描检测具有荧光标记的细胞及其数量。该方法无需细胞繁殖,灵敏度达1个细胞水平,2~3小时即可得到检测结果。
流式细胞计数
与荧光染色技术相似,微生物在溶液中被荧光的标记物标记并产生荧光底物。体系中的颗粒物依次通过流式细胞仪的激光检测器,并捕获荧光信号。该方法适合于检测液体中的微生物。
4
各种检测方法的优劣势分析
4.1 传统法-直接接种法
该方法优点在于操作简便、成本低、技术要求低;缺点则是接种量固定、检出率低、操作污染风险大。如果待检样品数量有限(如细胞库、病毒库)或不易溶解,过于粘稠,不易过滤,推荐采用直接接种法,检测流程见下图。

👆图1中国药典 [1]
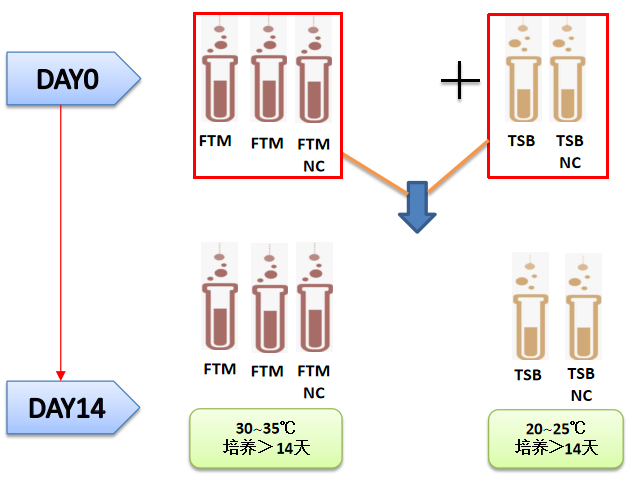
👆图2美国药典[3]
4.2 传统法-薄膜过滤法
该方法优点在于检出率高、检测量大、操作污染风险小;缺点则是成本较高、程序繁琐、技术要求高。如果想扩大样品的单次检验量,提高检出率,推荐采用薄膜过滤法,检测流程见下图。

👆图3中国药典 [1]

👆图4美国药典[3]
4.3 无菌快速检验方法[2]
01 ATP生物发光
主要用于限度实验和环境监测,基质中ATP会干扰计数结果,造成灵敏度不够高。
02 电阻抗技术
食品行业应用较多,培养基基质干扰严重,污染菌数较少时,结果不稳定。二氧化碳比色-灵敏度较高,阳性菌最低检出度<10CFU/ml。早在2004年,美国Genzyme就获得了FDA的批准,在无菌测试中应用该方法。
03 荧光染色技术
具有较高的准确性和重复性较好,然而需要较高辨识度的荧光染料,操作程序复杂,成本较高。世界范围内,该方法更多应用在食品、饮品、化妆品、环境及其医疗过程等。
04 流式细胞技术
可以快速检测的方法,但硬件投入较大,对于基质的要求相对较高,高背景干扰导致LOD无法与药典无菌检查法相一致。
05 CO2检测技术

5
无菌检查的方法适用性试验[2-9]
我们知道,在进行供试品的无菌检查前,必须要开展供试品的无菌检查方法适用性试验。那么,究竟为何要进行供试品的方法适用性试验呢?答案是为了保证检验的准确与真实,保证检验的严谨性。
国外药典很早就有了无菌检查方法学的验证试验,《中国药典》(2005年版)开始收载方法学的验证,并规定,当建立药品的无菌检查法时,应进行方法验证试验,以确认所采用的方法适合于该药品的无菌检查。若检验程序或产品发生变化可能影响检验结果时,应重新进行方法适用性试验。
由于传统无菌检查方法包括直接接种法和薄膜过滤法,都是药典里规定的法定方法,因此日常中使用此方法进行供试品的适用性试验及样品检测遵照药典开展即可。然而,无菌快检法并不在法规规定的方法中。无菌快检法是《中国药典》2020版 9201药品微生物检验替代方法验证指导原则中允许的方法。
那么,满足哪些条件才能使用快速方法呢?如果我们想要采用无菌快检法,首先需要进行微生物检验替代方法验证。验证的指标包括专属性、检测限、耐用性和重现性。与药典传统方法进行比对,如果验证结果优于或一致,则可以用无菌快检法代替传统培养法。如果验证结果劣于或低于传统方法,则不可代替传统法。与传统方法一致,每个样品检查前均需进行方法适用性试验。
6
微谱无菌检查解决方案
对于无菌检查,微谱可以根据不同客户需求,不同样品种类,提供多元的定制化无菌检查方案。
一对一定制化服务
针对供试品数量有限的细胞库和病毒库,及不易溶解或质地粘稠的原辅料,我们可以制定与产品一对一的直接接种法方法适用性试验及无菌检查法。
能力覆盖多元方法
根据客户需求想扩大单次检验量,提高检出率的供试品,我们可以提供薄膜过滤法方法适用性试验及无菌检查法。
专业的无菌快速检验
针对供试品的效期短、价格昂贵、数量有限、不易溶解、粘稠或者想要提高检出率的需求,我们可以根据不同产品提供无菌快速检验方法,包括无菌检查替代验证方案、替代方法验证、方法适用性试验及检测服务。
满足中美欧药典需求
我们提供的服务符合《中国药典》、《欧洲药典》、《美国药典》等国内外法规要求。
精准 有效 快速 合规
依据客户样品类型,提供更加精准、有效、快速、合规的无菌检查方法适用性试验方案和技术服务。
【参考文献】
[1]《中国药典》2020版 三部和四部1101无菌检查法
[2]《中国药典》(2005年版)三部和四部1101无菌检查法
[3] 中国药典分析检测技术指南—国家药典委员会编著2017.07出版(1)
[4]《中国药典》2020版 9201药品微生物检验替代方法验证指导原则
[5]《美国药典》1223 VALIDATION OF ALTERNATIVE MICROBIOLOGICAL METHODS微生物替代方法的验证
[6]《欧洲药典》5.1.6 Alternative methods for control of microbiological quality控制微生物质量的替代方法
[7]《PDA》TR33 Evaluation, Validation and Implementation of New Microbiological Testing Methods可选择的和快速的微生物检测方法的评价验证与执行
[8]《中国药典》通则征求意见稿 胞类制品微生物检查法 2021.10.26—国家药典委
[9]《中国药典》(2005年版)三部和四部1101无菌检查法