CDE动态
6月11日,国家药品监督管理局药品审评中心发布了关于公开征求《化学仿制药参比制剂目录(第八十三批)》(征求意见稿)意见的通知,现全文转载如下。
以下为通告全文:
关于公开征求《化学仿制药参比制剂目录(第八十三批)》(征求意见稿)
意见的通知
发布日期:20240603
▲ 图源 | CDE官网
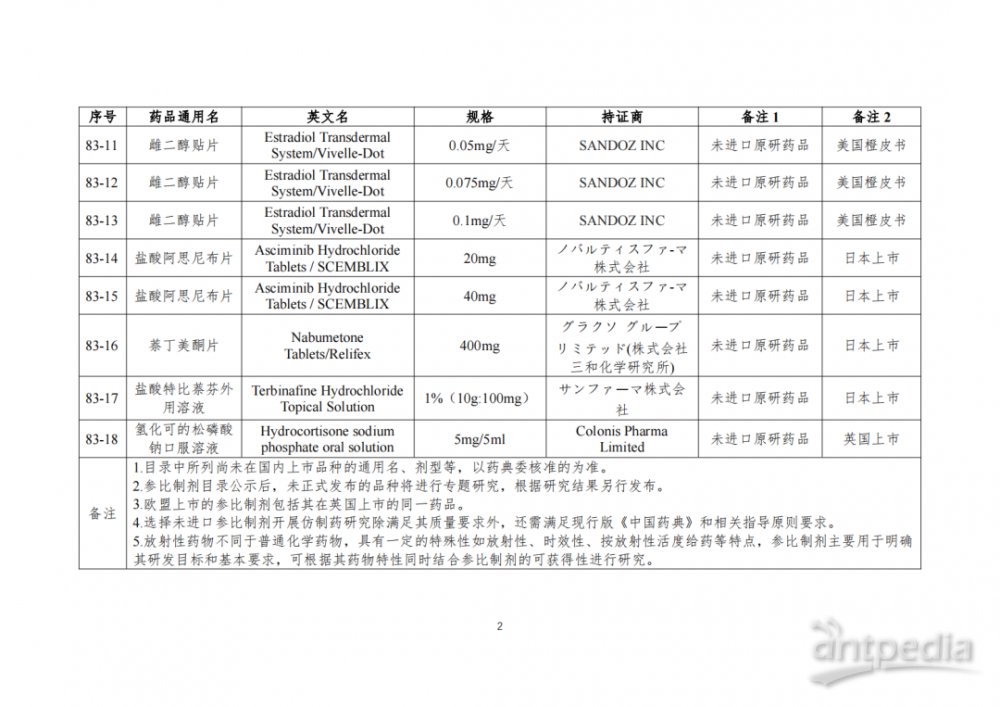
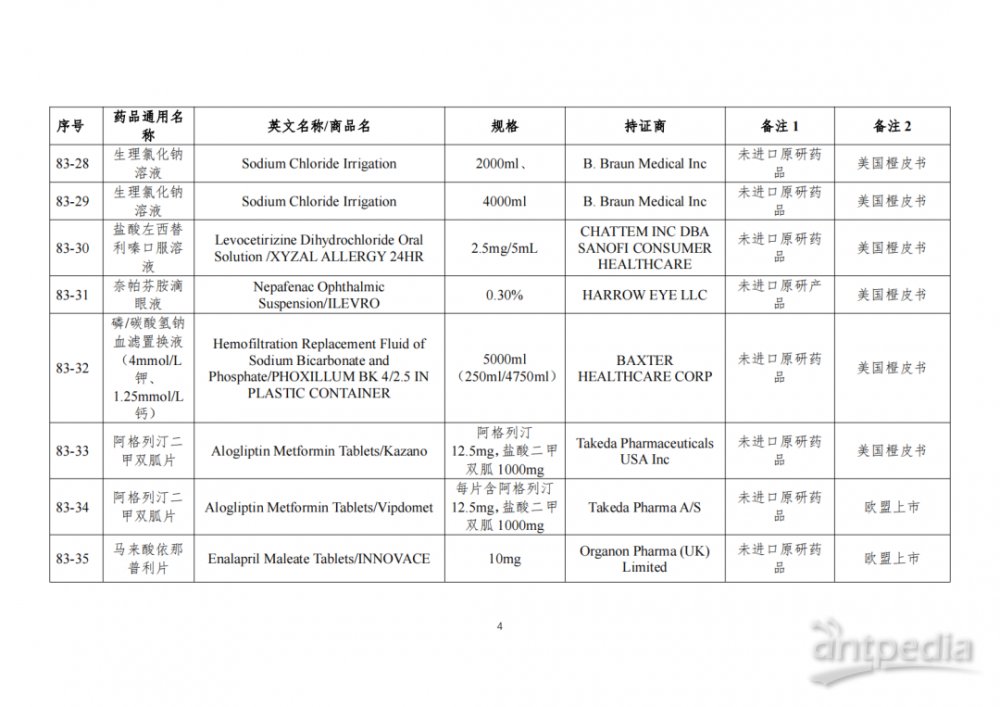
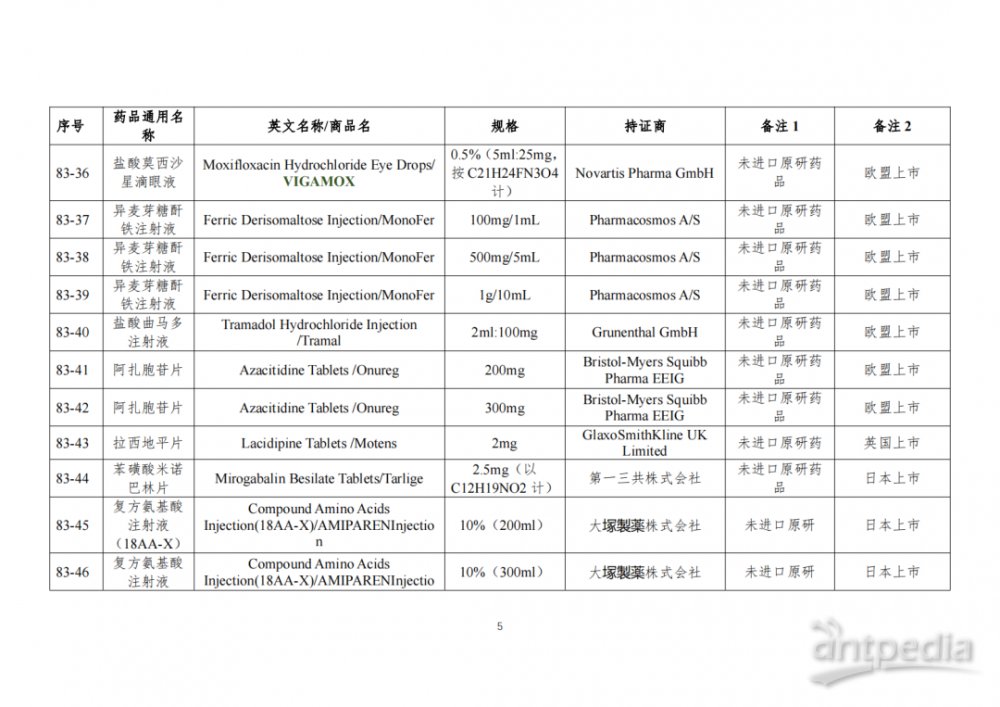
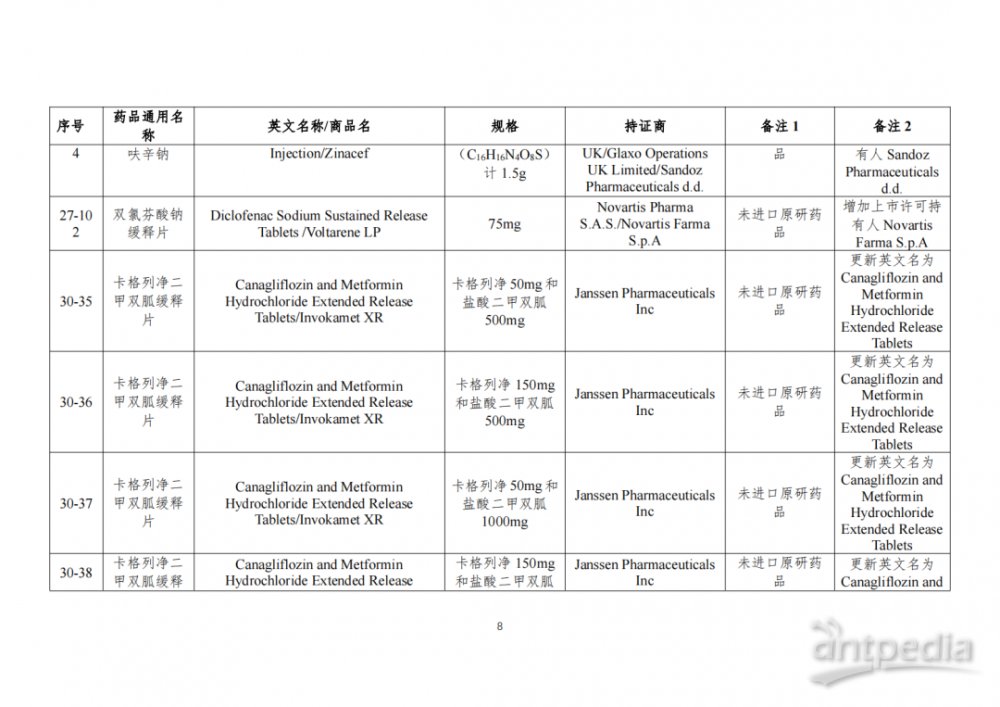
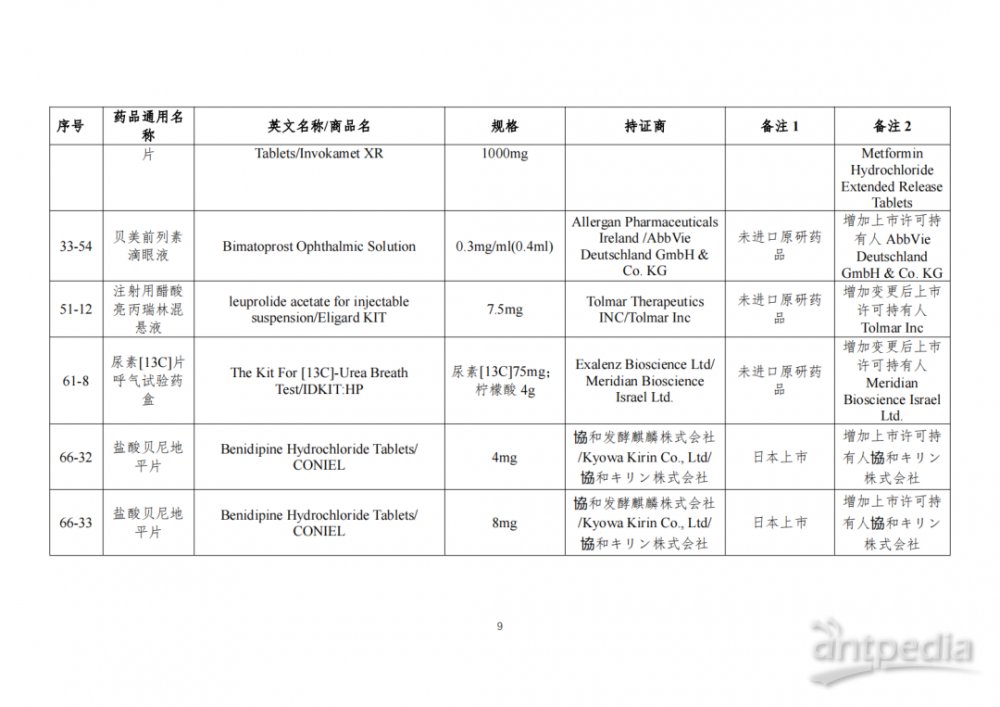
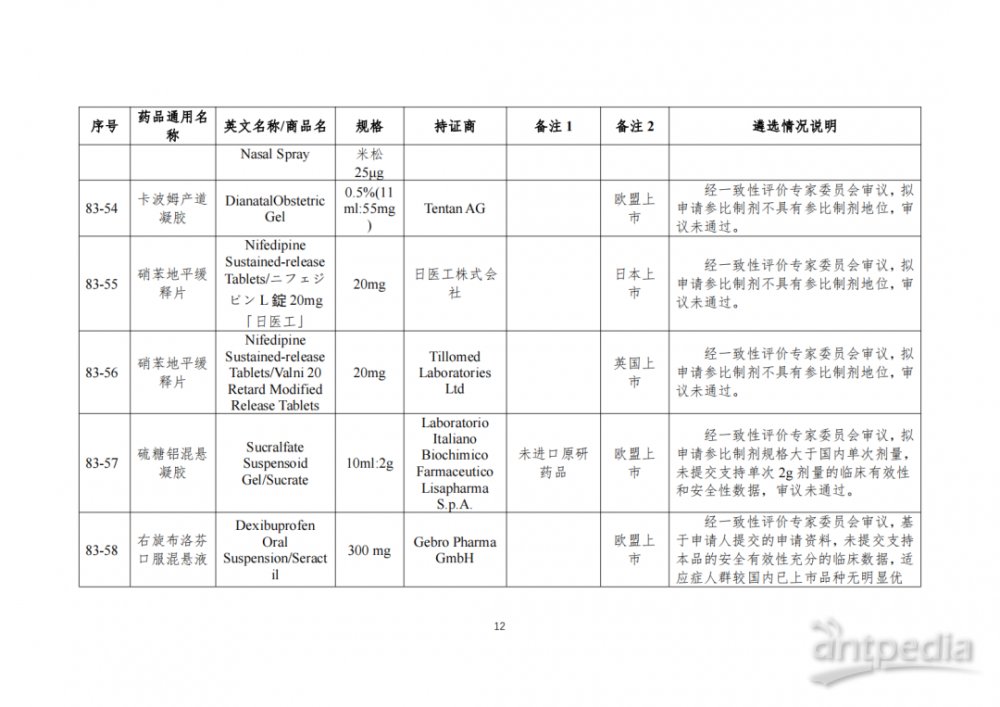
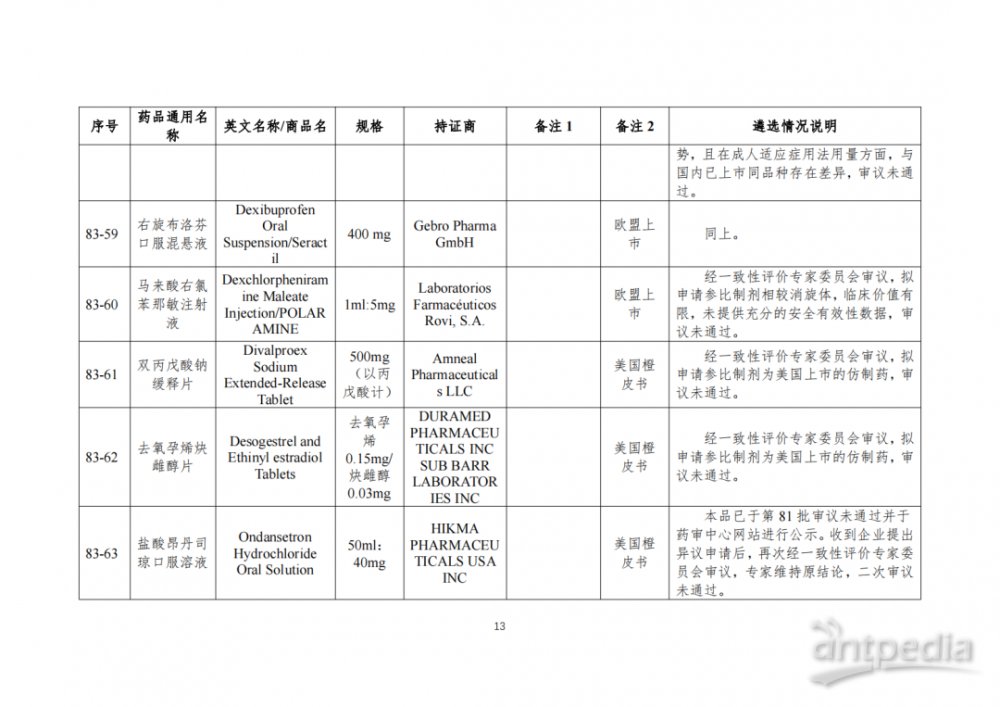
根据国家局2019年3月28日发布的《关于发布化学仿制药参比制剂遴选与确定程序的公告》(2019年第25号),我中心组织遴选了第八十三批参比制剂(见附件),现予以公示征求意见。
公示期间,请通过参比制剂遴选申请平台下“参比制剂存疑品种申请”模块向药审中心进行反馈,为更好服务申请人,反馈意见请提供充分依据和论证材料,反馈材料应加盖单位公章,并提供真实姓名和联系方式。
公示期限:2024年06月11日~2024年06月24日(10个工作日)。
国家药品监督管理局药品审评中心
2024年6月11日






THE END
关于我们
微研优仿医药科技(江苏)有限公司是微谱在药物研发板块的全资子公司。前身为江苏优仿医药科技有限公司,成立于2018年,坐落于苏州工业园区。作为值得信赖的药物研发伙伴,公司持续深耕药物研发与创新市场,拥有近5000㎡研发实验室和百余名专业技术人员,以及完善的研发设备,为药企客户提供药品研发一体化服务,是微谱布局CRO全产业链的重要一环。

更多详情 · 请联系
电话:021-3178-5055
邮箱:yiyao-marketing@weipugroup.com
往期推荐:
人物专访丨宜明生物王志民:加速全球布局迎接出海挑战
案例分享 | 化妆品注册备案驳回案例分享(三)
公司新闻|微谱荣获“2023年度TIC优秀第三方检测机构评选坚如磐石奖”!

我知道你在看哟