背景是一种非原子吸收现象,多数人认为主要来自:
(1)光散射(微固体颗粒引起) 火焰中的气溶胶固体微粒存在,会使入射光发生散射,产生高于真实值的假吸收,使结果偏高。
(2)分子吸收 分子吸收是指在原子化过程中生成的气体分子、氧化物及盐类分子对辐第三射吸收而引起的干扰,包括火焰的成分,如OH、CH、NH、CO等分子基因吸收光源辐射;低温火焰中常存在碱金属和碱土金属的卤化物的吸收,如NaCl、KCl、CaCl2等双原子分子在波长小于300mm的紫外区有吸收带;在高温火焰中碱土金属的氧化物或氢氧化物也会吸收辐射,如Ca(OH)2的吸收带干扰钡553.56nm的吸收峰。
图1示出了钠的卤化物分子的吸收谱带。光散射是指在原子化过程中产生的固体微粒对光产生散射,使被散射的光偏离光路不为检测器所检测,导致吸光度值偏高。
背景吸收除了波长特征之外,还有时间、空间分布特征。分子吸收通常先于原子吸收信号之前产生,当有快速响应电路和记录装置时,可以从时间上分辨分子吸收和原子吸收信号。样品蒸气在石墨炉内分布的不均匀性,导致了背景吸收空间分布的不均匀性。
提高温度使单位时间内蒸发出的背景物的浓度增加,同时也使分子解离增加。这两个因素共同制约着背景吸收。在恒温炉中,提高温度和升温速率,使分子吸收明显下降。
在石墨炉原子吸收法中,背景吸收的影响比火焰原子吸收法严重,若不扣除背景,有时根本无法进行测定。
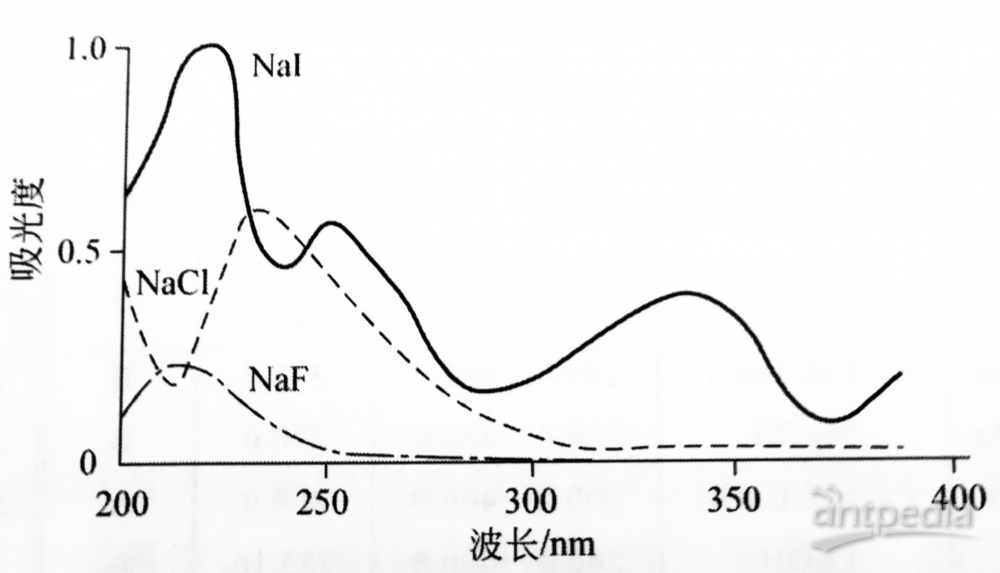
图1 卤化钠的分子吸收谱带
(3)火焰产生吸收现象 为消除背景干扰的影响,人们提出了各种方法。火焰原子化法中使用高温强还原性火焰,是一种有效的方法,但这样的火焰会使一些元素的灵敏度降低,并非适用于所有元素的测定。利用空白试液进行校正,配制与待测试样含有相同浓度基体元素的空白试液,测定其背景吸收值,再在试液测定中减去,可以达到校正的目的。此法虽然简单易行,但必须事先了解试样的基体元素及含量,往往会存在困难。
表1列出了空气乙炔火焰中一些元素分子吸收光谱的分布范围、最大吸收波长及其强弱程度。
表1 空气乙炔火焰中的分子吸收光谱
分子吸收带 | 吸收波长 范围/nm | λmax /nm | 强度① | 分子吸收带 | 吸收波长 范围/nm | λmax /nm | 强度① | ||
Li | LiCl | 190.0~270.0 | 226.0 | B | Li | LiI | 190.0~350.0 | 190.0 225.0 | B |
LiBr | 190.0~310.0 | 190.0 250.0 | B | LiOH | 190.0~340.0 | 200.0 260.0 | A | ||
Na | NaCl | 190.0~300.0 | 236.0 | B | Ti | TiO? | 200.0~400.0 | B | |
NaBr | 190.0~350.0 | 190.0 250.0 | B | V | VO? | 200.0~400.0 | 250.0 300.0 | A | |
NaI | 200.0~380.0 | 220.0 | B | Cr | CrO | 200.0~400.0 | 219.0 297.5 | A | |
NaOH | 200.0~400.0 | 234.0 332.0 | A | Mo | MoO? | 200.0~380.0 | 208.0 | ||
K | KCl | 190.0~285.0 | 243.0 | B | W | 200.0~400.0 | 220.0 | B | |
KBr | 200.0~320.0 | 210.0 | B | Mn | MnOH | 200.0~400.0 | 256.0 | A | |
KI | 190.0~380.0 | 190.0 240.0 | B | Fe | 200.0~400.0 | B | |||
KOH | 200.0~400.0 | 200.0 329.0 | A | Co | 200.0~400.0 | B | |||
Rb | RbCl | 190.0~295.0 | 190.0 250.0 | B | Ni | 200.0~400.0 | B | ||
RbBr | 215.0 | B | Pt | 200.0~350.0 | 205.0 | B | |||
RbI | 190.0~380.0 | 190.0 245.0 | B | Au | 200.0~400.0 | B | |||
Cs | CsCl | 190.0~285.0 | 190.0 248.0 | B | Al | AlO? | 200.0~430.0 | 241.0 | A |
CsBr | 190.0~330.0 | 190.0 275.0 | B | Ga | GaC l GaO | 200.0~300.0 | 240.0 | A | |
CsI | 190.0~380.0 | 200.0 245.0 | B | In | InCl InO | 200.0~340.0 | 267.0 | A | |
Be | BeO 或 BeOH | 190.0~400.0 | 217.0 | B | C | C2 | B | ||
Mg | MgOH | 200.0~400.0 | 270.0 | B | Si | ? | 200.0~400.0 | 225.0 | B |
Ca | CaO 或 CaOH | 200.0~400.0 | 200.0 | A | Sn | SnO | 200.0~380.0 | 322.0 | B |
CaOH | 540.0~600.0 | 553.16 | A | N | NO | 190.0~230.0 | 214.9 | B | |
Sr | SrO 或 SrOH | 590.0~660.0 | 625.0 | A | P | PO | 200.0~390.0 | 246.3 | A |
SrOH | 620.0~700.0 | 670.0 | B | S | SO2 | 180.0~350.0 | 207.0 | B | |
Ba | BaO 或 BaOH | 200.0~350.0 | 200.0 | A | 200.0~400.0 | — | A | ||
La | LaO 或 LaOH | 200.0~430.0 | 200.0 | A | Tl | — | 200.0~250.0 | 216.0 | B |
Ce | CeO? | 200.0~400.0 | B |
①A表示吸收值大,B表示中等程度吸收。
石墨炉中,分子吸收是在灰化、原子化阶段,某些稳定的化合物以分子形式蒸发进入吸收区或某些化合物分解形成的小分子进入吸收区产生。表2列出了部分盐类分子吸收波长范围及最大吸收波长。表中分子一列的含义是如H2SO4的吸收光谱,主要是SO2产生的分子吸收,磷酸盐的吸收光谱是磷的氧化物的分子吸收。
表2 部分盐类分子吸收波长范围及最大吸收波长
化合物 | 吸收波长 范围/nm | 分子式 | λmax /nm | 化合物 | 吸收波长 范围/nm | 分子式 | λmax /nm |
H2SO4 | 190~330 | SO2 | 200 | Ha2SO4 | 190~350 | SO2 | 200 |
HNO3 | 190~240 | NO | 205,215 | SQ | |||
H3PO4 | 190~300(弱) | PxOy | NaNO3 | 190~500 | NO | 205,215 | |
Na2HPO4 | 190~350(强) | PxOy,P2 | NO2 | ||||
LiCl | 190~280 | LiCl | 226 | SrCl2 | 190~300 | SrCl | 219 |
LiBr | 190~310 | LiBr | 250 | BaCl2 | 190~300 | BaCl | 220 |
LiI | 190~350 | LiI | 225 | CdCl2 | 200~270 | 210 | |
NaCl | 190~310 | NaCl | 240 | Al(NO3)3 | 200~280 | AlO | 214,254 |
NaBr | 190~350 | NaBr | 250 | Al-NaBr | 276~284 | AlBr | 279,280 |
NaI | 200~380 | NaI | 22,234 | Al-NaCl | 258~265 | AlCl | 261,262 |
KCl | 190~300 | KCl | 195,244 | Al-NaF | 227 | AlF | 226,227 |
KBr | 200~330 | KBr | 254,274 | Ga(NO3)3 | 190~280 | GaO | 240 |
KI | 190~380 | KI | 240 | GaCl3 | 241~270 | GaCl | 247 |
RbCl | 190~295 | RbCl | 250 | GaBr3 | 265 | GaBr | 265 |
RbBr | 190~325 | RbBr | 215 | Ga-NaF | 209~220 | GaF | 211 |
RbI | 190~380 | RbI | 245 | 292~305 | |||
CsCl | 190~285 | CsCl | 248 | In(NO3)3 | 206~350 | InO | 206,270 |
CsBr | 190~330 | CsBr | 275 | InCl3 | 265~296 | InCl | 266,267 |
CsI | 190~380 | CsI | 245 | InF3 | 227~253 | InF | 234 |
BeCl2 | 357 | BeCl | 357 | In-NaBr | 285~308 | InBr | 284 |
BeF2 | 330~400 | BeF | 301 | TlCl | 190~290 | TlCl | 252,311 |
MgF2 | 220~360 | MgF | 235,269,358 | 305~330 | 323 | ||
MgCl2 | 200~300 | MgCl | 270,377 | SnCl2 | 190~350 | SnCl | 198,323 |
CaF2 | 300~330 | CaF | 331,325 | PbCl2 | 200~300 | ||
CaCl2 | 190~300 | CaCl | 214 |
①吸收波长的中心位置。
散射背景是指原子化过程中产生的固体微粒对光源辐射光的散射而形成的假吸收。当基体浓度大时,由于热量不足,基体物质不能全部蒸发,一部分以固体微粒状态存在。微粒散射光强度与微粒本身的大小和入射光的波长有关,当微粒的直径小于入射光的波长的1/10时,服从瑞利散射定律:
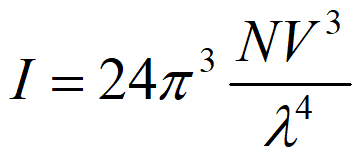
式中,I为散射光强度;N为产生散射光的微粒数;λ为入射光的波长;V为微粒的体积。散射光强度和波长的四次方成反比。随着微粒直径的增大,不再遵守瑞利散射定律,而是遵守米氏散射定律,即散射强度与波长无关。
散射对吸收线位于短波区的元素的测定影响较大,当基体浓度高时,或使用长光程火焰、发亮火焰或全消耗火焰进行测定时,更要注意散射的影响。
在原子吸收光谱法中,由分子吸收和光散射产生的表观的虚假吸收可以采用各种背景校正技术消除,最常用的一种是连续光谱法(氘灯法),即用氘灯测定背景吸收,再从测得的表观总吸收值中减去背景吸收值,得到真实吸收值;另一种常用的方法是利用塞曼效应校正背景的方法。其他较常用的还有双波长法、共振线吸收法、时间分辨测光法和波长调制法等(以上方法将原子吸收光谱分析中的背景校正技术中作较详细的介绍)以上各种背景校正技术都为光学方法,其他的方法还有石墨炉原子吸收中增加灰化温度,加入基体改进剂,利用电容放电高速加热和平台技术,在灰化阶段引入氧气和采用适当的升温程序等。在火焰原子吸收中采用高温火焰和用与试剂溶液相似成分的标准溶液作工作曲线的方法来消除背景吸收干扰。