颈内动脉闭塞曾被认为是外科不能触及领域,因为干预(颈内动脉剥脱、血管旁路移植及血管内治疗)风险往往远大于获益,闭塞血管开通成功率较低,死亡率较高,广泛颈内动脉血栓形成、解剖限制及串联病变存在更使开通难度增大。
随着各种栓塞保护装置的出现,经皮腔内血管成形术(PTA)成为可行,目前闭塞血管开通成功率为65%~73%。DSA仍为颅内外血管病变评价金标准,可清晰显示颈动脉粥样硬化斑块部位、大小、形态及管腔狭窄率,但无法了解血管壁组织结构、闭塞段血管真腔、斑块成分特点、有无附壁血栓及支架植入后情况等,往往影响手术决策及术后效果。
血管内超声(IVUS)借助导管直接置入血管,不仅清晰显示血管壁、管腔及斑块情况,还能根据斑块声学特征作组织学分型,已在心脏与外周血管疾病诊治中显示优势。本研究通过IVUS导引下PTA术治疗1例颈内动脉闭塞患者,效果良好。现将应用体会介绍如下。
1.材料与方法
本例患者男性53岁,以缺血性脑卒中收治入院。左侧肢体活动不利2周,既往有冠状动脉硬化性心脏病、高血压、2型糖尿病、高脂血症,左侧肢体肌力4级。CT及CTA提示右侧基底节区梗死灶,右侧颈内动脉闭塞,前交通动脉开放,代偿部分中动脉供血(图1①~③),脑灌注成像提示右侧大脑半球低灌注状态。患者签署手术知情同意书后,接受PTA治疗。术中DSA证实右侧颈内动脉自起始部闭塞,采用微导丝及微导管同轴技术通过闭塞段(图1④~⑨),启动IVUS诊断仪(美国Volcano公司),沿微导丝将IVUS导管推送出导引导管后除去环晕尾影,再推送至闭塞段,对回放采集影像中血管壁组织结构作测量分析,确认始终位于真腔内,将微导管跨越闭塞段作造影确认远端血管通畅,调整后在0.014英寸Traxcess微导丝(美国MicroVention公司)导引下将Spider颈动脉栓塞保护器(美国ev3公司)跨越狭窄段置于动脉远端,再将IVUS导管推送至病变远端,并与自动回撤装置连接,设置导管自动回撤速度,记录开始后以1.0mm/s速度拉IVUS导管,回撤至导引导管后停止检测采集;通过主机对回放采集影像中血管壁组织结构、斑块成分特点及管腔情况等(图1⑩)作测量分析,然后选取略小于颈内动脉直径的PTA球囊导管(爱尔兰ClearStream技术公司)作预扩张(降低血管重度狭窄且代偿不良后缺血-再灌注损伤),再更换更大球囊作扩张;IVUS检测发现狭窄段斑块稳定,管腔截面积由30.3mm2增加至48.4mm2,改善明显(图1⑪)。
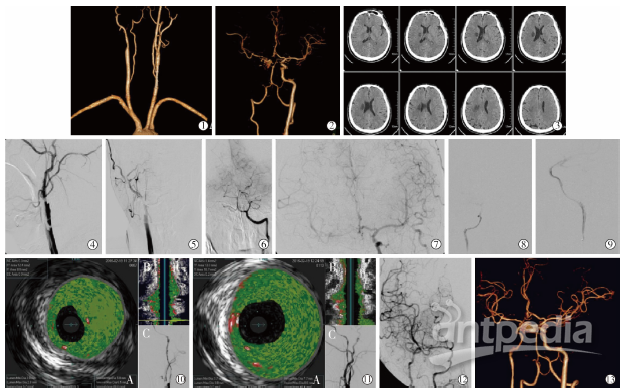
图1
2.结果
患者术后复查DSA、CTA显示右侧颈内动脉正向血流恢复良好(图1⑪),脑灌注成像提示右侧颞枕顶叶低灌注状态明显改善,脑梗死再通治疗后血流TICI分级评估为3级。
3.讨论
导致颈内动脉闭塞的原因很多,包括颈动脉粥样硬化、颈动脉夹层、心源性栓塞、海绵窦部位病变及脑底异常血管网病等。即使给予规范的药物治疗,再次脑卒中风险也达到6%~27%,长期颅内低灌注导致部分患者认知功能障碍,并由于同侧血管闭塞,代偿血管血流负担增加导致部分患者发生颅内动脉瘤,还有可能导致Willis环病理重构。慢性颈内动脉闭塞患者逐渐建立起侧支循环代偿,在能满足颅内脑组织血供时通常无自觉症状,但一旦出现全身贫血、心律失常、血压降低、全身血容量不足,甚至侧支代偿血管也发生狭窄或闭塞等,侧支循环有效代偿平衡被打破,病情随之恶化,进展为低灌注性脑梗死。
目前PTA治疗颈内动脉闭塞可获得较高的再通成功率,但仍需严格把握适应证。首先,患者存在闭塞相关症状性卒中或短暂性脑缺血发作,影像学上有颅内低灌注症状,此为再通适应证的重要标准;其次,闭塞段血管远端尽量不超越眼动脉段,近端有闭塞血管残端,这可确保介入治疗可行性,近端无闭塞残端开口则说明存在纤维帽,使开通成功率降低。手术中需要避免出现脑高灌注综合征(CHS)。其机制可能是机体为维持正常脑血流,小动脉扩张、慢性血管扩张导致血管自动调节功能障碍,无法适应颈动脉闭塞开通后瞬时高血流量所致,甚至出现脑出血、蛛网膜下腔出血等严重事件。
传统血管超声能够观察颈总动脉闭塞和颈内动脉起始段血管内特征,但无法判定颅内段闭塞血管内血栓特征。神经介入医师如果采用传统超声,术中往往需配备一名有经验的超声医师,由于介入室布局及减影需求,传统超声受到很大限制。IVUS很好地解决了这个问题,介入医师可独立完成操作及诊断,并全程监测,对兴趣节段可结合DSA同时动态分析,提升了手术精准性。介入治疗中更多困扰临床医师的是DSA以对比剂充盈影像间接反应管腔情况,虽然精度较高,但无法了解病变血管壁组织结构与粥样硬化斑块组成情况,支架植入后无法进行有效评价,具有一定的局限性。有研究表明,IVUS辅助冠状动脉支架植入术可降低支架内再狭窄率。
此外,突破动脉残端纤维帽进入闭塞血管真腔是介入治疗成功的关键,一旦导丝误入动脉中层斑块,DSA常不易判定。有研究报道在颈动脉内膜剥脱术的同时,直视下置入动脉鞘于颈动脉远心端并开通颅内闭塞段血管,但复合手术对患者创伤较大,适应证较窄,且手术同期植入支架在抗凝聚用药上存在矛盾,致使这一术式普及困难。这时若通过IVUS显示管腔横截面影像提供的管壁和斑块详细特征判断真假管腔,补充DSA不足,有助于解决临床棘手问题。
本例患者术中经球囊预扩张、更换更大球囊再扩张,随后IVUS评价斑块及管腔变化提示狭窄段斑块纤维帽稳定,管腔截面积由30.3mm2增加至48.4mm2,管腔狭窄率<40%,故仅行单纯球囊扩张治疗。必要时可反复进行后扩张,直至达到满意标准为止。如果患者斑块纤维帽断裂,坏死组织暴露于管腔内,或管腔狭窄率未达标,则需植入支架治疗,并再次评价斑块、管腔变化及支架效果。闭塞血管开通过程中利用IVUS虚拟组织学序列,可有效地了解开通段血管斑块及管腔情况,包括斑块近管腔内壁纤维帽情况、斑块成分、血栓负荷量、坏死及钙化组织比例等信息。
狭窄节段较长时全程支架成形并不现实,可根据IVUS检查结果选取斑块纤维帽破裂节段或易损斑块节段植入支架,确保恢复正向血流同时尽量减少支架植入枚数。支架植入贴壁不良或扩张不充分均为术后发生再狭窄及血栓形成等并发症的主因,这可能是由于血管平滑肌细胞增生所致,进而诱发支架内急性或慢性血栓形成。IVUS可有效地检测支架形态及贴壁情况,了解对称性和扩张情况并及时调整,降低并发症发生率,提高远期疗效。作为心脏介入治疗开发的IVUS,初步应用于颈动脉诊疗甚至颅内血管诊疗尚处于尝试阶段,目前国内外尚无相关标准及应用指南,临床上通常根据冠状动脉病变治疗特点用于颈动脉血管病变治疗。然而IVUS价格高昂,临床无明确应用指南支持,使得征得患者及家属同意应用较困难,故本中心总结的临床患者较少。冠状动脉直径相对颈动脉明显较细,IVUS在检测过程中在血管内受到血流波动影响相对较大,造成影像质量相对偏低,但通过调节IVUS检测直径数值等进行纠正,得到相对完整可靠的图像。
总之,通过本例PTA术实践,可以肯定IVUS是提升颈内动脉闭塞介入治疗效果的手段之一。