【前沿技术】Nature最新揭露:比类器官还要高级的操作——类装配体
01研究背景
类器官大部分来源于能自我分化的干细胞,常形成三维细胞团,具有器官的部分特性,但是此类模型未考虑到天然的组织结构和微环境,而且大量的细胞从生理环境中取出都会改变其特性。
这篇研究中使用了正常膀胱干细胞或膀胱肿瘤患者的类器官,使之与组织基质和微环境其他成分一起重构,包括组织基质中的基质成纤维细胞、内皮细胞、免疫细胞和肌肉细胞,并提出了表观遗传控制肿瘤可塑性机制。
02结果解构
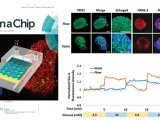
1)作者在原有培养的膀胱类器官中通过3D打印技术加入了组织基质和肌肉成分——基质成纤维细胞(小鼠胚胎成纤维细胞)和内皮细胞(HULECs-以及肌肉层,培养成了能够生长200天的三层膀胱类装配体,作者通过H&E染色和免疫荧光融合图展现了不同细胞组分在空间上的构象:具有多层折叠的尿路上皮基质含有波形蛋白阳性的间质成纤维细胞和CD31阳性内皮细胞,被α-平滑肌肌动蛋白(α-SMA)阳性平滑肌细胞(SMC)和CD31 +内皮细胞组成的肌肉层所包围。此外,作者使用平滑肌激动剂(SAG)或抑制剂(vismodegib)处理以及基因敲除小鼠进行对比,发现正常膀胱和膀胱装配体的反应性和遗传特性有一致性。
2)接下来作者证明利用单细胞RNA测序确定7中不同的细胞类型,同时比较培养7天以后的装配体和正常膀胱的序列相似性,约为90%。作者分析转录组尿路上皮亚群数据发现,尽管在最初使用异源细胞类型进行装配,但膀胱异装配体却经历了成熟过程,通过各种重组细胞类型之间的相互作用来重塑膀胱。功能方面,右旋糖酐渗透性测定还显示尿路上皮屏障功能得以维持,而且作者还建立了尿路感染模型(UTI),观察损伤诱导过程,发现少数上皮基底细胞可以再生膀胱上皮。
3)建立成功异源膀胱装配体后,作者又展开了下一项挑战:膀胱肿瘤类装配体——采用3D重建患者来源的膀胱肿瘤类器官(两个腔和两个基底),以及来自患者匹配的内皮细胞(HULEC)和癌相关成纤维细胞(CAF)。同时,作者观察到重建的内皮细胞常发展成血管网络,可促进肿瘤聚集体中的肿瘤生长,而且测序结果提示亲代肿瘤中的遗传改变在常规肿瘤类器官和肿瘤类装配体中均得到维持。在补充数据中作者还建立了较为成功的基于T细胞的免疫微环境的小鼠肿瘤组装体,确定该方法可用于研究免疫治疗领域。
4)在建立了强大的方法及平台以后,作者深入探索了肿瘤基质对维持类装配体遗传稳定的机制,作者通过测序找到FOXA1这个基因,过表达该基因发现肿瘤亚型发生官腔亚型的改变,敲除这个基因以后装配体同样发生基础亚型的改变,提示FOXA1通过控制增强子重编程来调控肿瘤亚型。进一步查阅文献和设计实验,证实上游是Hedgehog信号通路中的基质骨形变蛋白(Bone morphogenetic protein, BMP)在诱导FOXA1的表达。至此,作者找到影响膀胱装配体基底细胞与官腔细胞双向分化的一条调控轴:FOXA1-BMP-hedgehog轴,点出了肿瘤亚型可塑性的背后机制。
文章总结
虽然装配体(assembloids)这一概念并非这篇文章首次提出,但是作者利用异源组装的装配体,进一步建立了人源肿瘤装配体,还搭建了基于3D打印的高通量筛选平台,可谓一步到位。此外还进行了深入的机制研究,补充材料也包含了大量的测序数据,使证据环路更加充分,可以预见,这篇发表在Nature的关于assembloids的文章也将是未来体外器官研究进一步的发展方向。