碘量法
碘量法是以I2的氧化性和I-的还原性为基础的氧化还原滴定法。碘量法分为直接碘量法和间接碘量法。
(1)直接碘量法 直接碘量法也称碘滴定法。它是利用I2的氧化性直接滴定一些还原性较强的物质,如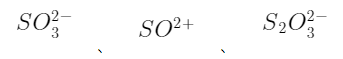 和维生素C等。由于I2的氧化性较弱,所以直接碘量法不如间接碘量法应用广泛。
和维生素C等。由于I2的氧化性较弱,所以直接碘量法不如间接碘量法应用广泛。
(2)间接碘量法 间接碘量法又称为滴定碘法。它是利用I-与氧化剂反应,定量地析出l2,然后用还原剂Na2S2O3标准溶液滴定析出的I2,其反应式为:

利用这一方法可以测定很多氧化性物质, 等,所以间接碘量法应用相当广泛。
等,所以间接碘量法应用相当广泛。
淀粉是碘量法的专属指示剂。直接碘量法以出现蓝色为滴定终点,间接碘量法以蓝色消失为滴定终点。应注意的是在间接碘量法中,淀粉指示剂应在近终点时加入,以防止较多的I2被淀粉包裹,而导致终点滞后。
(3)碘量法的误差来源及应采取的措施 碘量法的误差来源主要有两个方面:一是碘易挥发;二是在酸性溶液中I-易被空气中的O2氧化。为了减小滴定误差,保证分析结果的准确度,在滴定过程中应采取以下措施:
①加入过量的KI(一般比理论量大2~3倍)
②KI与氧化性物质间的反应需在密闭的碘量瓶中进行;为使反应完全,加入KI后要在暗处放置5~10min,避免阳光照射,并用水封住瓶口。
③反应完全后立即用Na2S2O3标准溶液滴定。
④滴定I2时不要剧烈摇动,应尽量轻摇、慢摇,以减少I2的挥发。
⑤溶液的酸度不宜太高,否则会增加被空气氧化的速度。
⑥滴定速度要适当快些。
其他的氧化还原滴定法还有高锰酸钾法、重铬酸钾法、溴量法等。
