
推荐要点
01
此文从如下几个角度入手:AMH 亚型的检测与分析、AMH 测量中的干扰因素、AMH 测定系统之间的偏差和转化系数,对 AMH 的实验室测定过程中常见的问题进行了阐述。
AMH 根据其分子生物学特性,在体内存在 AMH-C、AMH-N、AMH-NC;其中 AMH-NC 与 AMH-C 存在生物学活性,但 AMH-C 的生物学活性较弱;AMH-N 无生物学活性。因此在 AMH 的测定中,可能会导致测试结果高于患者实际结果而导致偏差的出现。未来 AMH 测定和厂商的发展趋势可能是 AMH 亚型的标准化分型测定。
主要内容
02摘要
抗苗勒管激素(AMH)是一种 140 kDa 的同型二聚体糖蛋白,由两个相同的亚单位组成,通过二硫键连接,由睾丸和卵巢合成。其临床应用主要是用于预测卵巢反应和促排卵过程中促性腺激素的剂量选择。在男性和儿童,AMH 用于研究性发育障碍和性腺功能。AMH 通常通过酶联免疫吸附试验或不同方法学的自动免疫分析试验进行分析。但 AMH 的测定仍存在标准化测定缺乏的问题,AMH 的供应厂商较多,不同的方法学也使得其测量结果互有偏差,这在一定程度上困扰着临床和检验医师。
内容简介
本文使用 PubMed 和 Google Scholar 数据库进行电子文献搜索。使用的搜索词为:「AMH」、「MIS」、「测量」、「方法比较」、「方法评估」、「分析干扰」【原文:「AMH」, 「MIS」, 「Measurement」, 「Method comparison」, 「Method evaluation」, 「Analytical interference」】。纳入标准为限定为人体 AMH 测定的研究。排除标准为无法找到全文、非英语文献、参考文献不全或发表年限超过 20 年。探讨的关键问题为 AMH 分析的标准化、AMH 测量中使用的抗体、检测干扰、手动和自动 AMH 检测的检测限以及 AMH 分析之间的系统误差。
检验医学是为临床医学所服务的,因此准确可靠的测量结果是实现准确的诊断和疾病监测的重要基础,临床上针对特定疾病的截断值的建立以及临床诊断、应用均要基于测量结果的稳定可靠。AMH 免疫分析的测量在过去二十年中不断发展。不同厂家使用了各种校准品和抗体对来定量 AMH。因此,偏差、不精确性和检测限表现出很大的异质性,分析灵敏度一直是 AMH 的测定中最大的挑战点。近年来各大公司在新的仪器开发上采用自动化模式,提高了分析灵敏度。表 1 总结了目前市场上 AMH 测定产品主要特征对比情况。

文献中提出,缺乏使用参考方法对照国际标准对 AMH 分析进行校准会导致分析间偏差。AMH 测量受到不同厂家生产的仪器及实际的相应分析标准的影响较大。AMH 的不同厂家使用仅适用其自身的校准方法,因其溯源不同,其数值也会不同。这导致各厂家的 AMH 标准曲线的差异性较大,使得同样的样本在不同厂家的仪器上进行测定时,其测量数值也表现出差异,当这种差异较大时,会对临床诊疗造成一定程度的困扰。世卫组织国际标准的参考试剂(标准化)或标准与技术研究所(NIST)认证的标准参考材料(SRM)仅用于特定应用下有限数量的测量。因为建立标准化方法学极其昂贵,需要巨量的人力资源,还包括各个阶段极其复杂的过程。
临床专家呼吁建立能够校准不同厂家 AMH 测定结果的国际标准,因为这能使不同厂家 AMH 的测定结果(通过换算等方式)进行通用,可以极大程度上方便临床的使用、对 AMH 功能的进一步开发以及研究。世卫组织专家委员会于 2014 年批准了 AMH 免疫分析国际标准的制定,将这一重组 AMH 试验制剂成为 SS-581,保证在冻干形式下仍可表现出稳定性;后又研究出一种重组 AMH 制剂,编码 16/190,为世卫组织所认可。但 16/190 仍存在其局限性,在不同厂家的仪器上进行测定时,其表现并不尽如人意,因此世卫组织仅将其作为参考试剂,而未将之定义为国际标准所启用的试剂,但无论如何,这种尝试走出了 AMH 标准化的第一步。
AMH 的亚型结构带来的干扰
随着分子生物学的研究,AMH 是从其前体 pro-AMH 合成来,pro-AMH 通过「先水解,再剪切」的模式才能变成有活性的 AMH。Pro-AMH 在 229AA 和 451AA 处包含两个切割位点,切割后可形成 AMH 亚型家族。Pro-AMH 的蛋白水解导致分子裂解为无活性的分子量为 58 kDa 的 N-末端「pro-region」结构域(AMH-N)和具有生物活性的分子量为 12.5 kDa 的「mature」C-末端结构域(AMH-C)的形成,AMH-N 和 AMH-C 也为二聚体存在,最后通过非共价二硫键连接形成分子量为 140kDa 的同时具备 N、C 端的 AMH-NC,通过糖基化并分泌入血,因此人体内同时存在 AMH-N 和 AMH-C,以及其结合产物 AMH-NC。此外 AMH-N、AMH-C 也是通过二聚体形式存在。研究中发现,仅有 AMH-C 和 AMH-NC 存在生物学活性,AMH-N 无生物学活性,然而,AMH-C 仅为部分活性,需与 AMH-N 结合,变成 AMH-NC 才能通过与 AMH-II 型受体结合以发挥其最大作用。因此,在市面上 AMH 的测定中,存在将 AMH 测定数值放大化而导致其测定数值高于实际活性的情况。因此在检测中,非活性(AMH-N)、部分活性(AMH-C)和完全活性被测物(AMH-NC)会增加被测物总浓度并产生假阳性结果。血中 AMH 各个亚型的比率尚未完全研究透彻。鉴于当前的 AMH 免疫分析技术的限制,在血中检测到的 AMH 为表示生物活性和非活性亚型的总和。因此,总的 AMH 实验室结果可能会「虚假地」升高,在临床应用尤其是辅助生殖领域中,可能会错误地对患者的临床状态进行分类。见图 1.
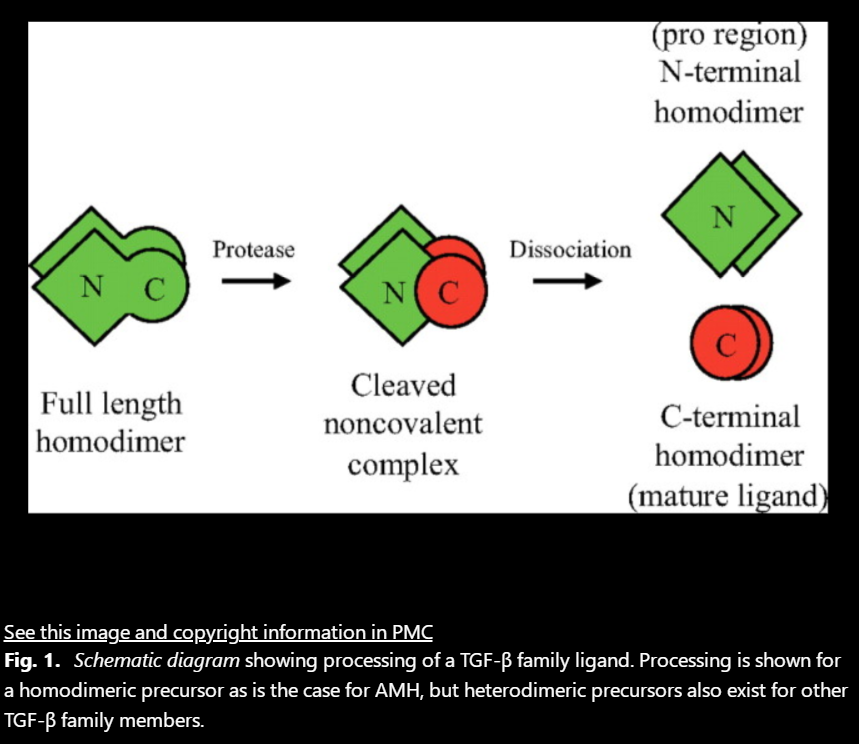
AMH 的准确测定还受到下列因素的制约:不同疾病状态下,AMH 的亚型比例也可能不同,这将影响 AMH 的准确测定。然而,这需要对病理学和健康状态下人群,其所含 AMH 不同亚型的比率进行分析研究,以便为测量体内特定 AMH 亚型的选择性分析提供信息。此外具有不同 pH 值和离子浓度的基质,可以改变 AMH 亚型的三维结构及其检测从而可能影响 AMH 水平测量。
此外,抗体特异性的差异也会影响 AMH 检测的结果,在三种 AMH 产品(AMH Gen II,超敏 AMH、picoAMH)中 AMH 水平测定的横断面研究中,观察到 picoAMH(97%)和超敏 AMH 分析法(92%)检测 AMH 水平的比例明显高于 Gen II 分析法(84%)。抗体设计的持续发展需要考虑特异性、交叉反应性、表位位置和临床应用的变化。因此文章提出,各厂商如能就相关的 AMH 生物亚型达成一致,或将提高 AMH 检测的特异性和分析一致性。
AMH 的免疫分析干扰
众所周知,免疫分析受到多种来源的分析干扰,包括嗜异性抗体、人类抗动物抗体、血清蛋白(如类风湿因子、结合白蛋白等)、药物和药物代谢产物以及异常血液状态(如溶血、高脂血症和高蛋白血症)。在干扰水平较大时,通常会以样本污染等方式「退出」检验;然而,在日常检测中,低水平干扰可能无法被检测,这种干扰会表现数值的偏差并对结果产生不利影响由于 AMH 的限制(免疫学检测项目),其相对较易受到各种分析干扰。
基于生物素-链霉素亲和素的免疫分析已证明在竞争性和非竞争性夹心免疫分析中分别存在正分析干扰和负分析干扰。目前市面上许多 AMH 分析使用基于生物素-链霉素亲和素的方法,故存在此类干扰的风险。使用替代抗原捕获方法则避免了这种分析干扰。
此外,补体水平会干扰 AMH 测量,导致测量结果偏低。这种情况多出现于前述的 AMH Gen II,后其引入预稀释步骤,改善了补体干扰,但存在测量结果偏高的风险。
已被证明,自动检测会在一定程度上降低手动检测多个繁琐步骤所带来的的干扰,自动检测的普及,提供了更高的灵敏度和更优异的检测限,对低水平的 AMH 检出也越来越好。
不同厂商所生产的 AMH 产品测量数值之间的比对
表 2 给出了不同厂商、不同产品见 AMH 产品测量数值的比对情况和换算关系,由于检验方法学的不同,其结果差异也较大。供参考。
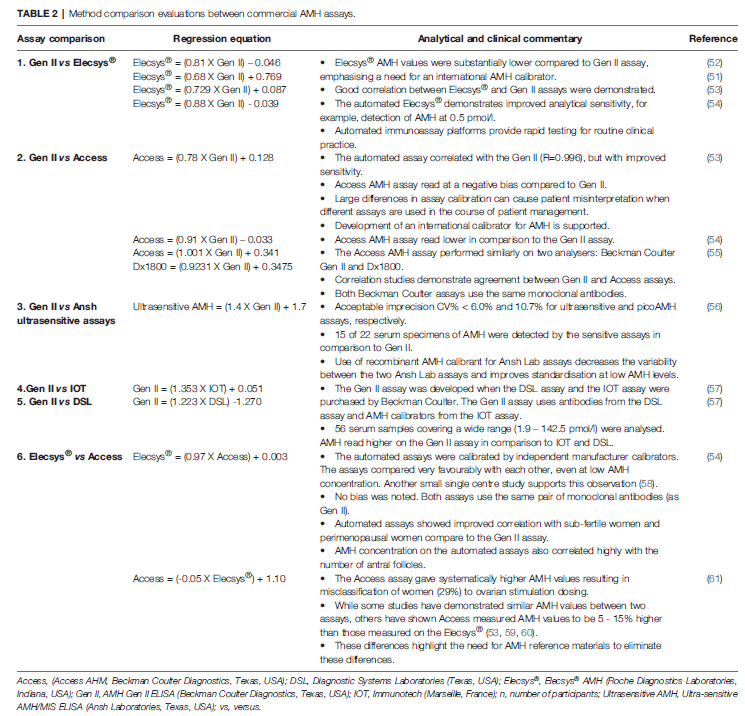
总结
AMH 在不同厂商的产品上测定结果差异较大,最重要的原因是缺乏确保统一校准的国际标准化材料。但世卫组织所推荐的参考试剂,有望改善分析之间的可比性。影响测定结果的其他因素包括抗体设计、免疫学方法、测定模式(手动/自动)以及对 AMH 亚型精确识别的技术空缺。在检验学技术和免疫学方法的完善和发展下,AMH 的测定水平将更加精准;未来 AMH 测定和厂商的发展趋势可能是 AMH 亚型的标准化分型测定。
参考文献:Front Endocrinol (Lausanne). 2021 Sep 3;12:719029. doi: 10.3389/fendo.2021.719029. eCollection 2021