2022末AutoChrom
竞赛优秀答案之一
2022年末AutoChrom竞赛参考答案与获奖名单已于上周公布,大家对高分大神的答卷是否很好奇呢?
本周,ACD/Labs将陆续公布竞赛前三名的优秀答案,供大家学习和参考!
本次分享的优秀答案来自南京百泽医药科技有限公司的王贤老师。
01
在下图的logD叠合图里,黑色箭头所指的曲线代表列表中的几号物质(编号1-9),请阐述判断的原因。

答:9号物质。
通过logD曲线可以看出,黑色箭头指定的化合物在pH0~5范围内loD持续减小,然后在pH5~12范围内保持不变,可以推测该化合物是一个强酸性化合物,pKa较低,在较低的pH范围内即可完全解离,且该化合物在pH0~12范围内其logD<0,说明其去质子化后疏水性较弱极性较大,故推测该化合物是9号物质,苯环上取代的磺酸基团可以解释以上特征的pH~loD曲线图。
02
在进行pH 筛选时,获得了以下的筛选结果。请根据色谱行为判断以下7个物质的酸碱性特点。请选择以下您最满意的一针,并阐述理由。
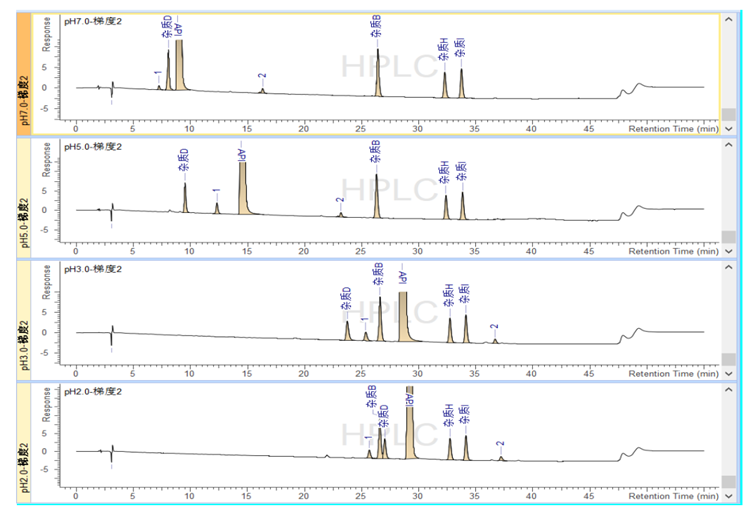
答:1)杂质B、杂质H和杂质I,pH从2.0~3.0~5.0~7.0逐步升高,保留几乎不变,推测是中性化合物,pH对它们的保留几乎没有影响;
2)化合物1、化合物2及API,pH从2.0~3.0~5.0~7.0逐步升高,pH2.0和3.0时保留几乎无变化,但继续升高pH至5.0或7.0时,保留逐渐减弱,推测是弱酸性化合物,pKa在4~5左右;
3)杂质D,pH从2.0~3.0~5.0~7.0逐步升高,保留逐渐减弱,推测也是弱酸性化合物,但比上述几个化合物酸性更强,pKa应在<4左右;
4)我认为在pH=3.0时结果最好,原因如下:首先pH2.0时前面几个杂质分离不佳舍弃;其次pH5.0的体系常用的磷酸盐体系没有缓冲作用,乙酸铵的体系在缓冲范围内,但若是末端吸收的化合物也不适用,且此时pH与大部分化合物pKa较为接近,耐用性较差不可取;第三,pH7.0时常用的磷酸盐虽然有缓冲作用,但常规pH能耐受到2~8的范围的长期在pH7.0使用寿命也会下降的较快,特别是没经过惰性处理的不封端色谱柱,且pH7.0时主峰和前两个杂质相隔较近,保留较靠前,耐用性考察条件变化时容易有分离和峰型的风险;而在pH3.0时各化合物分离良好,保留适中,与大部分化合物pKa相隔较远,多数化合物均以分子形态存在,常用的磷酸缓冲液在pH3.0时缓冲还可以,方法重现性和耐用性风险较低,因此pH3.0应更合适(梯度还可以有再继续优化缩短的空间)。
03
如图化合物,在杂化C18耐碱色谱柱上进行筛选时,不同的pH下主峰峰形以及保留时间存在有趣的变化,请基于物质结构描述主峰峰形以及保留时间变化的原因。

答:1)分析化合物结构,含有2个羰基,其中环酮上的羰基,可能受亲核进攻,导致化合物呈现不同的存在形式,峰型就会变差,这一亲核反应在高pH条件下会被抑制,使化合物呈单一形式,峰型就会变好,但在低pH峰型更差,但是该例子里低pH的高氯酸条件下峰型也很好,说明峰型变差可能主要不是亲核加成导致的。2)另外一个原因可能是该结构环酮上的羟基会有烯醇互变,整个结构芳香化了,在酸碱性条件下都是以烯醇式为主,可以看成类似苯酚的结构,在pH=11.5时可能只存在离子化的结构,峰型较好,而强酸性pH环境下也主要以单一烯醇式结构存在,呈现分子型,因此峰型也较好,中间pH两种形式可能都存在峰型较差,pH从9.2~11.5变化时,化合物的峰型越来越好,同时随着pH值升高,化合物上的酚羟基解离越多,呈离子状态的部分越多,导致logD值下降,化合物的保留越来越弱(这里更能说明是类似酚羟基的烯醇式结构),而pH9.7与pH9.2的保留反转可能是此时pH与酚羟基的pKa接近,保留和峰型更容易变化导致,但也能看出来pH9.2更远离pKa峰型更好。
另外,对于化合物在pH1.6的高氯酸溶液中,存在形式呈单一,此时保留增强可能是因为高氯酸作为离液剂,在一定程度上修饰了含有碱性基团(有一个弱碱)的化合物的峰型同时延长了保留,而且此时化合物上呈分子型疏水性更强,保留也会相应变强。
04
硅胶基质相同但孔径不同的色谱柱其特性也会有明显的不同,如下图ACE 5 C18, ACE 5 C18-300色谱柱的TANAKA测试结果。

请问:用同样的中性条件运行相同的梯度来分离以下1,2号化合物,上下两张色谱图中,哪张是ACE 5 C18-300的结果?这和TANAKA柱效测试的哪个参数最相关?请加以阐述。

答:下面那张的色谱图是ACE 5 C18-300色谱柱的结果;可能的原因如下:
1)首先与第上面的那张色谱图相比,下面的色谱图中两个化合物的保留时间更小,这与Retention Capacity(kPB)参数相关,从色谱柱的TANAKA测试结果来看,ACE 5 C18-300色谱柱的Retention Capacity(kPB)比ACE 5 C18 小,说明300孔径的色谱柱保留能力更弱一些,孔径越大,比表面积越小,固定相表面覆盖的量更低,保留也会相对减弱,因此下面的图应是大孔径的柱子。
2)其次与上面的那张色谱图相比,下面的色谱图中两个化合物的分离度明显增加,这与Steric Selectivity(αT/O)参数相关,化合物2与化合物1多连了一个六元杂环(其他结构很相似,杂环上无酸碱基团),增加了空间位阻,此时空间选择性对这两个化合物的分离也不能忽视,从色谱柱的TANAKA测试结果来看,ACE 5 C18-300色谱柱的Steric Selectivity(αT/O)比ACE 5 C18 大,因此选择性会更好,分离度更大。当然这两根色谱柱的氢键选择性也有一定差异,其中ACE 5 C18的aC/P值更大,说明氢键的作用力也更强,可能也会对保留有一定的贡献。
05
Intersil ODS-3 色谱柱和SB-C18 色谱柱在物质的保留上有相似之处也有不同之处,请结合有图TANAKA 柱效测试的数据比较的结果解释左图的保留行为现象。
*注释,左下图的线性较好的实心菱形为中性化合物,且基本无杂原子取代基团

答:1)首先分析色谱条件:流动相A是pH=2.8的磷酸溶液,流动相B是乙腈。在此条件下,从色谱柱的TANAKA测试结果来看,两根色谱柱参数差异从绝对值来看,最大的是Retention Capacity(kPB),分别是7.74和6.00,其次是Ion Exchange Capacity pH2.7和7.6(αB/P),然后是H-bonding Capacity(αB/P),分别是0.48和0.65;
2)继续分析左图结果:中性化合物且几乎无杂原子取代基团(实心菱形),主要的分离和保留原理是疏水性的差异,即与色谱柱的Retention Capacity(kPB)和Hydrophobic selectivity(aCH2)参数最为相关,从上述分析发现两根色谱柱的Hydrophobic selectivity(aCH2)相差不大,但Retention Capacity(kPB)相差较大,说明两根色谱柱的固定相键合密度和比表面积有一定差距,因此会对化合物的疏水保留能力不一样,根据疏水作用力的大小呈线性关系,因此中性化合物且几乎无杂原子取代基团(实心菱形)在两根色谱柱上的logK作图时,r值大于0.99;
3)而对于强碱性化合物(多边形)和脂肪胺(正方形),在pH=2.8条件下,化合物均处于质子化状态,带正电荷且均含有N原子,除疏水作用外,离子交换能力和氢键作用对其保留影响都很大,即与色谱柱Ion Exchange Capacity pH2.7(αB/P)和色谱柱H-bonding Capacity(αB/P)参数最为相关,而从TANAKA测试结果来看,这两根色谱柱这两个参数差异较大,尤其是离子交换能力pH2.7时相差10倍以上,其中Inertsil® ODS-3色谱柱是典型的C18封端柱,而SB-C18柱属于带有侧链大体积空间位阻保护硅醇基的不封端色谱柱,硅醇基的活性更强,因此强碱性化合物(多边形)和脂肪胺(正方形)在两根色谱柱上的logK作图时,与中性化合物且几乎无杂原子取代基团(实心菱形)相比,它们在SB-C18上的离子交换作用更强,保留更强,导致偏离线性。说明很多时候化合物的保留和分离不仅仅是简单的疏水作用力,还有其他的离子交换、氢键作用力、空间位阻作用力等都是不可忽略的作用力。
06
与传统杂化C18色谱柱相比,硅胶球表面带有电荷的色谱柱的保留行为会有所不同。如下图安捷伦公司的CS-C18。请结合物质结构以及logD图,分析解释CS-C18色谱柱上保留行为与HPH-C18色谱柱的差异性。

答:1)从色谱图上的保留顺序来看,两根色谱柱的酸性化合物8和9的保留均最强,那么流动相的pH应为酸性条件,此时实验pH条件下8和9均呈离子型,带负电荷,与HPH-C18色谱柱相比,CS-C18色谱柱表面的的正电荷对带负电荷的化合物8和9有较强的静电吸引作用力,所以其保留比在HPH-C18柱上强;
2)化合物5~7均是只含碱性基团的化合物,其中7是脂肪胺碱性较强,5和6是弱碱碱性较弱,在实验pH条件下7完全质子化,5和6部分质子化,因此与HPH-C18色谱柱相比,CS-C18色谱柱表面的的正电荷对7的电荷排斥作用力较强,在两根色谱柱上7的保留变化较大,而对5和6的静电排斥作用力较小,故5和6的保留在两根色谱柱上的变化相对较小。
3)化合物1~4均是同时含有酸性和碱性基团的化合物,在实验pH条件下碱性基团也均质子化,酸性基团基本完全呈分子型,此时化合物1~4在HPH-C18色谱柱上按照疏水性的大小依次2、1、3和4出峰,而在CS-C18色谱柱上除了疏水性以外,还有色谱柱与化合物之间的静电排斥作用力,该4个化合物在CS-C18色谱柱上整体保留均比HPH-C18小的多,而且观察到在这种复杂的静电和疏水等作用力综合下,化合物1和2在两根色谱柱上还出现了保留的反转,可能与1和2的化合物空间位阻相关,1比2更容易与CS-C18柱产生相互静电排斥,从而保留更弱。
07
下图是一个研究员的两因素两水平优化实验设计及其谱图,请基于谱图指出不同因素对色谱峰形态,保留以及分离的影响,识别四张典型谱图中的所有风险,给出下一步优化的方向。



答:对比图1和图2(或图3和图4)可知:
► 温度升高,化合物1、4保留几乎不变;化合物2、3、5、6保留减弱;化合物7~15保留增强;
► 温度升高,化合物14(主峰)峰型改善明显;
► 温度升高,更多对化合物之间的分离变差;
对比图1和图3(或图2和图4)可知:
► 梯度变缓,几乎所有化合物(除化合物1外)保留都有不同程度的增强;
► 梯度变缓,主峰的峰型更展宽;
► 梯度变缓,对各化合物之间的分离影响不大;
根据这4张图可知:
► 化合物1的保留存在风险;
► 在低温时,化合物14(主峰)峰型存在风险;
► 化合物14(主峰)与相邻杂质化合物13存在严重的分离风险;
► 化合物2与3之间、化合物6~9之间、化合物11与12之间的分离均存在风险;
下一步优化方向:
► 对于化合物1的保留和峰型较差(溶剂效应)的风险,考虑降低有机相初始比例延长保留,必要时可换成较亲水的色谱柱并增加一段等度运行再上梯度,或者根据化合物结构调整流动相pH值,或加入离子对试剂或者离液剂(末端吸收离子对梯度洗脱慎用)或使用混合型色谱柱等手段来增加保留;
► 对于主峰峰型的风险,需从结构出发,考虑是否筛选pH,选择合适的缓冲液或加入离子对或离液剂等改善峰型;
► 对于整体化合物之间的分离较差的风险,可综合考虑上述因素,先考虑简单的两因素实验,在现有的基础上降低有机相起始比例(如10%或5%)和降低柱温(35℃和15℃)重新设计模拟,再根据结果考虑是否设计更复杂的实验如:缓冲液pH&梯度&温度或有机相种类(比例)&梯度&温度等多因素,设计三因素(3*3*3)试验,借助ACD建模,来寻找设计空间,以保证方法的耐用性;
08
在进行手性分离的建模优化时,进行温度单因素的研究,单因素温度取样点为(10,20,40摄氏度),结果建模后碰到了如下图实测和预测误差大的情况,请问应该如何解决?

答:根据文献和经验可知,一般手性化合物的分离通常至少需要3点作用力,主要以氢键、空间位阻选择性、π-π作用、偶极-偶极或静电等相互作用力进行手性识别,手性分离对温度和流动相组分的变化相对于普通反相色谱来说更敏感,因此仅进行温度单因素(虽已经做了3水平,考虑到二阶多项式)建模,建模后试验与模拟结果之间的误差仍然比较大(ΔtR在8%~15%)。为解决这一问题,有必要进行流动相比例和温度两因素DoE试验,实验设计应最少为3*3,必要时还可以增加试验点数,以便于得到更好的模型,寻找更好的耐用性空间。
09
Dwell Volume(柱前体积,梯度延迟体积) 存在差异是仪器间方法转移时经常会碰到的挑战。测量Dwell Volume的方法如下:

请描述您在进行仪器间转移时克服Dwell 差异的策略。
答:不同仪器间方法转移可能会因为Dwell差异导致转移失败,一般简单的策略可以考虑增加或改变梯度的等度运行时间,在转移时也可以根据不同品牌仪器将延迟体积输入色谱软件进行换算,但是实际上真正在实验室进行转移时改变方法的风险很大,接收方基本不会冒险接受,而且也会受到审评机构的挑战,从经验上看,有效避免转移失败的方法是在转移之前需要做到开发或验证阶段就应该将不同品牌仪器(特别是接收方有的)、不同批号色谱柱(新旧色谱柱差异有的会很大)、不同型号色谱柱(耐用性需要增加备用柱考察)、不同天不同人、不同方法参数(耐用性)都要做过详细的考察才能更有保障。但究其根本是方法的耐用性较差导致的。采用传统的“试错”模式开发出的方法,未考虑到各因素之间的交互效应,“最佳”方法可能是在设计空间的边缘,方法耐用性极差。为解决这一问题,应该采用分析方法生命周期管理(ALM)和质量源于设计
(AQbD)理念,通过评估方法变量之间复杂的交互作用,借助计算机辅助软件(ACD)将多元参数进行系统性优化,并将在一定范围内的参数变化(包括不同仪器之间的Dwell的体积差异)在方法开发期间就考虑进去,对耐用性空间进行筛选,提前识别风险点,从而更好的控制方法的变异。建议可按以下步骤进行:
1) 确定分析目标(ATP)和关键分析属性(CAAs);
2) 风险评估:借助科学的色谱知识,找出高风险因素;
3) 初步的方法开发;
4) 实验设计(DOE):先筛选(如采用Placet-Burman设计评估分析条件(X)对色谱响应(Y)的影响,并确定显著性分析条件),后优化(如采用Box-Behnken设计对方法进行优化,考虑多因素交互效应,将色谱响应控制在可接受范围内);
5) 设计空间(DS)和中心点的选择:实验设计数据可借助ACD软件进行建模,找到设计空间和中心点,确定最佳方法;
6) 耐用性考察:预测区间将应用于评估分析方法的耐用性,可用于评估未来常规分析过程中不同色谱条件交互作用引起的变异程度,通过将预测空间与给定的设计空间(DS)比较,可以得出该方法对交互作用的耐用性抵抗能力(如可建立析因设计以评估分析方法的耐用性)。
7) 方法验证:从精密度、准确度、专属性、灵敏度等各方面考察方法。
8) 持续的方法性能验证:进行分析方法生命周期管理(ALM)。
10
请比较Plackett -Burman 实验设计方法和传统耐用性实验方法的差异。

答:1)传统的耐用性研究是在中心点选定后,固定其他因素,每次只变动一个因素的水平考察其对结果的影响。这种实验设计方法无法评估多个因素同时发生微小变化时的风险。
2)而采用Plackett -Burman设计方法,可以对多个考察点同时进行考察,试验数量则仅为十几个,大大增加了时效性。在Plackett -Burman设计中,选择方法的高低水平及相应的关键方法属性和限度要求,经过统计学软件的分析后,借助主效应图和显著因子,可以识别出对方法耐用性挑战最大的因素是什么,以便于调整中心点,或者进一步优化。通过Plackett -Burman的耐用性研究,建立起整套方法的知识空间和可操作空间,了解对于每一个关键方法属性有影响的因素和影响因素的大小,为之后的方法验证及转移打下良好的基础。
3)从提供的表格里7个参数来看,常规预验证耐用性考察至少需要做15组实验的考察,而采用PB设计高低2水平最多也是12组实验,从实验组数来看也更有优势。为正式的方法学验证时能提供更全面的一个方法评判依据。