胰蛋白酶水解分析。蛋白质水解产生的肽段利用反相高效液相色谱分析,流动相采用含TFA体系(参见第15-17页),以起始浓度约5%的乙腈梯度洗脱(乙腈起始浓度低于5%可能导致较早洗脱出肽的色谱的不可重现性),乙腈浓度逐渐升至70%(参见图31)。
梯度洗脱的时间取决于待水解蛋白的大小。
大分子蛋白比小分子蛋白水解产生更多的肽段,因此肽段的分离需要更长洗脱时间。
小分子蛋白(小于20kd)水解产生的肽通常可在45~60分钟内完成分离。
大分子蛋白(20-50kd)需要较长的洗脱时间,一般为60~120分钟。
分子量大于50kd的蛋白质需要120~180分钟的洗脱时间。
采用1~2 ml/min 的流速和适宜的温度时分辨率最佳。
通常采用C18 反相柱。可以使用孔径为100埃或300埃的柱子,其选择性通常不同。
图31. 牛血清白蛋白的肽图
色谱柱:ACE 5 C18-300 宽孔柱,4.6 x 150 mm
流动相:4%~70%乙腈-0.1% TFA 体系,混合梯度洗脱120分钟。

蛋白质修饰引起肽保留时间的变化。如果蛋白质因翻译或表达错误,降解(脱酰胺作用、氧化反应)或过程变异而改变,则这种改变将会反映在一种或多种肽段。
由于与肽的反相相互作用的灵敏度,肽的任何变化都将导致该肽保留时间的变化。
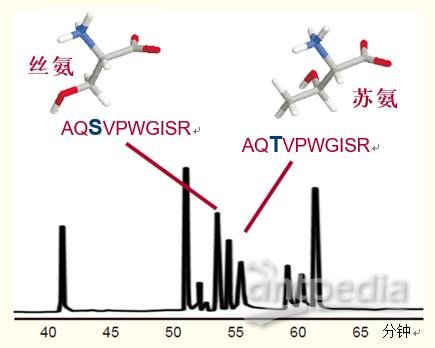
在图32示例中,相差一个氨基酸的两种十肽,其中一个为苏氨酸,另一个为丝氨酸,在反相HPLC图谱中出现了两个峰。
不仅仅是一个氨基酸的差别,而且两种氨基酸均为羟基氨基酸,它们的不同之处在于苏氨酸侧链上加了一个甲基。
这说明了蛋白质的任何变化都会反映为肽的变化,从而导致该肽保留时间的改变。
肽图分析的本质是反相HPLC能够实现差别细微的多肽的分离。
图32. 以RP-HPLC对紧密关联的肽类进行分离。
仅有一个氨基酸不同的两种十肽菌素,一种含丝氨酸,而另一种含苏氨酸。
条件
色谱柱:C18 宽孔柱, 4.6 x 250 毫米
洗脱液:
A. 含有0.1%三氟乙酸的水溶液
B. 含有0.08%三氟乙酸的乙腈溶液
梯度:0 - 35%的B溶液超过73分钟
试样肽图与参照蛋白质肽图的比较。肽图能够提供有关蛋白质的很多信息。
惯常做法是对试样的肽图和参照蛋白质的肽图进行比较。
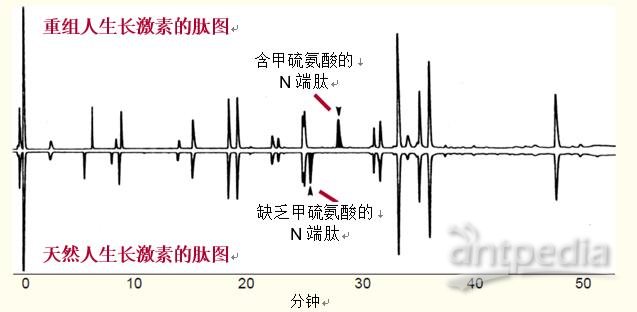
图33对重组人生长激素(在大肠杆菌中表达)的肽图和天然人生长激素(缺乏甲硫氨酸)的肽图进行了比较。
由于甲硫氨酸的疏水性质,重组人生长激素比天然人生长激素较晚洗脱出来。
在这个例子中,为了便于比较,将第二幅图谱倒置显示。
在一些情况下,为了确认微小的变化和证明分析工具与肽图的变化无关,会将两种水解产物混合进行色谱分析。
肽图比较揭示了蛋白质的改变和修饰,如:基因改变、翻译错误、蛋白降解(脱酰胺作用、氧化反应),以及翻译后修饰的改变。
图33. 重组人生长激素和天然人生长激素(缺乏甲硫氨酸)肽图的比较。
条件:
色谱柱:C18宽孔柱,4.6 x 150 mm
流动相:0~70% 乙腈-0.1% TFA 体系梯度洗脱