摘要:体外诊断试剂对于人体样本(各种体液、细胞、组织样本等) 的体外诊断(In Vitro Diagnosis, 缩写为 IVD) 起着关键性的作用,其中使用的纯化水也同样扮演着重要的角色。
体外诊断试剂属于医疗器械的一部分,它包括检测试剂、试剂盒、校准品(物)、质控品(物)等,可单独使用或与仪器、器具、设备或系统组合使用。在疾病的预防、诊断、治疗监测、预后观察、健康状态评价以及遗传性疾病的预测过程中, 体外诊断试剂对于人体样本(各种体液、细胞、组织样本等) 的体外检测(In Vitro Diagnosis, 缩写为 IVD) 起着关键性的作用。
按照《体外诊断试剂注册管理办法》所述,体外诊断试剂分为第一类,第二类,第三类。不同级别的体外诊断试剂风险程度不同,第三类最高。
国家食品药品监督管理总局2014年发布了《YYT 1244-2014 体外诊断试剂用纯化水》 ,明确指出医药行业中体外诊断试剂对于使用纯化水的要求:
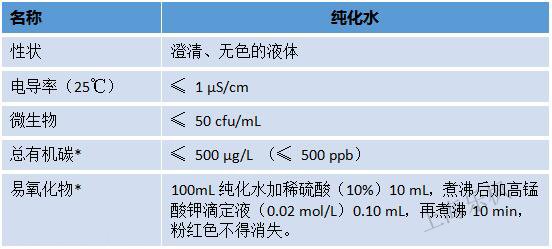
* 总有机碳和易氧化物择一检测
体外诊断试剂用纯化水相当于国标GB6682的几级水?
从水质来看,体外诊断试剂用纯化水相当于国标GB6682的二级水。
对于一些有特殊要求的试剂生产,纯化水的水质应该有更高的要求。例如分子生物学试剂对DNAse、RNAse、热原就有很高的要求。
与中国药典(2015版)的指标相比,体外诊断试剂用纯化水有哪些不同?
1、检测项目大幅减少
YY/T1244-2014标准较《中国药典》(2015版)减少了6个项目(pH、硝酸盐亚硝酸盐、氨、不挥发物、重金属)。这些减少的项目除了酸碱度使用pH计测量之外,其他项目均采用目测比色的方法,对于非药品生产企业,特别是IVD企业来说,日常实验室配制溶液、比色分析的试验能力与专业的药物分析实验室相距甚远,这样的大幅度删减检测项目的做法,无疑对IVD生产企业来说是利好消息。
2、对于氧化物的检测方法不同
YY/T 1244-2014标准中规定总有机碳和易氧化物任选其一。而《中国药典》(2015版)规定总有机碳的检测方法应使用总有机碳测定仪。
3、电导率要求不同
经过换算后,我们确认YY/T1244-2014规定的纯化水电导率(25℃)≤ 1 μS/cm;而《中国药典》(2015版)规定的纯化水电导率(25℃)≤ 5.1 μS/cm。前者相当于国标GB6682的二级水,后者相当于三级水。YY/T1244的电导率要求更高。
4、微生物要求不同
YY/T 1244-2014规定微生物≤ 50 cfu/mL;《中国药典》(2015版)规定:微生物≤ 100 cfu/mL。YY/T1244的微生物要求更高。
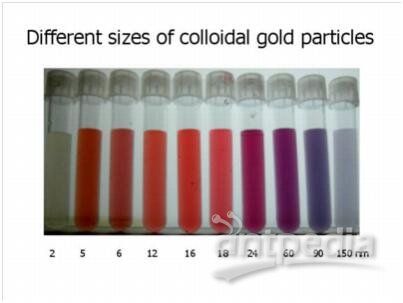
对于胶体金的制作,应该使用什么样的纯水?
胶体金是由氯金酸在还原剂(如白磷、抗坏血酸、枸橼酸钠等)作用下,聚合成特定大小的金颗粒,并由静电作用成为一种稳定的胶体状态。
离子会改变pH值及离子强度。pH值对最终的颗粒大小有一定的影响。溶液的颜色和其pH值相关联。离子强度影响胶体金与蛋白质的成功结合,或导致胶体金粒子的凝聚,降低胶体金的检测能力。
有机物除了可能改变pH值外,还会与蛋白质形成结合体。或者不稳定容易失活,或者影响探针的灵敏度。干扰蛋白-金复合体的制备。
颗粒会干扰胶体金颗粒的生成,形成的颗粒大小不一,颜色微红、无色或混浊不透明。
因此,制备胶体金务必使用低离子含量、低TOC、无颗粒的纯水。
体外诊断试剂对纯化水厂商有什么要求?
按照《体外诊断试剂生产实施细则》所述,制水设备应当满足水质要求并通过验证。所以,纯水设备生产厂家必须提供3Q验证服务,帮助体外诊断试剂生产厂家通过GMP验证。乐枫可以为用户提供中英文双语的验证手册和服务,高品质的技术和维护支持,确保您用水无忧。



