病例男,36岁,以“体检彩超发现腹部包块3周”为主诉入院。患者饮食睡眠尚可,无发热乏力,无腹痛腹泻,无恶心呕吐,无排便习惯改变。查体:全腹软,无压痛反跳痛,未触及包块,肝脾肋下未触及,肠鸣音正常。
彩超:腹部脐旁右侧低回声包块,直径约4.0 cm,周围肠壁增厚,提示恶性不除外。3周后复查超声脐旁右侧低回声包块较前无明显变化。全腹增强CT提示:右下腹肠系膜肿块,类圆形,大小约3.3 cm×3.0 cm,密度尚均匀,平均CT值约29HU;增强扫描动脉期病灶呈轻度强化,CT值约40HU;静脉期肿块仍可见强化,CT值约43HU,中央可见小片状稍低强化影;考虑淋巴源性(Castleman病)可能性大。
PET/CT检查:提示L5椎体水平右下腹肠系膜间隙3.5 cm×3.1 cm包块,边缘光整,FDG代谢轻度摄取(SUVmax=3.96),考虑良性病变可能性大。遂行肠系膜肿物切除术,术后病理:(肠系膜)神经鞘瘤,瘤细胞梭形,束状排列。免疫组化:S-100(+);CD117(-);Dog1(-);Desmin(-);SMA(-);CD34(-);Ki-67(3%+)。

图1 平扫CT示肠系膜类圆形软组织肿块,平均CT值约29HU,边界清晰,密度尚均匀。
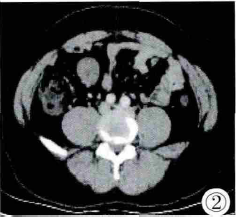
图2 增强CT动脉期示肿块轻度强化,CT值约40HU。
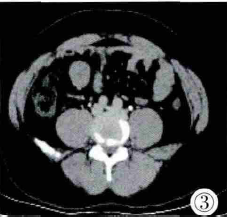
图3 增强CT静脉期示肿块仍强化,CT值约43HU,中央可见小片状稍低强化影。
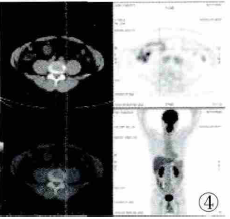
图4 PET/CT显像示肠系膜肿块FDG代谢轻度摄取,SUVmax=3.96。
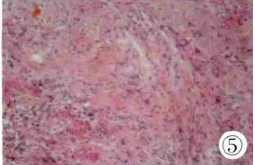
图5 病理学检查,瘤细胞梭形,束状排列(HE染色)。
讨论
神经鞘瘤又称施旺细胞瘤,是一种来源于神经鞘的肿瘤。神经鞘瘤多见于头颈部、四肢、纵隔及腹膜后,起源于肠系膜的神经鞘瘤极为少见。患者多见于20~50岁,肿瘤生长缓慢,绝大多数为良性,多为类圆形软组织肿块,有包膜,内部可发生囊变、坏死及钙化等,90%为单发。患者多无临床症状,体检发现,肿瘤较大者可对邻近组织、器官压迫,引起相应症状(腹胀、肠梗阻等)。
肠系膜神经鞘瘤可见于腹腔内任意位置,Tang等对13例肠系膜神经鞘瘤汇总分析,其中位于结肠4例,小肠3例,盲肠2例,胃2例,直肠及阑尾各1例。恶性神经鞘瘤极少,但一般认为这种肿瘤开始即为恶性,而不是由良性的神经鞘瘤转变而来。恶性肠系膜神经鞘瘤可包绕、侵及肠管、淋巴结及血管,出现腹腔积液,甚至可发生肝、肺转移。影像学上,超声可探及肿块位置、形态、与邻近组织器官关系,肠系膜神经鞘瘤多为边界清晰的低回声包块。CT可以更清晰的显示肿块的特征,对肿块进行三维定位,为术前作好评估;增强扫描肿块多为轻度或中度强化,发生囊变部分不强化。
MR在显示肿块范围和囊变、坏死方面优于CT。神经鞘瘤在T1加权像上呈低或等信号;在T2加权像上,肿块的信号与组织成分有关,实性部分呈低或等信号,发生囊变、坏死部分呈高信号;增强扫描囊变、坏死部分不强化,实性部分可呈明显强化。PET/CT可显示肿块的代谢情况,肿块可呈轻度或中度的FDG摄取。对于恶性神经鞘瘤,PET/CT不仅可显示肿块放射性浓聚情况,也可发现早期的淋巴结转移和远处转移。
尽管各种影像学检查可对肠系膜神经鞘瘤的大小、形态及周围侵及情况进行显示,但都缺乏特异性,难以做出准确诊断。组织学上,神经鞘瘤由两个部分组成:AntoniA区(细胞成分)和AntoniB区(黏液成分)。AntoniA区由致密的梭形细胞组成,密度较高;AntoniB区细胞稀疏,细胞呈多形性,囊变是主要形式。免疫组化S-100蛋白阳性对神经鞘瘤具有较高的诊断价值。
总之,肠系膜神经鞘瘤是一种起源于施旺细胞的罕见肿瘤,由于缺乏特异的临床及影像学特征,常规的影像学检查较难与其他肿瘤鉴别。目前,肠系膜神经鞘瘤的确诊仍然依靠术后的组织病理学检查,但对于明确肿瘤位置、初步判断良恶性以及术前评估、术后随访,影像学检查仍然作为首选。