导读
根据世界卫生组织及国家食品药品监督管理局的相关规定,新疫苗在申请生产批件之前,需开展批间一致性研究,以验证疫苗生产过程的一致性。疫苗颗粒粒径和分布会随着生产工艺、保存和运输条件的改变而变化,从而在不同程度上影响疫苗的批间一致性,严重时影响疫苗的安全性和有效性。传统的疫苗批间一致性研究主要通过临床试验来评价疫苗的免疫原性和安全性,对疫苗颗粒粒径和分布的批间一致性研究甚少。
岛津疫苗行业组以蛋白类疫苗为例,使用岛津激光粒仪(如图1)建立了疫苗颗粒粒径和分布测定方法,并将该法用于疫苗颗粒批间一致性评价。该方法测定范围宽,一次测定覆盖了疫苗颗粒粒径全范围,数据完整性好。

图1 岛津激光粒度仪SALD-7500nano
01
疫苗颗粒粒径测定
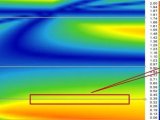
使用岛津激光粒度仪SALD-7500nano检测同厂家不同批次疫苗颗粒粒径和分布,使用Wing SALDⅡ软件采集散射衍射光光强数据,根据光强数据换算得出颗粒粒径大小和分布数据。共测定四批次疫苗颗粒粒径,测定结果叠加图如图2所示。

图2 四批次疫苗颗粒大小和分布叠加图(疫苗批次号为代称号)
02
疫苗颗粒批次一致性评价
从不同批次疫苗颗粒分布叠加图来看,C-2和C-4两批次疫苗颗粒分布比较一致,C-3批次疫苗颗粒分布略小,而C-1批次疫苗颗粒分布偏大。
同时,C-1批次疫苗颗粒中值粒径D50为8.7 μm(表1),较其它批次偏大;C-2、C-3和C-4批次疫苗颗粒中值粒径比较接近,分别为6.1 μm、5.1 μm和6.4 μm。C-2、C-3和C-4三批次疫苗颗粒D50值的变异系数CV为11.5%,C-1、C-2、C-3和C-4四批次疫苗颗粒D50值的变异系数CV为23.3%,C-1批次疫苗导致变异系数CV成倍数增加,说明C1批次疫苗颗粒一致性较其它批次相对较差。
表1 不同批次疫苗颗粒D50值
疫苗批次
D50(μm)
颗粒范围(μm)
C-1
8.74
0.67~101
C-2
6.09
0.67~61.1
C-3
5.12
0.59~44.6
C-4
6.42
0.59~62.4
备注:D50(中值粒径)指颗粒累积体积百分含量达到50%时所对应的粒径值。
撰稿人:黄小艳