
蛋白质糖基化是蛋白翻译后修饰(PTM)中最常见、结构最多样的一种修饰形式,对于维持糖蛋白的正常结构和功能发挥重要作用。目前,在已经上市的生物技术药物中有60%以上是糖蛋白,它们主要由哺乳动物细胞表达,如抗体、重组激素和酶等。糖基通过共价键与蛋白质中特定的氨基酸残基连接,有些已经被列入相应药物的关键质量属性。
蛋白质糖谱分析不是一项简单的工作,它涉及到复杂的N -糖和O-糖分子的识别,而这些糖分子的结构往往非常相似。大量经验与实例表明,亲水相互作用液相色谱法(HILIC)是一种成熟的分离和定量聚糖的分析方法。
一般当我们需要分离具有相同单糖单元的聚糖、或脱酰胺化的多肽及氧化的scFc’s等,无疑都需要更高的柱效和选择性。Phenomenex公司的专用的Biozen色谱柱系列,将两种高效的基本颗粒技术结合到一起,一种是我们高柱效的核-壳颗粒,这种技术在小分子领域已经取得了较大的成功,另一种是我们全新的全多孔和高惰性热改性颗粒。
高效、可扩展的核-壳颗粒平台

全多孔、高惰性的热改性颗粒平台

生物惰性钛硬件,提高回收率和重现性

这里,我们来介绍N-糖链分析流程
可以使用几种不同的方法来鉴定糖型,例如高分辨率精确质谱、糖肽图谱和HILIC色谱法。我们将专门讨论N-糖链释放,及随后的荧光标记和HILIC分析。
步骤1
用PNGase F去糖基化
PNGase F是从脑膜炎败血黄杆菌中分离的“内切糖苷酶”
可在大肠杆菌 (N-Glycanase®) 中重组表达
切割各种N-连接糖链(双、三和四触角、高甘露糖型和杂合型)最内侧的 GlcNac
岩藻糖基化核心除外,而不是α(1-6)[即在植物和细菌中发现的α(1-3)]
在大多数 pH 条件下稳定(最佳 8.6);洗涤剂有帮助,但非必要。
步骤2
还原胺化法进行荧光标记
因为聚糖没有发色团,并且因为通常没有足够充分的量来运行 ELSD 或其它通用检测器,所以聚糖必须用荧光团标记以被检测。最常见的是 2-氨基苯甲酰胺或 2-AB。简而言之,聚糖是还原糖,在环状(典型闭环)和“无环”(开环)形式之间平衡存在。伯胺基团可以与无环形式的羰基碳反应-这形成希夫碱,然后用氰基硼氢化钠还原。
在标记之前,必须干燥每个聚糖样品,因为标记是在 DMSO 和乙酸中进行的。
步骤3
荧光染料清除
最常用的是 HILIC 固相萃取-96孔板或小柱形式。因为这是 HILIC,所以在水相缓冲液中洗脱。因此微96孔洗脱板是最佳选择。
步骤4
HILIC色谱分析

上图看到的是“人类 IgG 聚糖”库图谱。主要是在人血清(同种型混合物)和它们各自的糖链异质体中发现的所有 IgG。Man5 和 Man6 聚糖被加标以显示这些通常难以分开的聚糖的选择性。
另外注意到,除了高甘露糖聚糖之外,聚糖几乎完全是中性、复合型和双触角聚糖,尽管有少量的唾液酸化聚糖 (G0F + SA) 和 (G1F + SA)。


HILIC用于荧光标记的N-连接糖链分析


在HILIC模式下,主要依靠氢键、偶极-偶极和静电相互作用!
一般来说,聚糖按亲水性顺序洗脱- 具体来说,是由单糖残基的数量决定的。由于部分形状选择性,高甘露糖聚糖(例如 man 5)可以不同于 G0(两者都具有8个单糖残基)洗脱。此外,唾液酸化的聚糖 - 带负电荷 - 可能具有弱静电相互作用,因此洗脱得更晚。
选择性明显不同于RP-LC
极性化合物在高有机相比例下进行保留
乙腈等非质子溶剂是首选
缓冲液是强溶剂- 醋酸铵或甲酸铵最常见
bioZen Glycan的特点总结:
它使用一个核-壳颗粒,因此在使用较短的色谱柱也能获得高柱效。
酰胺多元醇不仅有标准的氢键,还具备受氢选择性。此外,bioZen Glycan上的形态选择性大不相同,所以聚糖的洗脱顺序会与其它酰胺色谱柱不同。
还要注意的是有部分静电荷,这也有助于唾液酸化聚糖的分析。



2-AB标记的人类IgG聚糖库,
使用Man5和Man6加标



这里我们可以看到人类 IgG 聚糖库的 bioZen 聚糖图谱;基本上是已经去糖基化的多克隆 IgG。然后,多种聚糖被标记为 2-AB。此外,我们在 Man5 和 Man6 中增加了更具代表性的可能具有未成熟聚糖重组表达的蛋白质;例如在 CHO 中是常见的蛋白质。
比较相对于标准亚-2µm 酰胺的选择性,biozen Glycan可以将高甘露聚糖从其他双触角聚糖上洗脱下来。


另外,两种正交方法也可对糖型进行鉴别
糖肽图谱
使用高分辨率精确质谱分析完整质量数
第一种方法是糖肽图谱。这需要纯化、分离的糖蛋白(这里是 mAb),然后基本上执行与用丝氨酸蛋白酶,如胰蛋白酶酶解的肽图相同的方法,然后通过反相或 HILIC 来鉴定糖链异质体。这种方法可能是首选,因为您可以确认位点占用率 - 或糖基化的确切位点。
虽然糖肽以相似的保留时间洗脱,但我们仍然可以测定糖链异质体的相对量。注意源内裂解(即–GlcNac 和 HexNac)会使相对丰度复杂化。
注:肽图使用的是biozen peptide XB-C18 产生的数据。

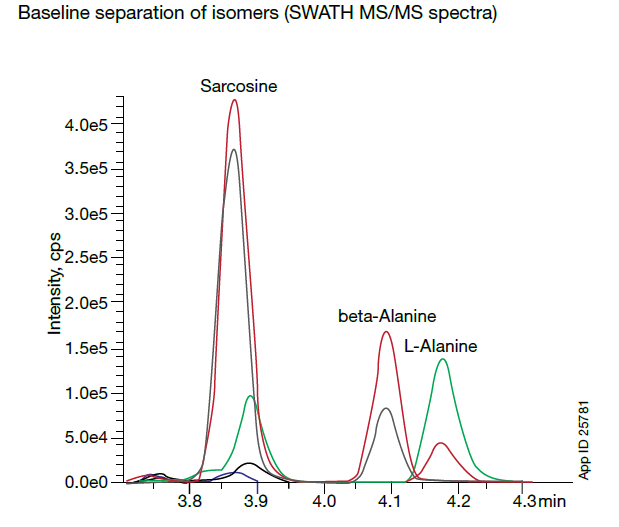
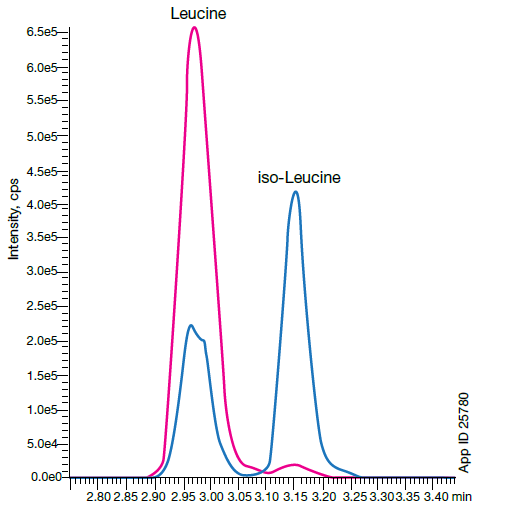
应用案例:细胞培养基质中38种氨基酸的非衍生化定量分析(bioZen 2.6 μm Glycan, 100 x 2.1 mm, 00D-4773-AN)
本应用案例中,在LC-MS/MS上开发了细胞培养基质中38种氨基酸的非衍生化定量分析方法。由下图展示可知,HILIC色谱柱上极性大的氨基酸保留和异构体的分离佳,日间与日内重复测试、不同进样体积、不同批次等各种条件下分析结果稳定。bioZen Glycan非常适合分离非衍生氨基酸的色谱柱。


应用案例:使用bioZen™亲水作用(HILIC)色谱法与固相萃取法定量测定糖蛋白的中性聚糖和唾液酸化聚糖
已建立的糖基化糖蛋白表征方法使用PNGase F消化过程之后再通过HPLC-UV或LC-MS/MS进行N-聚糖标记和相对定量。传统的样品制备过程中要进行密集操作,同时出现了样品损失,但使用如bioZen N-Glycan Clean-up等HILIC固相萃取(SPE)提取板,得到的结果灵敏、有效、节省时间。HILIC SPE的亲水性相互作用是一个值得关注的问题,而唾液酸化聚糖尤其难以通过HILIC SPE进行优化,这是因为唾液酸化聚糖的极性比其他荧光标记的聚糖的极性更强。
聚糖工作流程如下图所示。
在这项研究中,我们荧光标记和回收了N-连接聚糖释放的血清衍生α-1酸性糖蛋白(AGP)。该模型蛋白是一种具有多触角、含有中性聚糖和唾液酸化聚糖的、复杂、高度唾液酸化的糖蛋白的合适替代物。


Biozen N-聚糖分析工作流程


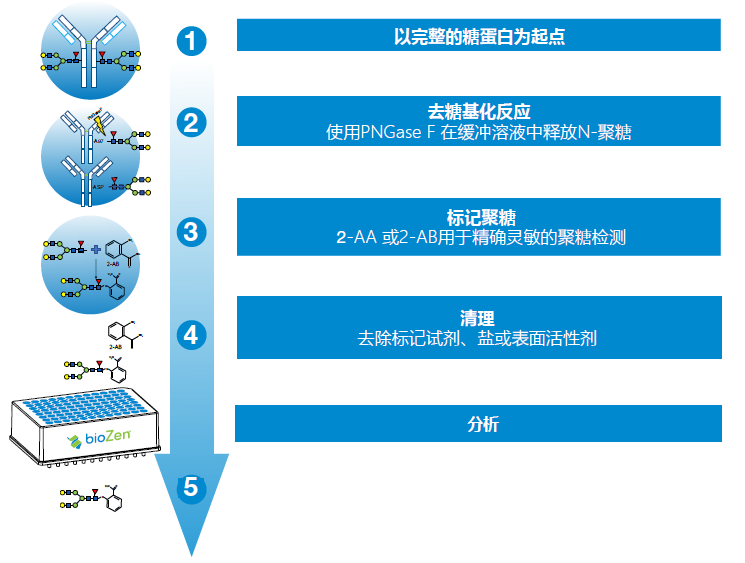

图:由AGP产生的标记聚糖
Trisialylated | 三唾液酸化聚糖 |
Disialylated | 二唾液酸化聚糖 |
Monosialylated | 单唾液酸化聚糖 |
Tetrasialylated | 四唾液酸化聚糖 |
唾液酸化聚糖的分离和鉴定是一个挑战性的任务,因为它们最多可以有四个触角,四个触角上带有四种唾液酸。必须将流动相A(即HILIC中的强溶剂)中50 mM甲酸铵的一般浓度增加至250 mM才能获得最佳的色谱效果。调整梯度和改变流动相后,从聚糖中分离出中性唾液酸化聚糖、单唾液酸化聚糖、双唾液酸化聚糖、四唾液酸化聚糖以及唾液酸化的几种归属。
结 论
bioZen™ N-聚糖净化板和bioZen Glycan 色谱柱柱可以有效分析荧光标记的N-连接聚糖。这种分析方法对唾液酸化聚糖特别有效,使用新型酰胺多元醇固定相,中性、双触角聚糖和高度支化、唾液酸化聚糖都可以使用优化的梯度和条件进行分离
核-壳颗粒可用于聚糖的快速筛查方法
产品订购信息


参考文献:
1.Fukuda MN, Sasaki H, Lopez L, Fukuda M. Survival of recombinant erythro¬protin in the circulation: the role of carbohydrates. Blood. 1989;73:84-9
2.Reusch D, Tejada ML. Fc glycans of therapeutic antibodies as critical quality attributes. Glycobiology. 2015;25:1325-1334
3.Hermentin, Peter, et al. “The Hypothetical N-Glycan Charge: a Number That Characterizes Protein Glycosylation.” Glycobiology, vol. 6, no. 2, 1996, pp. 217-230., doi:10.1093/glycob/6.2.217.
