
2023 版美国药典《mRNA 疫苗质量分析方法 - 指南草案》简介

美国药典(USP)标准历来被认为是一种重要的公共医药工具,2022 年 2 月 USP 在官网发布了第一版 mRNA 疫苗质量分析方法,主要围绕 mRNA 药物原料药,为整个行业提供了巨大的技术支持。
2023 年 4 月,USP 重磅更新了新的一版《mRNA 疫苗质量分析方法-指南草案》(后文简称“2023 版草案”),2023 版草案从整个 mRNA 疫苗产品的全生命周期出发,主要内容包括:
1
Proposed testing for plasmid DNA prior to release
质粒 DNA 质量属性的测试
2
Characterization and release testing for mRNA Drug Substance
mRNA 药物原料的表征和放行测试
3
Characterization and release testing for mRNA Drug Product
mRNA 药物制剂的表征与放行测试
2023 版本草案新增了多项高效液相色谱(HPLC)、液质联用(LC - MS)以及基于微孔板的检测方法,本文重点为大家解析草案中涉及的微孔板检测项目及方法。

mRNA 药物的生产工艺和测试
2023版草案指出:mRNA 药物原料和药物产品的质量,由原料和产品的设计、开发和在开发和生产过程中应用的标准决定。指南分别就以上各阶段给出了推荐的放行检测项目:

《mRNA 疫苗质量分析方法-指南草案》第二版主要新增项目
小编汇总了“2023 版草案”中 mRNA 疫苗不同阶段中所涉及的所有基于微孔板水平的检测项目及方法,以及安捷伦可以提供的检测设备推荐方案:

1
UV 法核酸定量
“2023 版草案”中的质粒 DNA 放行检测及 mRNA 药物的原料药表征和放行检测中均提到了 UV 法对质粒 DNA 及 RNA 进行浓度测定,UV 法的优势是操作简便,无需额外的试剂。
检测原理:核酸的嘌呤和嘧啶环含有共轭双键,在 260 nm 左右的紫外光有较强的吸收;根据 Beer - Lambert 方程,通过测量 260 nm 的吸光值可计算出 DNA、RNA、寡聚核苷酸的浓度。
在 260 nm 和 1 cm 光路经下 1 OD 值相当于:
• 50 μg/mL 双螺旋 DNA(质粒)
• 40 μg/mL 单螺旋 DNA(RNA)
• 20 μg/mL 寡核苷酸
260/280 的比值用于评估样品的纯度,纯的 DNA A260/280 比值为 1.8,纯的 RNA A260/280 比值为 2.0,样品中如含有杂蛋白及苯酚,A260/A280 比值即明显降低。
应用方案 1:使用高通量微量检测板(例如 Take3 板)配合多功能酶标仪,可开展多通量体积低至 2 μL 的核酸定量检测,检测限低达 2 ng/μL。

Epoch + Take 3 微量检测板
• 2 μl的核酸/蛋白定量
• 快速检测 16/48 个样本
• 操作及维护保养方便
应用方案 2:采用 96 或 384 体系的 UV 可透过微孔板,配合多功能酶标仪,进行高通量核酸定量检测。这个方案相对于微量检测板,样本消耗量较大,但通量更高。并且需要仪器软件带有自动光程矫正的算法。

Epoch + 96/384 UV 微孔板
• 高通量核酸定量
• 内嵌光路校准程序
2
ELISA 法残留项目检测
mRNA 疫苗整个生命周期的生产流程中,有多项残留项目检测,包括质粒 DNA 放行阶段的宿主细胞残留检测、卡那霉素残留检测;mRNA 原料阶段的 dsRNA 检测、T7 聚合酶检测等,这些检测项目的共同点都是采用经典的酶联免疫吸附法(ELISA)进行测定。
ELISA 的检测原理:ELISA 可以说是一种历史悠久,使用场景极为丰富的检测方法,核心原理是抗原与抗体免疫学反应,具有特异性。将一定浓度的抗原或者抗体通过物理吸附的方法固定于微孔板表面,加入待检标本,通过酶标物显色的深浅间接反映被测物的浓度,由于酶标记可以催化底物分子发生反应,产生放大作用,使 ELISA 具有很高的敏感性。
ELISA 的实验设计有很多,主要包括间接法、 双抗原/抗体夹心法和抗原竞争法等,根据待测物的特点选择其合适的 ELISA 方法,例如 2023 指南中涉及的几种检测项目:
HCP 检测:推荐采用夹心 ELISA 法,目前ELISA 检测法仍然是生物制品 HCP 检测的金标准,有非常多的市售商品试剂盒可选,包括大肠埃希菌残留蛋白检测、酵母工程菌体残留蛋白检测、假单胞菌菌体残留蛋白检测、CHO 细胞残留蛋白检测等。
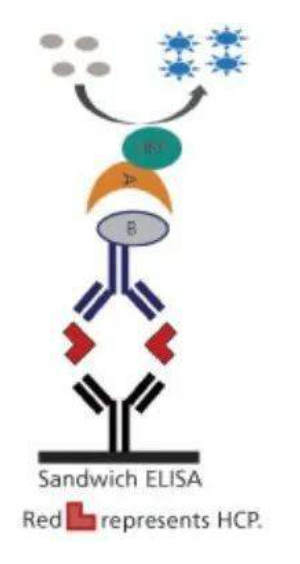
夹心ELISA原理示意图
卡那霉素残留检测:推荐采用间接竞争 ELISA 检测,具有简便、准确,灵敏度高,和操作时间短等特点。有文献表明,采用该方法的回收率达到 90% ,对卡那霉素的有效检测范围为 0.5 ~ 40.5 ng·mL-1,标准曲线相关系数 r = 0.9996,RSD 小于 10%。

间接竞争 ELISA 原理示意图
T7 聚合酶残留检测:推荐使用双抗体夹心 ELISA 法。mRNA 规模化生产过程中主要涉及的工具酶有 T7 RNA Polymerase、Dnase Ⅰ、RNA Inhibitor、Pyrophosphatase Inorganic 等,工具酶本身对于药物成品来说亦是一种杂质,这些杂质与 mRNA 一起通过 LNP 包封进入细胞释放后,极有可能产生高强度的免疫原性从而连带引发 mRNA 的降解。USP 及我国 CDE 颁布的指南中均指出需要对生产工艺产生的杂质进行监测分析。目前市售商品 T7 聚合酶检测试剂盒的灵敏度可达 2 ng/mL,检测范围:4-256 ng/mL。
dsRNA 检测:推荐使用双抗体夹心 ELISA,检测核酸提取物中的病毒 dsRNA 或非病毒来源的天然或合成 dsRNA,以及检测人工合成(m)RNA 制剂中的 dsRNA 杂质。采用该方法有高度特异性,不会受到 ssDNA、RNA、蛋白影响,检测范围:30-40 pg/mL 至 3ng/mL。
3
mRNA - LNP 包封率检测
包封率是 mRNA 载药体非常关键的指标,表示包裹在脂质纳米颗粒内部的 RNA 占全部 RNA 的比例,是确定 LNP 药物制剂精确给药剂量的基础,这个指标广泛应用于 LNP 早期开发及后期生产质控中。
包封率的测定方法:2023 版草案推荐采用基于 RiboGreen 的荧光检测。其原理是:当 RiboGreen 特异性插入核酸后,能够发出绿色荧光,可用于定量溶液中的 RNA,检测下限可以低至 1 ng/ml,使用 96 孔板检测时,每孔 200 uL 样品中可以检测到 200 pg RNA,并且具有特异性好,线性范围宽等优势。
主要检测流程:包括 buffer 和 LNP 样本制备、 96 孔板样本及标准品加样、加入 triton 孵育破乳、加入 RiboGreen 试剂(以上和各种液体孔板打交道的工作,都可以交给自动化移液工作站完成,比如安捷伦的 Bravo),最终送入BioTek Synergy 高通量酶标仪,调取现有方案,一键开始荧光强度读数,最快只需数十秒即可完成检测。
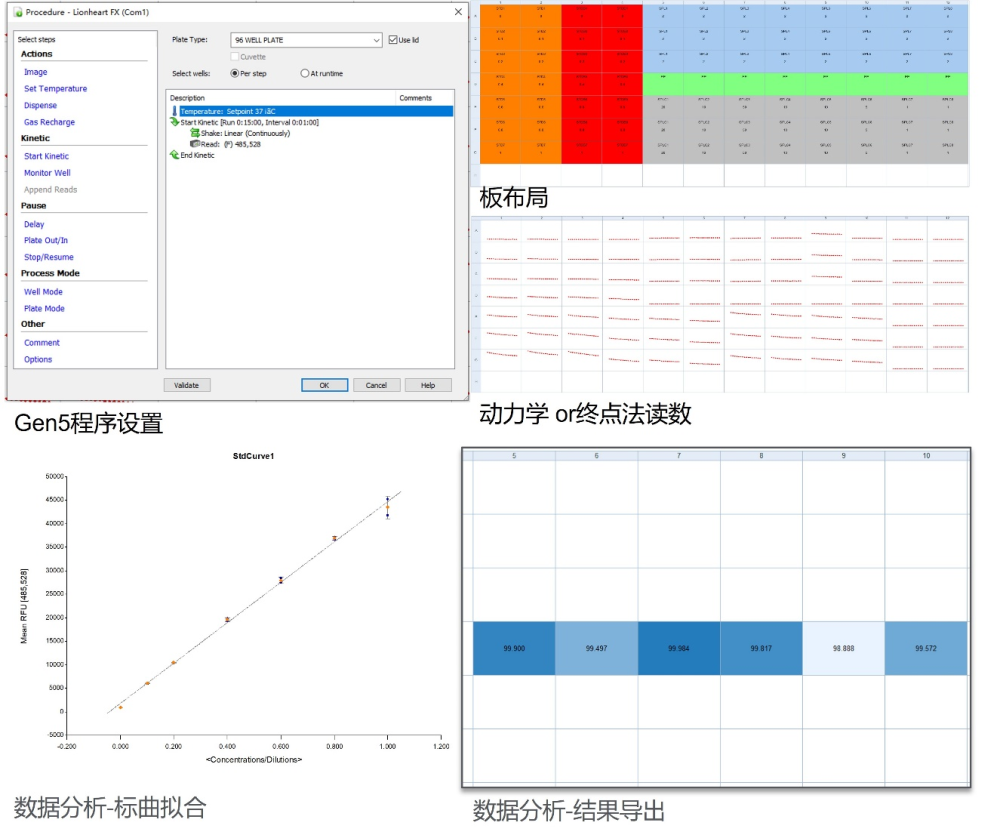
Gen5 软件可实现 LNP 包封率检测程序设置、板布局、原始数据及数据分析一站式方案
4
mRNA 生物学效力检测:基于细胞的蛋白表达分析
在 2023 版草案中,对于 mRNA 原料和 mRNA 制剂推荐采用 Cell-based assay 评价 mRNA 疫苗的效力,相对于传统的动物实验,这种体外细胞学水平的评价经济快捷,标准化程度高,并且非常适合开展高通量自动化操作。
主要检测原理:通过对 mRNA 及 mRNA-LNP 转染细胞中表达蛋白的功能结合试验,可以证明 mRNA-LNP 的效力(以确认 mRNA 分子的完整性,并证明表达蛋白的关键表位)。对于特定产品的 mRNA 编码蛋白的评价可以通过 ELISA 法,检测细胞水平的蛋白表达,以及表达蛋白的结合功能评价。
主要检测流程示意图如下:

USP 指南中使用 HepG2 细胞进行细胞表达,可以使用其他细胞系或方法。
5
内毒素检测
内毒素/酯多糖(LPS)是革兰氏阴性菌细胞壁外膜外侧的一种结构成分,被发现广泛分布,覆盖约 75% 外膜表面。可触发高热、败血性休克等严重的生理反应,对于药品放行,内毒素是必检项目。在 mRNA 疫苗生产流程中多项环节都有此检测项目,2023 版草案中推荐的内毒素检测方法是参考 USP <85> 中的鲎试剂检测法(中国药典(ChP)1143 细菌内毒素检查法同样是鲎试剂法),其中包括三种类型的检测方法:
凝胶法:鲎试剂与内毒素产生凝集反应的原理进行限度检测或半定量检测内毒素的方法。
动态浊度法:鲎试剂与内毒素反应过程中浊度变化而测定的内毒素含量变化方法。
动态显色法:检测鲎试剂与内毒素反应过程中产生的凝固酶使特定底物释放出的呈色团的多少而测定内毒素含量的方法。
另外,目前基于重组 c 因子的内毒素检测方法也越来越多受到关注,关于内毒素的详细应用案例,我们后续会有专题报道。

上图:细菌内毒素检测鲎试剂法的主要检测原理
最后,整体推荐方案时间到
安捷伦 mRNA 疫苗质量控制微孔板检测方案推荐

特别推荐:高通量 Cell based assay 一站式解决方案

USP 疫苗质量控制指导原则中,推荐使用 Cell-based assay 开展 mRNA 原液和制剂的放行检测,其中涉及大量细胞铺板、洗板、孵育和检测的步骤,BioSpa8 平台可根据客户需要灵活搭建自动化的细胞检测平台。

关于 BioTek
BioTek 是世界领先的多功能微孔板检测仪及软件的研发生产公司,拥有 54 年的悠久历史。BioTek 的 Synergy 系列多功能微孔板检测仪拥有灵活的功能配置和优异的检测结果,配合友好强大的操作软件,为广大用户提供了便捷高效的使用体验。服务科学,促进科学始终是我们追求的目标。2019 年 BioTek 加入安捷伦科技有限公司,成为细胞分析事业部的重要组成成员。
关于安捷伦
安捷伦科技有限公司(纽约证交所:A)是生命科学、诊断和应用化学市场领域的全球领导者,致力于为提升人类生活品质提供敏锐洞察和创新经验。安捷伦的仪器、软件、服务、解决方案和专家能够为客户最具挑战性的难题提供更可靠的答案。2022 财年,安捷伦营业收入为 68.5 亿美元,全球员工数约为 18,000 人。

长按识别二维码,关注安捷伦细胞分析