演讲主题
医学基因组联盟:罕见病基因组测序的最佳实践开发
当实验室要开展遗传检测时,诊断力也许是最受关注的话题了。Marshall教授开篇从诊断入手,常规的遗传实验室检测手段通常获得19%左右的平均诊断力,但全基因组测序(WGS)的诊断力约能达到41%。当然额外检出的部分,多数来源于“原方案未覆盖”的基因,也有非编码区域和拷贝数异常等这类“原技术未能检测”的区域,总体相对于WES或Array芯片,WGS的额外检出率大约10%,相当于将多种技术集成合一。这也解释了为什么近年间,WGS临床应用方向逐步扩展,在一些研究中已被当成一线手段提升诊断效力。
也正因这样的时代背景,不同的学会及协会如基因健康全球联盟,ClinGen,CSER等均有整理相关的最佳实践,但是,这些学会的前期工作并不限定于临床全基因组测序的标准操作,这也推动了医学基因组联盟(Medical Genome Initiative)在2019年的成立,大家的共同目标是发现目前临床基因组测序应用的空白并整理共识去填补空白。
医学基因组联盟的使命
通过发表常规实验室里的最佳实践,扩展高质量临床基因组测序用于罕见未确诊遗传病诊断的可及性。
联盟的两个发起目标
建立并发表实验室&临床的最佳实践,从而推动基因组测序应用于罕见病诊断
联合临床研究协作组衡量全基因组测序的临床及经济学效用
联盟的架构
由九个平等参与的成员机构组成的联合指导委员会,共同商定项目和分配资源。为稿件撰写和其他项目组建工作小组,Illumina作为成员机构之一,提供了科学贡献,管理协助与资源赞助。
医学基因组联盟小组在2019年二月发表了第一篇最佳实践[1],迈出了以临床基因组测序为核心的指南推动的第一步,同时展示了联盟中的不同工作小组及成员们的阶段目标,分析验证,解读报告,临床效用等等热点话题都设定了产出成果的计划。
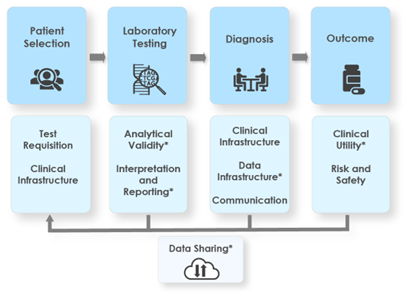
Marshall教授还详细解释了一个优质的专家共识产出的工作流程步骤与注意事项:
首先确定主题,我们觉得这个主题一定满足很多患者的需求,确定主题之后我们再确定指导委员会和主要作者。协作机构中的同仁们都可参与,组成核心团队,或者说是内容贡献者。
然后成员们确定工作范围、定义大纲,工作组内共享机制,还会设定一些后续的在线调研和公开讨论,对项目进行绘制,并且进行相关同行审查和修订。
完成了同行审查和修订之后,再经过指导委员会的审查,最终提交期刊或者形成整个一个诊疗白皮书或者指南。
已发布的三篇有关分析验证[2]、报告解读[3]和WGS临床效能[4]的最佳实践文章值得同道们学习,当联盟成员组在整理这些共识时,投入了大量时间和精力,因为此前并没有类似的工作,需要积累各种研究证据。
基因组的分析验证最佳实践[2]:
对想开展临床全基因组测序的实验室主管很有教学意义
对现有推荐的实验计划,实验验证及质量管理进行了操作调研
对几个关键点形成共识标准。
关于全基因组测序的质量验证关键流程应该如下图一般是个完整的闭环:

建议在每个不同的病例之中,找到相关的关键要素并进行管理。这些工作要素可能关联不同的验证。而最后的结果分析以及进一步的确定结果的过程,将矫正测试的准确性。这样的质量管理是非常重要的,是一个完整闭环,需要不断重复这样的流程从而优化基因组测序的检测质量。
对于测序深度,Marshall教授也给出了联盟中的建议,人们常觉得全基因组测序的覆盖度要达到35-40x,事实上这是一个动态变化的参数,刚开始建立实验标准的时候,40x确实比较推荐。但后来,随着不断更新的算法和基因组覆盖范围,WGS的灵敏度将不断提高,随之测序深度的减少也将节约成本。例如,当二级分析工具DRAGEN 升级至3.10.8后,较低的测序深度也可适配变异检测的高灵敏度。
医学基因组联盟在后续的工作计划中还包括由不同小组成员领衔的:临床表型患者选择最佳实践;数据架构与管理的最佳实践。团队也希望能快速针对疾病的变化作出反应,更灵活地了解临床需求,从而提出更合时宜的最佳实践。
Marshall教授提到一个有意思的概念,即“基因组测序的边界是什么?”,这个“边界”可能因实验室而异,也可能因国别而异。比如在美国,工作边界就是WGS是复杂的,临床医生们很难理解,时常会有一些临床意义不明(VUS)的测序结果成为医生们的工作障碍。而联盟小组的责任就是帮助缓和测序与临床的“边界”。对于VUS,刚刚发表的一篇最佳实践指南将尽可能解决临床医生们的障碍。由Heidi教授领衔的这篇论文[5]比较了来自诊断实验室的WGS和靶向panel的VUS报告率,在几个月内收集和分析了超过150万次测试的结果,论文分析事实证明,与panel相比,基因组/外显子组的VUS率更低,这个信息意义深远,降低了医生们对基因组或外显子组测序的应用顾虑。
最后Marshall教授表示,当医学基因组联盟产出了一些成果,大家会积极让成果得以收到更多同行们的曝光与反馈,伴随发展,收集临床基因组测序应用场景中的各项障碍,并对障碍级别排序,从而评估未来临床基因组测序最有前景的应用方向,再逐步应对挑战,优化使用,这才是良性的更具有推动性的循环。
查阅Marshall教授的课程回放,您将更全面深入的理解全基因组测序相关的共识指南工作如何开展,如何惠及从业同道们,参考论文原文链接可通过附录获取。
Christian R Marshall, et al. The Medical Genome Initiative: moving whole-genome sequencing for rare disease diagnosis to the clinica.Genome Med. 2020 May 27;12(1):48.
Christian R Marshall, et al. Best practices for the analytical validation of clinical whole-genome sequencing intended for the diagnosis of germline disease. NPJ Genom Med. 2020 Oct 23;5:47.
Christina A Austin-Tse, et al. Best practices for the interpretation and reporting of clinical whole genome sequencing. NPJ Genom Med. 2022 Apr 8;7(1):27.
Robin Z Hayeems, et al. Clinical utility of genomic sequencing: a measurement toolkit. NPJ Genom Med. 2020 Dec 15;5(1):56.
Heidi L Rehm, et al. The landscape of reported VUS in multi-gene panel and genomic testing: Time for a change. Genet Med. 2023 Jul 30;100947.