
CRISPR-Cas9是应用最广泛的非病毒编辑工具之一。近几年该技术快速发展,已有一些基于该技术的细胞疗法进入临床阶段,比如用于治疗β-地中海贫血、镰状细胞病和治疗眼部疾病等的治疗。但是获得高质量、高性能且符合GMP生产规范的Cas9仍是行业一大挑战。赛默飞近期已上市Gibco CTS TrueCut Cas9 Protein,以支持行业细胞与基因编辑治疗快速发展。


1
更严格的生产标准和安全性测试
Gibco CTS TrueCut Cas9(以下简称CTS Cas9)蛋白是在GMP生产规范下制造,其生产符合细胞、基因和组织产品的辅助材料标准(包括USP<1043>、欧洲药典5.2.12和ISO 20399-1、-2和-3),并在FDA注册的生产基地遵循21 CFR第820部分的原则进行生产。除具有广泛的可追溯性文件外(COO, COA, DMF, RSF等),还对产品进行了更广泛的安全性测试(表1)。

表1:CTS TrueCut Cas9蛋白的代表性质量规范。
2
优异的产品稳定性
2.1
CTS Cas9和RNP复合物的稳定性
评估CTS Cas9和核糖核蛋白(RNP)复合物在各条件下的稳定性。首先,将CTS Cas9蛋白在一定浓度范围内进行连续稀释,然后进行5次冻融循环。与无冻融循环的对照样组相比,进行5次冻融循环后未观察到切割活性出现显著变化(图1)。此外,在不同时间点(0 min、10 min、1 h、4 h和16 h)评估RNP复合物的稳定性以模拟正常使用条件。连续稀释RNP复合物,并使用体外切割检测测定切割活性。在不同时间点未观察到对切割活性造成显著影响(图2)。

图1.CTS Cas9在5次冻融循环后保持稳定,如体外切割检测所测。(A)在一定浓度范围内对CTS Cas9进行连续稀释,并测定切割活性。将不同量(8、16、32、0 ng)的CTS Cas9与过量(40 ng)靶向HPRT基因的gRNA以及含有HPRT序列的质粒(300 ng)在37°C下孵育10分钟。(B)通过凝胶成像系统进行定量。

图2.RNP复合物在室温下的不同时间间隔保持切割活性。将不同量(8 ng、16 ng和32 ng)的CTS Cas9与过量(40 ng)靶向HPRT基因的gRNA混合,并在室温下孵育10分钟至16小时。然后将样品与含有HPRT序列的过量质粒(300 ng)在37°C下孵育10分钟。
2.2
多生产批次间的产品稳定性
为了更好的满足大规模临床生产的需求,CTS Cas9 蛋白单批次生产量高,且批次稳定性优异。对来自3个生产批次的CTS Cas9蛋白进行连续稀释,测定每个剂量下的切割活性。在T细胞靶位点未检测到批间差异(图3)。

图3.在T细胞中多个批次间CTS Cas9的性能一致。
3
优异的切割效率
为了测定Cas9的性能,我们平行测试了CTS Cas9与供应商A 的GMP级Cas9。在每项测试中,CTS Cas9的性能始终匹配或超过供应商A Cas9的性能。
3.1
体外切割效率检测
将CTS Cas9和供应商A Cas9稀释到非饱和浓度,并评估切割活性。如图4所示,两种Cas9蛋白在80 ng的高(或饱和)剂量下表现出相似的切割活性。然而,在较低剂量下,两种蛋白之间切割活性的差异开始变得显著。在48 ng和16 ng的较低剂量下,CTS Cas9的切割活性明显高于供应商A Cas9。如图,供应商A Cas9切割活性达到35%需要48 ng的剂量,而CTS Cas9只需16 ng。这些数据表明,与供应商A Cas9相比,CTS Cas9的切割活性更高。
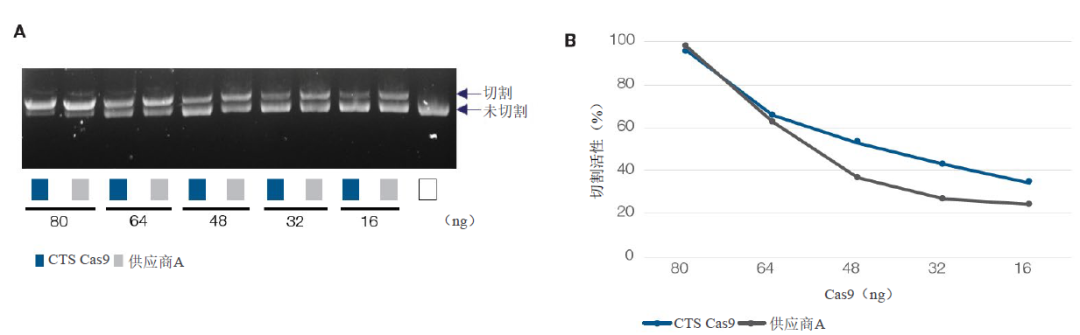
图4.在较低的蛋白剂量下,CTS Cas9的切割活性高于供应商A Cas9。将不同量的Cas9与等量的靶向HPRT基因的过量(40 ng)gRNA以及含有HPRT序列的质粒(300 ng)在37°C下孵育10分钟。(A)在饱和条件下,2种 Cas9表现出相似的切割活性。(B)随着样品被稀释,两种核酸酶之间的差异变得更加显著:在48 ng时,CTS Cas9的切割效率达到53%,而供应商A CTS达到36.5%。
3.2
基于细胞水平的Cas9效率检测
实验使用了靶向4个CAR T细胞相关治疗基因(TRAC、TRBC、PD1和CD52)的7种gRNA。分离并活化原代T细胞,然后利用Neon电转染系统和Cas9进行编辑。当选择4个靶向T细胞受体α和β(TRAC和TRBC)基因的gRNA,图5A显示了CTS Cas9的TCR KO超过88.7%,而供应商A Cas9的TCR KO达到61.7%。进一步使用NGS的靶向扩增测序确认(TAV)对基因分型变化进行了评估,从而计算4个靶标(TRAC-0、TRAC-4、TRAC-6和TRBC-1)的平均KO百分比。平均而言, CTS Cas9的敲除效率比供应商A Cas9高出20%以上,TRAC-4和TRAC-6的KO效率没有显著差异(图5B)。

图5.CTS Cas9的TCR KO效率高于供应商A Cas9。(A)TCR KO效率的流式细胞术数据示例。(B)基于NGS的TAV平均KO效率。与供应商A Cas9相比,CTS Cas9在各种靶标上达到的平均KO效率更高。所有反应均重复进行三次(**P<0.01)。
为了在基因组水平上进一步确定Cas9编辑效率,我们扩大测试范围:选择3个靶向CD52和PD1基因的gRNA(CD52-5、CD52-6和PD1-2)。结果显示,与供应商A Cas9相比,CTS Cas9与7种gRNA中的3个(TRAC-0、TRBC-1和CD52-5)达到的编辑效率更高。另外4个gRNA(TRAC-4、TRAC-6、CD52-6和PD1-2)的高编辑效率均超过80%,两种Cas9蛋白之间没有显著差异,推测是使用的试剂量(包括Cas9蛋白量)可能处于饱和状态,导致两种Cas9蛋白达到最大编辑效率(图6A)。
为了进一步探索两种Cas9蛋白之间的潜在性能差异,连续稀释两种Cas9蛋白(原始7.5 pmol;稀释度从1到1/16),在原代T细胞中对TRAC-4、TRAC-6、CD52-6和PD1-2进行功能检测。图6B所示的数据证明,当Cas9稀释度低于饱和水平时,CTS Cas9对所有4个gRNA达到的编辑效率高于供应商A Cas9。两种Cas9蛋白在性能上的差异以TRAC-6最为显著。在1/4稀释度下,供应商A Cas9的编辑效率为40%,而CTS Cas9的编辑效率为60%。总体而言,在所有靶标的不同稀释度下,CTS Cas9的切割活性比供应商A Cas9更高。

图6.在原代T细胞中,CTS Cas9的编辑效率高于供应商A Cas9。(A)将CTS Cas9或供应商A Cas9(7.5 pmol)与7.5 pmol的7个相应TrueGuide合成sgRNA混合,电转后3天进行编辑效率分析。在3个靶标(TRAC-0、TRBC-1和CD52-5)上观察到性能差异显著。(B)将稀释后的Cas9蛋白与7.5 pmol相应的TrueGuide合成sgRNA(TRAC-4、TRAC-6、PD1-2和CD52-6)混合,电转后3天进行编辑效率分析。结果提示,与供应商A Cas9相比,CTS Cas9的编辑活性相当或更高。反应以一式三份的方式进行(**P<0.01)。
结
论
赛默飞可提供高质量、高性能且符合GMP生产规范的Cas9,满足行业客户相关疗法的开发。如果您还处在项目早期或者研发阶段,我们也可推荐研究级别可用的版本。

如您需要询价、技术咨询、
资料下载等需求,请扫描下方二维码。


