腺相关病毒(adeno-associated virus, AAV)载体因其具有较好的安全性,针对各组织的良好的靶向性及感染性,已被广泛的应用于相关基因疗法的开发中,并在在多种适应症上取得了进展,包括罕见眼科疾病、β地中海贫血症、血友病、杜氏肌营养不良、肌萎缩性脊髓侧索硬化症(ALS)等。相关疗法的开发中面临的主要挑战之一是临床用AAV载体的大规模高滴度生产。
早期的AAV载体生产需要辅助病毒(如慢病毒、溶瘤病毒等)以复制产生子代病毒颗粒,但辅助病毒难以清除,易导致宿主体内产生炎症等副反应。当前AAV生产方法采用最多的就是经典的三质粒共转染法(Helper-free AAV包装系统,即无辅助病毒),FDA批准的首个治疗先天性黑朦病的基因疗法Luxturna(Spark Therapeutics)就是基于该方法开发的。
赛默飞可提供从研发(RUO)到临床生产(CTS)的不同版本的AAV-MAX Helper-Free病毒载体生产系统,助力行业客户无缝扩展到临床生产,同时减少客户自行构建优化全套系统所需的时间和成本。

AAV-MAX 系统特点:
高AAV滴度 — 单位生产体积可生产更多病毒颗粒,降低生产成本
可扩展性 — 悬浮培养系统具有可扩展方案,涵盖从摇瓶到生物反应器的不同规模
简化的工作流程 — 利用无辅助病毒三重转染的精简方案
无动物来源(AOF)组分 — 无动物或人类来源组分,可降低原材料安全风险
克隆化的293 F病毒生产细胞 — 高产量的克隆细胞系;提供完善的文件证明,CTS细胞符合cGMP标准的要求
研究级和GMP选项 — 从早期发现无缝过渡到商业化生产

图1:AAV-MAX Helper-Free生产系统所包含组分。
经优化的完整系统,更高病毒滴度生产
AAV-MAX 系统的各个组分经协同优化,可获得更高病毒滴度,且无需对试剂和方案进行优化。完整的AAV-MAX系统,无论是效率还是病毒生产滴度都要高于替换单个组分后的系统或使用常规的聚乙烯亚胺(PEI)转染试剂的系统(图2)。
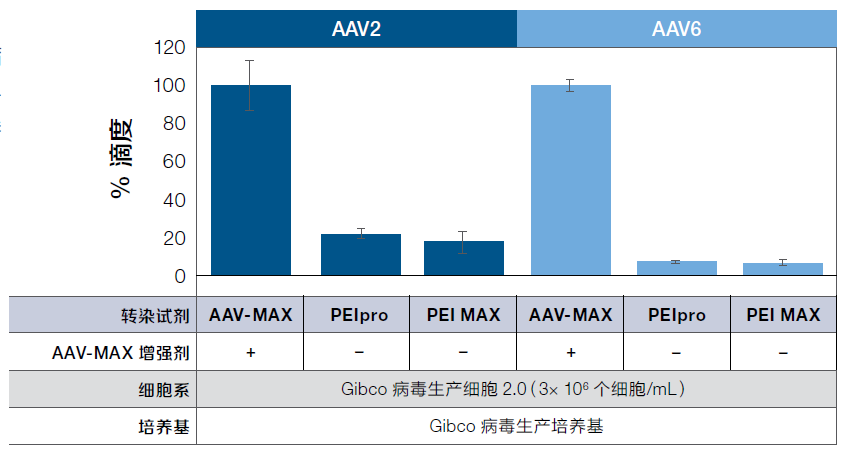
图2:完整的系统可实现最大性能。使用AAV-MAX系统在125 mL摇瓶中以30 mL规模生产AAV2和AAV6。评估整套AAV-MAX系统的性能,并与其他转染试剂进行比较。通过qPCR测量滴度,数据被归一化为整套AAV-MAX系统的滴度。
在多种血清型中具有高滴度
创新的AAV-MAX Helper-Free生产系统是一套完整且经过优化的悬浮系统,可在多种AAV血清型中无缝且有效地生产高滴度AAV载体(图3)。

图3.AAV-MAX系统能够在多种AAV血清型中产生高滴度病毒。本系统用于在125 mL摇瓶中以30 mL规模生产6种AAV血清型。通过qPCR测量滴度。
加速过渡到临床应用
AAV-MAX Helper-Free生产系统提供了从发现到研究和商业开发制造的平稳过渡,提供了一个经过优化的、可扩展的平台,具有研究级和GMP级别选项。图4显示了CTS和RUO系统与两种血清型的等效性,这将使您的研究顺利过渡到cGMP级商业化生产。

图4.研究级(RUO)和CTS试剂之间AAV滴度的比较。在125 mL摇瓶中以30 mL生产规模生产AAV血清型AAV2和AAV6。通过qPCR病毒滴度测量,RUO和CTS AAV-MAX系统试剂的性能被证明具有等效性。
可扩大规模,满足商业化生产需求
现有AAV生产系统面临的挑战包括:较低的滴度,符合cGMP生产标准的质粒DNA成本较高,可扩展性差,缺乏符合cGMP生产标准的试剂。AAV-MAX系统是一套可扩展的悬浮培养平台,能够在大规模培养时仍然保持高病毒滴度(图5和6),该平台的试剂经过了预优化且符合法规要求,专为高AAV滴度生产而开发,让您无惧上述挑战。

图5.本系统在多个生产规模中都可获得高滴度病毒。使用AAV-MAX 系统在四个不同规模的摇瓶中生产AAV2和AAV6。通过qPCR测量滴度,数据被归一化为125 mL摇瓶中 30 mL 生产规模的滴度。
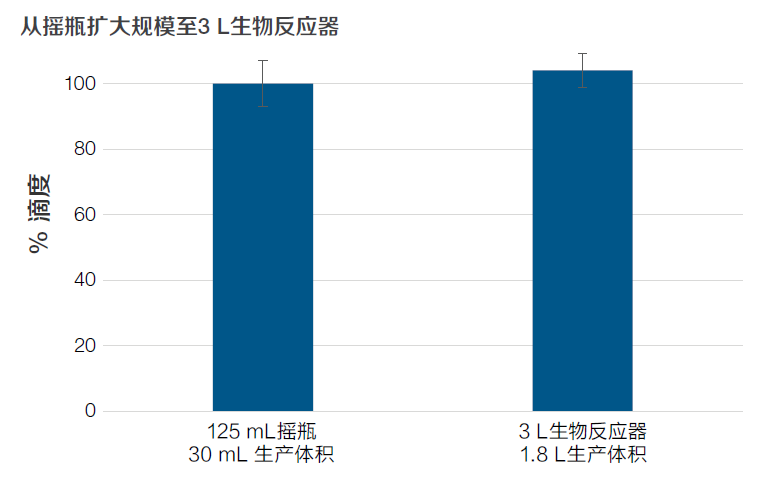
图6.在摇瓶和生物反应器规模下实现高病毒滴度。使用 AAV-MAX系统在125 mL摇瓶(30 mL生产体积)和3 L生物反应器(1.8 L生产体积)中生产 AAV2。通过qPCR测量滴度,数据被归一化为125 mL摇瓶中30 mL生产规模的滴度。
源于 293F 细胞系的克隆细胞
病毒生产细胞2.0:
克隆化的 293F 病毒生产细胞,不含 SV40 大T抗原或没有基因工程化
在化学成分明确的培养基中经过优化,适合用于高密度悬浮培养(>12×10⁶个细胞/mL),具有稳定的可扩展性和传代稳定性(图7-9)
CTS版本细胞可提供完善的文件证明,细胞库符合cGMP标准的要求-按照21 CFR 211和EudraLex第4卷生产,并按照ICH Q5A和ICH Q5D进行表征

图7.病毒生产细胞2.0在多次传代中保持相似的生长曲线。在病毒生产培养基中培养细胞,并在接种后第4天至第7天测量细胞活力和VCD。

图8.病毒生产细胞2.0在多次传代中仍保持约23.5 小时的倍增时间。基于接种后第3天和第4天之间的生长来计算倍增时间。
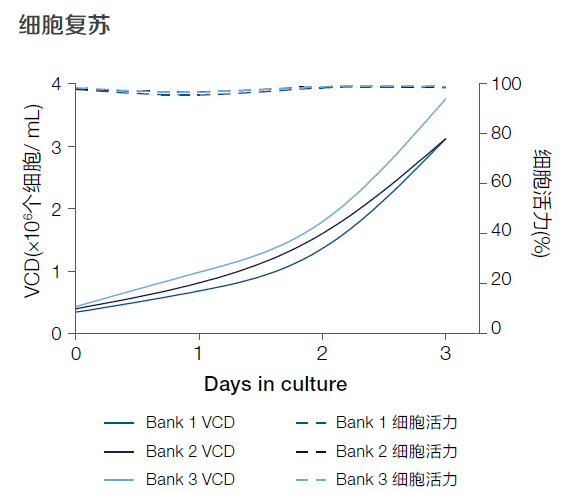
图9.病毒生产细胞2.0在反复冻融后仍保持良好的细胞活力和高活细胞密度(VCD)。解冻细胞,并在解冻后3天监测细胞活力和VCD。
如果您需要了解更多AAV扩大生产的方案、
残留检测方案、系统性能等信息,
请扫码获取,
相关技术需求会有工作人员与您联系!

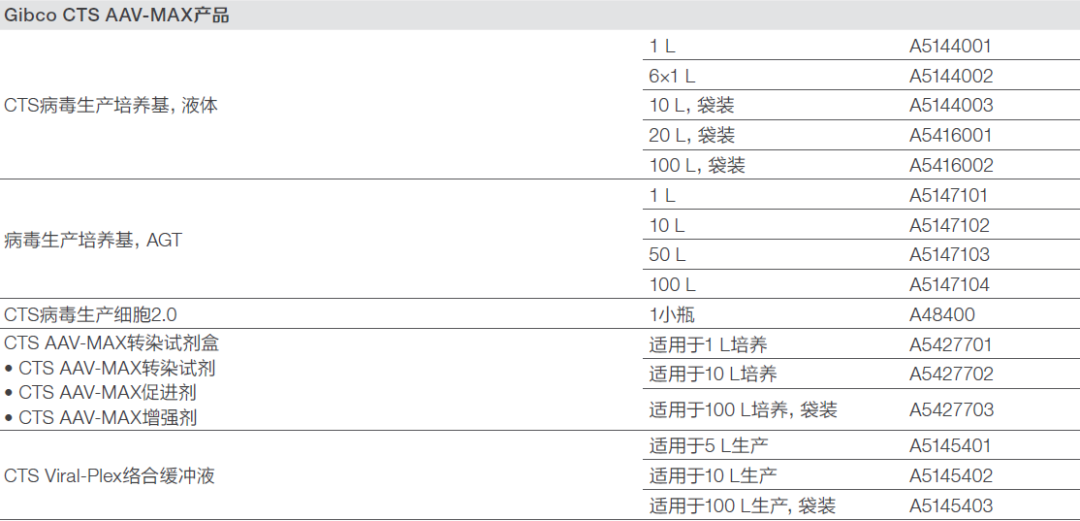
订购信息