新鲜食品中的含氮化合物大多以蛋白质为主体,不同的蛋白质含氮量不同。一般蛋白质含氮量为16%,即1份氮素相当于6.25份蛋白质,此数值称为蛋白质系数。不同种类食品的蛋白质系数不同,如玉米、荞麦、青豆、鸡蛋等为6.25;花生为5.64;大米为5.95;大豆及其制品为5.71;小麦粉为5.70;高粱为6.24;大麦、小米、燕麦等为5.83;牛乳及其制品为6.38;肉与肉制品为6.25;芝麻、向日葵为5.30。所以检验食品中蛋白质时,往往测定总氮量,然后乘以蛋白质换算系数,即可得到蛋白质含量。凯氏定氮法可用于所有动物性、植物性食品的蛋白质含量测定,它的最低检出量为0.05mg氮,相当于0.3mg蛋白质。但因样品中常含有核酸、生物碱、含氮类脂、卟啉以及含氮色素等非蛋白质的含氮化合物,故通常将测定结果称为粗蛋白质含量。
凯氏定氮法由Kieldahl于1833年首先提出,经长期改进,迄今已演变成常量法、微量法、改良凯氏定氮法、自动定氮仪法、半微量等多种方法。
1、常量凯氏定氮法
1)原理
样品与硫酸和催化剂一同加热后消化,使蛋白质分解,其中的碳和氢分别被氧化成二氧化碳和水蒸气逸出,而有机氮转化成氨后与硫酸结合生成硫酸铵,然后在碱性条件下蒸馏使氨游离,用硼酸吸收后再用硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即得蛋白质含量。以甘氨酸为例,该过程的反应方程式如下:
消化 2NH2(CH2)2COOH+13H2SO4→(NH4)2SO4+6CO2+12SO2↑+16H2O
蒸馏 (NH4)2SO4+2NaOH--2H2O+Na2SO4+2NH3↑
吸收 2NH3+4H3BO3-(NH4)2B4O7+5H2O
滴定 (NH4)2B4O7+2HCl+5H2O 2NH4CI+4H3BO3
在消化过程中,浓硫酸具有脱水性和炭化性,使有机物脱水并炭化为碳、氢、氮。浓硫酸又有氧化性,使炭化后的碳氧化为二氧化碳硫酸则被还原成二氧化硫:
2H2SO4-2SO2+2H2O+CO2↑
二氧化硫使氮还原为氨,本身则被氧化为三氧化硫氨随之与硫酸作用生成硫酸铵留在酸性溶液中:
H2SO4+2NH3-(NH4)2SO4
在消化反应中,为了加速蛋白质的分解,缩短消化时间,常加入下列催化剂。
①硫酸钾 加入硫酸钾的目的是为了提高溶液的沸点,加快有机物的分解。硫酸钾与硫酸作用生成硫酸氢钾可提高反应温度,一般纯硫酸的沸点为340℃左右,而添加硫酸钾后,可使温度提高至400℃以上,而且随着消化过程中硫酸不断地被分解,水分不断逸出而使硫酸氢钾的浓度逐渐增大,故沸点不断升高,其反应式如下:
K2SO4+H2SO4--2KHSO4
2KHSO4-K2S04+H2O↑+SO3
但是,硫酸钾的加入量也不能太大,否则消化体系温度过高,又会引起已生成的铵盐发生热分解析出氨而造成损失:
(NH4)2SO4→NH3↑+(NH4)HSO4
2(NH4)HSO4 2NH3↑+2SO3↑+2H2O
2CuSO4 Cu2SO4+SO2↑+O2↑
除硫酸钾外,也可以加入硫酸钠、氯化钾等盐类来提高沸点,但效果不如硫酸钾。
②硫酸铜 硫酸铜在消化中起催化剂的作用。并且,蓝色的硫酸铜溶液还可指示消化终点的到达,以及下一步蒸馏时作为碱性反应的指示剂。
除硫酸铜外,凯氏定氮法中可用的催化剂种类很多,还有氧化汞、汞、硒粉等,但考虑到效果、价格及环境污染等多种因素,应用最广泛的是硫酸铜。另外,使用时常加入少量过氧化氢、次氯酸钾等作为氧化剂以加速有机物的氧化分解。
2)主要仪器
凯氏烧瓶(500mL),定氮蒸馏装置,如图5-9所示。
图5-9凯氏定氮消化、蒸馏装置
1-水力真空管;2一水龙头;3-倒置的干燥管;4一凯氏烧瓶;5,7一电炉;
6.9一铁支架;8一蒸馏烧瓶;10进样漏斗;11-冷凝管:12吸收瓶
3)试剂
①浓硫酸。
②硫酸铜。
③硫酸钾。
④400g/L氢氧化钠溶液。
⑤40g/L硼酸吸收液 称取20g硼酸溶解于500mL热水中,摇匀备用。
⑥甲基红溴甲酚绿混合指示剂 5份2g/L溴甲酚绿95%乙醇溶液与1份2g/L甲基红乙醇溶液临用时混合均匀。混合指示剂在碱性溶液中呈绿色,在中性溶液中呈灰色,在酸性溶液中呈红色。
⑦0.1000mol/L盐酸标准溶液。
4)操作方法
准确称取固体样品0.2~2g(半固体样品2~5g,液体样品10~20mL),小心移入干燥洁净的500mL凯氏烧瓶中,加入研细的硫酸铜0.5g、硫酸钾10g和浓硫酸20mL,轻轻摇匀,安装消化装置,并将其以45°斜支于有小孔的石棉网上。用电炉以小火加热,待内容物全部炭化,泡沫停止产生后,加大火力保持瓶内液体微沸,至液体变蓝绿色透明后,再继续加热微沸30min。冷却,小心加入20mL蒸馏水,待完全冷却后,加入玻璃珠数粒以防蒸馏时暴沸。
将凯氏烧瓶蒸馏装置连好,塞紧瓶口,冷凝管下端插入吸收瓶液面下(瓶内预先装入50mL40g/L硼酸溶液及混合指示剂2~3滴)。放松漏斗夹子,通过漏斗加入70~80mL400g/L氢氧化钠溶液,并摇动凯氏烧瓶,至瓶内溶液变为深蓝色,或产生黑色沉淀,再加入100mL蒸馏水(从漏斗中加入),夹紧漏斗夹子,加热蒸馏至氨全部蒸出(馏出液约250mL即可),将冷凝管下端提离液面,用蒸馏水冲洗管口,继续蒸馏1min,用表面皿接几滴馏出液,以奈氏试剂检查,如无红棕色物生成,表示蒸馏完毕,即可停止加热。将上述吸收液用0.1000mol/L HCl标准溶液直接滴定至由蓝色变为微红色即为终点,记录盐酸溶液用量,同时做试剂空白(除不加样品外,从消化开始操作完全相同),记录空白试验消耗盐酸标准溶液的体积。
5)计算

式中 w——蛋白质的质量分数,%;
c——盐酸标准液的浓度,mol/L;
V0——空白滴定消耗标准液的体积,mL;
V1——试样滴定消耗标准液的体积,mL;
14——氮的毫摩尔质量,g/mmol;
F——氮换算为蛋白质的系数;
m——样品质量,g。
6)说明及注意事项
①所用试剂溶液应用无氨蒸馏水配制。
②消化时不要用强火,应保持和缓沸腾,注意不断转动凯氏烧瓶,以便利用冷凝酸液将附在瓶壁上的固体残渣洗下并促进其消化完全。
③样品中若含脂肪或糖较多时,消化过程中易产生大量泡沫,为防止泡沫溢出瓶外,在开始消化时应用小火加热,并不断摇动;或者加入少量辛醇或液体石蜡或硅油消泡剂,并同时注意控制热源强度。
④当样品消化液不易澄清透明时,可将凯氏烧瓶冷却,加入30%过氧化氢2~3mL后再继续加热消化。
⑤若取样量较大,如于试样超过5g,可按每克试样加5mL的比例增加硫酸用量。
⑥一般消化至呈透明后,继续消化30min即可,但对于含有特别难以氨化的氮化合物的样品,如含赖氨酸、组氨酸、色氨酸、酪氨酸或脯氨酸等时,需适当延长消化时间。有机物如分解完全,消化液应呈蓝色或浅绿色,但含铁量多时,呈较深绿色。
⑦蒸馏装置不能漏气。
⑧蒸馏前若加碱量不足,消化液在蒸馏时不生成氢氧化铜沉淀,此时需再增加氢氧化钠用量。
⑨硼酸吸收液的温度不应超过40℃,否则对氨的吸收作用减弱而造成损失,此时可置于冷水浴中使用。
⑩蒸馏完毕后,应先将冷凝管下端提离液面清洗管口,再蒸1min后关掉热源,否则可能造成吸收液倒吸。
2、微量凯氏定氮法
1)原理
同常量凯氏定氮法。
2)主要仪器
①凯氏烧瓶(100mL)。
②微量凯氏定氮蒸馏装置
3)试剂
①0.0100mol/L盐酸标准溶液。
②20g/L硼酸吸收液:称取20g硼酸溶解于1000mL热水中,摇匀备用。
③其他试剂同常量凯氏定氮法。
4)操作方法
(1)样品消化 精密称取均匀固体样品0.2~2.0g,或半固体样品2~5g或吸取液体样品10~20mL,小心移入100mL干燥的凯氏烧瓶中。向瓶内加入0.2g硫酸铜、3g硫酸钾及一定量的浓硫酸(每克样品加硫酸15mL)将凯氏烧瓶45°倾斜置于电炉上。同常量法消化至消化液呈透明蓝绿色溶液时,再继续加热0.5h,完成消化。待消化液冷至室温后,用蒸馏水干净地转入100mL容量瓶中,并用蒸馏水定容,摇匀,备用。
(2)蒸馏与吸收 连接好微量定氮装置,于水蒸气发生瓶内装水至2/3容积处,加甲基橙指示剂数滴及硫酸数毫升,以保持水呈酸性,加入数粒玻璃珠,加热煮沸水蒸气发生瓶内的水。检查装置的气密性。
在接收瓶内加入25mL20g/L硼酸及2滴混合指示剂,将冷凝管下端插入液面以下。准确量取消化稀释液10mL,经漏斗加入反应管内,用少量蒸馏水冲洗漏斗。经漏斗再加入10mL400g/L氢氧化钠溶液,使呈强碱性,立即夹好漏斗夹,并加少量水于进样漏斗中封口,以防漏气。夹紧废液排出口的螺旋夹,进行水蒸气蒸馏。蒸馏至冷凝管下端的吸收液变为绿色开始计时,继续蒸馏3min后,将冷凝管尖端提离液面再蒸馏1min,用蒸馏水冲洗冷凝管尖端后停止蒸馏。蒸馏结束时,夹紧簧夹,断绝蒸汽,使蒸馏瓶内的溶液吸入回流管中。松开弹簧夹,从漏斗加入蒸馏水40~50mL,再通蒸汽加热回流,将蒸馏瓶洗涤一次备用。
(3)滴定 吸收液用0.0100mol/L盐酸标准溶液滴定至微红色为终点。
(4)空白试验 不加试样,按上述操作作空白试验。
5)计算
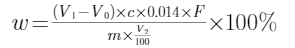
式中 w——蛋白质的质量分数,%;
V0——滴定空白蒸馏液消耗盐酸标准液体积,mL;
V1——滴定样品蒸馏液消耗盐酸标准液体积,mL;
c——盐酸标准液的浓度,mol/L;
0.014——氮的摩尔质量,g/mol;
F——蛋白质系数;
m——样品质量,g;
V2——蒸馏所加样品消化液的量,mL。
6)说明
①蒸馏前给水蒸气发生器内装水至2/3体积处,加甲基橙指示剂数滴及硫酸数毫升,以使其始终保持酸性,这样可以避免水中的氨被蒸出而影响测定结果,同时可以指示因水蒸气气压不足而使氨气发生倒吸溶于水中,使得测定结果偏低。
②在蒸馏时,蒸汽发生要均匀充足,蒸馏过程中不得停火断汽,否则将发生倒吸。
③加碱要足量,操作要迅速;漏斗应采用水封措施,以免氨由此逸出损失。