已执业登记医学检验科(分子生物学专业或者临床细胞分子遗传学专业)可开展的项目名称请参考《医疗机构临床检验项目目录(2013年版医疗机构临床检验项目目录(2013年版)》。项目列举如下:
项目类型 | 项目 | 临床指引 |
肝炎艾滋系列传染病检测产品 | 乙型肝炎病毒HBV-DNA | 乙型肝炎病人抗病毒治疗的辅助诊断,用于监测药物疗效,预测病情,判断预后 |
超敏乙型肝炎病毒 HBV-DNA | 2013年乙肝核酸试剂指导原则指出:乙肝最低检测限不高于30IU/ml。帮助医生更好的判断药物疗效及治疗终点。 | |
丙型肝炎病毒HCV -RNA | 丙型肝炎病人抗病毒治疗的辅助诊断,用于监测药物疗效,预测病情,判断预后 | |
乙型肝炎病毒YMDD基因突变 | 用于乙型肝炎病毒类核苷(酸)类药物耐压基因检测 | |
人类免疫缺陷病毒HIV-RNA | 用于HIV-1感染的辅助诊断,及抗HIV-1药物治疗的临床效果监测。 | |
肿瘤筛查及分流管理 | 15种高危型人乳头瘤病毒HPV分型检测 | 用于体外定性检测女性宫颈脱落上皮细胞样本中的高危型人乳头瘤病毒(HPV)16 型、18 型、31 型、33 型、35 型、 39 型、45 型、51 型、52 型、53 型、56 型、58 型、59 型、66 型、68 型这 15 种型别的核酸 DNA,并鉴别基因型,用于高危型宫颈癌病人的早期辅助诊断及初筛 |
15种高危型不分型检测人乳头瘤病毒HPV检测 | 用于体外定性检测女性宫颈脱落上皮细胞样本中的高危型人乳头瘤病毒(HPV)16 型、18 型、31 型、33 型、35 型、 39 型、45 型、51 型、52 型、53 型、56 型、58 型、59 型、66 型、68 型这 15 种型别的核酸 DNA,并鉴别基因型,用于高危型宫颈癌病人的早期辅助诊断及初筛 | |
人乳头瘤病毒HPV 16/18检测 | 用于高危型宫颈癌病人的早期辅助诊断及初筛分流管理 | |
EBV病毒 EBV-DNA | 鼻咽癌、淋巴瘤等恶性肿瘤的早期诊断 | |
性传播类病原体检测相关 | 沙眼衣原体CT-DNA | 性病的早期辅助诊断及性病高危人群的初筛,不孕不育筛查 |
淋球菌NG-DNA | 性病的早期辅助诊断及性病高危人群的初筛,不孕不育筛查 | |
解脲支原体UU -DNA | 性病的早期辅助诊断及性病高危人群的初筛,不孕不育筛查 | |
人乳头瘤病毒HPV 6/11检测 | 尖锐湿疣等良性下生殖道感染诊断 | |
人类巨细胞病毒 HCMV -DNA | 用于孕妇及婴幼儿巨细胞病毒感染的早期辅助诊断,器官移植病人类巨细胞病毒活动性感染的跟踪监测 | |
单纯疱疹病毒HSV-DNA | 新生儿感染HSV的辅助诊断,性传播疾病筛查 | |
儿科相关 | EBV病毒 EBV-DNA | 儿科传单、慢性活动性EBV早期与活动型感染诊断 |
肠道病毒通用型 EV-RNA | 临床肠道病毒感染的辅助,手足口病的病原体 | |
肠道病毒71型 EV71-RNA | 儿童手足口病病原的鉴别诊断 | |
柯萨奇病毒16型 CA16-RNA | 儿童手足口病病原的鉴别诊断 | |
其它病原体 | 肺炎支原体MP-DNA | 用于MP的早期诊断 |
结核杆菌TB-DNA | 结核病的辅助诊断 | |
甲型流感病病毒Flu-A-RNA | 甲型流感筛查 |
其他可拓展项目
项目名称 | 临床指引 | |
B族链球菌核酸检测 | 优生优育筛查与新生儿败血症/脑膜炎等感染性疾病诊断 | |
白色念珠菌核酸检测 | 快速诊断临床/食品深部白色念珠菌感染 | |
肺炎衣原体核酸检测 | 呼吸道感染疾病肺炎衣原体检测 | |
乙肝病毒分型检测 | 指导临床诊疗方案 | |
丙肝病毒分型检测 | 指导临床诊疗方案 | |
呼吸道合胞病毒核酸检测 | 呼吸道疾病鉴别性病原学诊断 | |
细小脲原体核酸检测 | 性病的早期辅助诊断及性病高危人群的初筛 | |
新布尼亚病毒核酸检测 | 新布尼亚病毒疫情监控,及不明原因发热查因 | |
H1N1流感病毒核酸检测 | H1N1流感疫情监控 | |
幽门螺旋杆菌核酸检测 | 肠道细菌感染诊断 | |
沙门氏菌和志贺菌核酸检测 | 肠道细菌感染诊断 | |
生殖支原体核酸检测 | 性病的早期辅助诊断及性病高危人群的初筛 | |
人型支原体核酸检测 | 性病的早期辅助诊断及性病高危人群的初筛 | |
麻疹和风疹病毒核酸检测 | 优生优育检查 | |
人鼻病毒核酸检测 | 由于鼻病毒引起的呼吸道感染疾病诊断 | |
七项呼吸道病原体核酸检测 | 呼吸道疾病鉴别性病原学诊断 | |
登革热病毒核酸检测 | 登革热病毒筛查公共卫生预防 | |
项目名称 | 临床指引 | |
HLA-B27基因检测 | 作为强直性脊柱炎的早期辅助诊断和鉴别诊断的指标 | |
苯丙酮尿症(PAH)基因检测 | 苯丙酮尿症临床诊断指标 | |
G6PD基因检测 | 人类最常见的酶缺陷病G6PD缺乏症的诊断指标 | |
先天性耳聋基因筛查 | 提高遗传性耳聋检出率,早期发现缺陷胎儿,进行医学干预。 | |
迟发性耳聋基因筛查 | 早期发现新生儿后天性耳聋发病风险,为患者家庭提供生活行为指导。 | |
药物性耳聋基因筛查 | 预防药物性致聋的发生。 | |
项目名称 | 临床指引 | |
NRAS | NRAS突变的晚期黑色素瘤患者对MEK通路抑制MEK162 更敏感。 | |
EGFR | 对非小细胞肺癌病人接受TKI药物如易瑞沙、特罗凯、凯美纳的有效性进行预测 | |
KRAS | 对非小细胞肺癌病人接受TKI药物如易瑞沙、特罗凯、凯美纳的有效性进行预测;对结直肠癌患者接受单克隆抗体药物如爱必妥、维克替比的有效性进行预测 | |
BRAF | 对黑色素瘤患者使用分子靶向药物威罗菲尼片的有效性进行预测;对结直肠直肠癌患者接受单克隆抗体药物如爱必妥、维克替比的有效性进行预测;对乳头状甲状腺癌患者进行辅助诊断及预后判断。 | |
项目类型 | 项目名称 | 临床指引 |
心脏药物相关应用 | 华法林代谢酶基因多态性检测 | FDA:个体基因SNP的检测,帮助确定华法林的最佳初始剂量,最大程度地降低出血风险等不良事件。 |
氯吡格雷抵抗基因多态性检测 | FDA:CYP2C19基因型的检测结果可作为医生调整治疗策略的参考标准,降低病人心血管事件的发生风险 |
从样本到结果的时间计算
基于PCR检测平台的病原体DNA检测项目,从样本提取到检测结果约3小时。
基于PCR检测平台的肿瘤基因DNA检测方面,从样本提取~样本评估~检测结果约5小时。
(根据具体项目配合撰写)列举分类目录如下:
分类 | 制度 |
设备管理 | 设备管理制度 |
仪器设备维护保养程序 | |
仪器设备校准程序 | |
仪器设备操作程序 | |
标本管理 | 标本管理制度 |
临床标本的收集程序 | |
临床标本的保存程序 | |
标本唯一标识编号规则 | |
标本核收、拒收与退单操作程序 | |
标本储存运输操作规程 | |
标本检测 | 临床标本的处理(核酸纯化)程序 |
核酸扩增及产物分析检测的操作程序 | |
结果报告管理 | 结果报告管理制度 |
修改和补发实验报告的管理制度 | |
试剂管理与评价 | 方法学性能评估管理制度 |
试剂管理制度 | |
试剂的质检操作程序 | |
实验室耗材管理 | 实验室消耗品购买、验收和贮存程序 |
质量管理 | 室内质量控制程序 |
室间质评管理制度 | |
投诉处理 | 抱怨处理程序。 |
纠正和预防措施管理制度 | |
生物安全与防护 | 实验室的清洁程序 |
消毒办法与消毒用品使用操作规程 | |
医疗废物管理制度 | |
医疗废物流失、遗漏、扩散紧急预案 | |
职业暴露防护管理制度 | |
职业暴露应急预案 | |
标本溢洒处理流程 |
5、实验室的仪器、试剂及人员要求
仪器、试剂要求
仪器:必须三证齐全
试剂:必须NMPA批准
项目:新开展检测项目应有相应临床科室出具的评估报告;在技术审核前应进行方法学验证
实验人员要求
必须持有PCR上岗合格证,PCR 实验室操作人员至少2名
通过参加省临床检验中心组织的临床基因扩增实验室技术人员上岗培训班获得上岗证,培训班内容包括理论培训和实验培训。
需要具备资格、培训、技能与业绩档案
需要有培训记录及实施记录:每人需有年度培训内容(包括外出学习、进修、内部质量手册学习、业务学习及新项目开展学习等)。
三、PCR实验室区域信息化平台平台建设
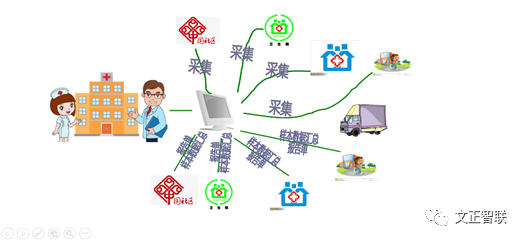
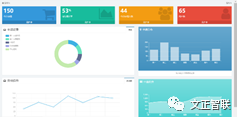
通过对市/县医疗机构PCR需求资源整合,以区域分子诊断中心实验室检测资源和检验信息共享为基础,建立区域检验数据中心,承载区域医疗卫生服务机构检验数据的采集、存储、交换、分析、应用和管理等,为各级医疗机构提供检验报告的集中发布与共享,检验质量的实时监控与评价,外送样本检验申请与样本物流管理,检验大数据分析与辅助决策支持等系统,为各医疗机构和管理部门提供检验方面的决策支持。
实现检验医嘱开立、样本采集与条码化、样本交接管理、样本物流过程管理、申请单信息传递、实验室检验、检验报告发布等方面提供信息化服务
图1:区域信息化互联云平台
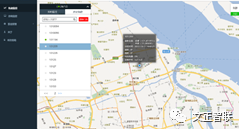
图2:样本冷链物流监控系统
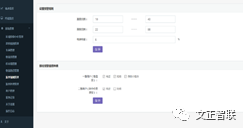
图3:试剂耗材管理系统