简介
VSV-G-假型自我灭活慢病毒载体是不可或缺的生物实验工具之一,与之前的γ-逆转录病毒载体不同的是,慢病毒载体可转导非分裂细胞,并可携带更多的转基因盒,在细胞中的转基因表达时间也更长,即可获得更高的滴度,而其遗传毒性相对较低。
一般情况下产毒细胞上清液中的载体滴度足以转导常规细胞系,但原代细胞较难转导,需要进行载体浓缩以获得较高浓度。此外,一些载体因整合了会降低滴度的遗传元件,且大多数细胞类型也不耐受产毒细胞生长培养基或其分泌蛋白,所以浓缩及清洗是慢病毒载体使用的必要步骤。
超速离心是病毒颗粒浓缩的常用方法之一,但其浓缩系数较低,每次处理量也偏小,且繁琐的多步操作会降低病毒颗粒回收率。离心过滤是相对较简单的浓缩方法,但过滤器本身会捕获截留大量载体,造成损耗。相较而言,切向流过滤(TFF)操作简单,损耗低,且可通过洗滤过程有效降低产毒细胞代谢物及分泌蛋白,但传统的一步式TFF浓缩程度仅可达50-100倍,本实验使用两步TFF,成功将5.5L 慢病毒载体原液浓缩至1mL左右,且回收率高达97%以上。而对终产物的质量分析显示,浓缩的慢病毒载体可有效转导原代人CD34+造血干/祖细胞和原代人纤维母细胞,且无明显毒性。
实验
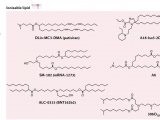
实验使用含pCCL载体质粒、gag/pol表达质粒及囊膜表达质粒pMD.G(VSV-G)的转染混合液转染293T细胞,并于转染后进行丁酸钠诱导,培养一定时间后,分两次回收含LV培养基,过0.8μm过滤器,滤液保存于无菌容器。
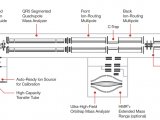
切向流过滤使用KrosFlo研发用IIi切向流过滤系统(产品编号:SYR2-U20-01N),第一步操作时,系统配用流路1(FP1,产品编号:EZ-M1-500S-260-01N-1,含500kD中空纤维过滤器(纤维数量320,纤维内径0.5mm,膜表面积615cm2)),第二步操作时,系统配用流路2(FP2,产品编号:EZ-CHIL07-01-1,含500kD中空纤维过滤器(纤维数量12,纤维内径0.5mm,膜表面积40cm2)。


过滤前先检查流路(FP1)完整性,用DPBS完全润湿流路后,运行系统,直到DPBS排干,关闭端口和阀门,运行泵,直到入口压力达到5psi左右,打开滤液端口,由于空气不能渗过润湿的过滤器纤维,如组件完整,则压力降不应超过0.01psi/s。
通过完整性测试后,开始浓缩含LV培养基。整个过程中,监测入口压力,并维持为6psi以下。第一步操作可将5.5L料液浓缩至50mL,即浓缩100倍左右。浓缩的载体再用1000mL含胎牛血清的洗滤缓冲液进行恒量洗滤。之后,将系统流路更换为FP2,通过完整性测试后,将第一步获得的50mL浓缩液进一步浓缩至1mL,即总浓缩达5000倍。该步入口压力维持为9psi以下
随后,通过HT-29细胞载体转导实验确认滴度,并使用多重实时PCR技术进行绝对定量分析。同时,以终浓度载体转导原代人CD34+造血干/祖细胞,确认浓缩后载体的转导效力。此外,构建针对诱导多能性干细胞(iPSC)生成的复合STEMCCA 载体,以相同的方法进行浓缩,检测其转导和重编程原代人纤维母细胞的能力。
结果
使用TFF进行LV浓缩可获得极高的浓缩系数和回收率,且对浓缩后LV的冻融实验显示,终产物具有良好的稳定性。
为测试浓缩LV的质量,进行了原代人CD34+造血干/祖细胞的转导实验,结果显示,转导非常成功,且随载体浓度的增加,转导成功率亦明显上升,而无明显毒性。而在原代人纤维母细胞转导实验中,含有高效STEMCCA元件的载体可有效转导并重编程原代人纤维母细胞,形成诱导多能性干细胞,且成功率随载体浓度增加而提高。

讨论
使用两步切向流过滤可以高倍数、高回收率地浓缩LV,工艺稳定,重复性好。针对CD34+的转导和表达实验表明浓缩后产物无明显毒性,而高浓度STEMCCA载体制备及诱导实验证明,该工艺可用于大规模复杂载体的生产和浓缩。