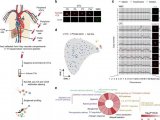
慢性炎症在肝细胞癌(HCC)中起着核心作用,但是尚不清楚肝细胞在肿瘤相关炎症中的作用。
2021年5月25日,南京大学孙倍成及林安宁共同通讯在Immunity 在线发表题为”The zinc finger protein Miz1 suppresses liver tumorigenesis by restricting hepatocyte-driven macrophage activation and inflammation“的研究论文,该研究报告锌指转录因子Miz1限制肝细胞驱动的炎症来抑制HCC,而与其转录活性无关。
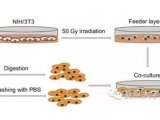
在HCC小鼠模型和相当一部分HCC患者中,Miz1被下调。小鼠中肝细胞特异的Miz1缺失产生了肝细胞的一个独特亚组,产生促炎细胞因子和趋化因子,使肿瘤浸润巨噬细胞的极化偏向促炎表型,从而促进HCC。从机制上讲,Miz1螯合了MTDH,阻止MTDH促进转录因子核因子κB(NF-κB)激活。在一部分HCC患者中也观察到了促炎性细胞因子产生肝细胞的不同亚组。此外,Miz1表达与HCC患者的疾病复发和不良预后成反比。总之,该研究将Miz1识别为一种肿瘤抑制因子,可阻止肝细胞驱动HCC炎症。

肝细胞癌(HCC)是世界范围内与癌症相关的死亡的第三大主要原因,通常由暴露于致癌物,感染肝炎病毒(乙型肝炎病毒[HBV]或丙型肝炎病毒[HCV]),脂肪肝疾病等,然后是引起肝损害的纤维化和肝硬化。慢性炎症通过促进肝肿瘤的发生和发展与HCC的发展有因果关系。
慢性HBV和HCV感染,酒精,致癌物DNA损伤和肥胖等主要危险因素是造成HCC炎性肿瘤微环境(TME)的原因。但是,肿瘤肝细胞对炎症的贡献尚不十分清楚。坏死性肝细胞死亡促进炎症,继而刺激化学HCC小鼠模型中存活的肿瘤细胞的代偿性增生。相比之下,凋亡转化的肝细胞在炎症相关的HCC小鼠模型中抑制了炎症。尚不清楚活的肝细胞是否促成炎症,如果是,则其机理是什么。
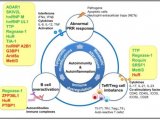
转录因子核因子κB(NF-κB)通过诱导其靶基因表达而成为细胞存活,炎症和免疫反应的关键调节剂,其靶蛋白参与免疫反应,炎症,病毒感染,细胞存活和肿瘤发生。NF-κB在被多种细胞外刺激激活后被IκB激酶复合物(IKK)激活。IKK还使NF-κB反式激活亚基RelA磷酸化,以增强NF-κB的转录活性。巨噬细胞NF-κB在肝肿瘤发生中具有促进肿瘤的功能。矛盾的是,肝细胞中的NF-κB通常在HCC动物模型和大部分HCC患者中被激活,但在某些情况下,NF-κB被感染的病毒灭活。肝细胞NF-κB在HCC进程中的非细胞死亡作用尚不清楚。
癌蛋白Metadherin(MTDH)参与了多种肿瘤发生,例如HCC。MTDH和RelA之间的相互作用促进了由肿瘤坏死因子α(TNF-α)诱导的NF-κB核易位。MTDH可以被IKK在Ser297(鼠)或Ser298(人类)上磷酸化,只有磷酸化的MTDH在其某些靶基因启动子上充当NF-κB的共激活因子。缺乏Mtdh的小鼠对二乙基亚硝胺(DEN)诱导的HCC的敏感性降低,并且肝细胞和巨噬细胞的NF-κB活化降低,MTDH的表达与不良的HCC预后相关。尚不知道在肝癌和其他疾病中如何调节MTDH促进NF-κB的活化。
锌指转录因子Miz1具有一个N末端痘病毒和锌指(POZ)结构域,这对它的转录活性至关重要,在C末端有13个锌指。Miz1或其POZ结构域的丧失导致小鼠胚胎致死性与大量细胞凋亡相关,尚无已知机制。Miz1可以激活许多与细胞周期阻滞,自噬和膜运输有关的基因并抑制许多促炎性细胞因子的表达。Miz1与MYC,Bcl-6或Gif-1的复合物可抑制许多参与细胞周期阻滞的基因的表达,从而促进某些类型的肿瘤发生。Miz1也位于细胞质中,可以抑制TNF-α诱导的JNK1活化,炎症和细胞死亡。然而,关于Miz1是否以转录非依赖性方式调控肿瘤发生的了解甚少。在这里,该研究报道细胞质Miz1通过阻止MTDH促进肝细胞NF-κB活性来抑制肝脏肿瘤发生,从而限制了肝细胞驱动的巨噬细胞的活化和炎症。
该工作由南京大学医学院附属鼓楼医院,南京大学现代生物研究院,美国芝加哥大学和中国科学院生物化学与细胞生物学研究所的研究人员共同完成。工作得到了科技部、国家自然科学基金委的经费支持。