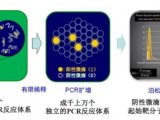
PCR技术可用于:(1)检验感染性疾病是否处于隐性或亚临床状态;(2)有效检测癌基因的突变,准确检测癌基因的表达量;(3)临床应用于检测地中海贫血的基因突变。
| 实验方法原理 | 基本原理类似于DNA的天然复制过程,其特异性依赖于与靶序列两端互补的寡核苷酸引物。 PCR由变性--退火--延伸三个基本反应步骤构成: ②模板DNA与引物的退火(复性):模板DNA经加热变性成单链后,温度降至55℃左右,引物与模板DNA单链的互补序列配对结合; ③引物的延伸:DNA模板--引物结合物在Taq酶的作用下,以dNTP为反应原料,靶序列为模板,按碱基配对与半保留复制原理,合成一条新的与模板DNA 链互补的半保留复制链。 重复循环变性--退火--延伸三过程,就可获得更多的“半保留复制链”,而且这种新链又可成为下次循环的模板。每完成一个循环需2~4分钟, 2~3小时就能将待扩目的基因扩增放大几百万倍。 |
|---|---|
| 实验材料 | |
| 试剂、试剂盒 | |
| 仪器、耗材 | |
| 实验步骤 | 一、标准的PCR反应体系 10×扩增缓冲液 10 ul 4种dNTP混合物 各200 umol/L 引物 各10~100 pmol 模板DNA 0.1~2 ug Taq DNA聚合酶 2.5 u Mg2+ 1.5 mmol/L 加双或三蒸水至 100 ul 二、PCR引物设计
(4)两个引物之间不应存在互补序列,尤其是避免3 ′端的互补重叠。 (5) 引物与非特异扩增区的序列的同源性不要超过70%,引物3′末端连续8个碱基在待扩增区以外不能有完全互补序列,否则易导致非特异性扩增。 (6)引物3‘端的碱基,特别是最末及倒数第二个碱基,应严格要求配对,最佳选择是G和C。
7. 循环次数 :一般为25 ~30次。循环数决定PCR扩增的产量。模板初始浓度低,可增加循环数以便达到有效的 扩增量。但循环数并不是可以无限增加的。一般循环数为30个左右,循环数超过30个以后,DNA聚合酶活性逐渐达到饱和,产物的量不再随循环数的增加而增加,出现了所谓的“平台期”。
|
| 注意事项 | 1. 由于PCR反应灵敏度很高,因此要特别主意防止DNA污染的发生。样品间的相互污染可能产生假阳性结果,特别是将PCR技术应用到临床病原菌感染确定中。 2. 如果是公用的、没有密码保护的PCR仪,经常检查PCR仪上的程序正确与否。 3. 不使用过量试剂“less is usually better (more specific)”。 4. 试剂购回后应分装成小份使用,这样一旦有污染发生,可以立即丢弃污染的试剂,不会造成大的损失;试剂分装也有助于减少反复冻融次数(例如dNTPs对反复冻融敏感)。 5. 加完所有试剂后用枪头吹打几次或稍微涡旋或轻弹管壁以保证充分混匀。 6. 使用阴性对照检查污染的发生。 7. 使用阳性对照(能良好扩增的样本)。 8. 电泳时使用DNA分子量标准品(指示是否PCR失败或条带跑出凝胶或拍照系统失败)。 9. 当扩增很长的、GC含量高的模板时或容易产生二级结构的模板时适量使用添加剂(glycerol, formamide, NMP使变性和退火温度降低几度;glycerol也可起到稳定聚合酶活性的作用;DMSO 减少二级结构的发生,并通过减弱非特异性引物结合的稳定性,提高反应的特异性)。 10. 不使用带有自动除霜功能的冰箱存储酶(避免反复冻融),每次取酶时都使用新的枪头酶,酶使用后应立即放回冰箱。酶要在加完缓冲液后再加,直接将酶加入水中可能导致酶变性失活。 11. PCR产物的电泳检测时间,一般为48 h以内,有些最好于当日电泳检测,大于48h后带型不规则甚致消失。 收起 |
| 其他 | 一、 PCR反应的关键环节 1. 假阴性,不出现扩增条带 (1)模板原因 (2)酶失活
(3)引物
(4)Mg2+浓度
(5)反应体积的改变 (6)物理原因 (7)靶序列变异 2. 假阳性,出现的PCR扩增条带与目的靶序列条带一致,有时其条带更整齐,亮度更高。 (1)引物设计不合适 (2)靶序列或扩增产物的交叉污染 3. 出现非特异性扩增:PCR扩增后出现的条带与预计的大小不一致,或大或小,或者同时出现特异性扩增带与非特异性扩增带。
(4) PCR循环次数 过多有关。
4. 出现片状拖带或涂抹带 (1)原因
④ Mg2+浓度过高。
|